|
|
მთავარი - ბიბლიოთეკის შესახებ - ელ.რესურსები |



 |
ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის სახელმძღვანელო |
|
|
| საბიბლიოთეკო ჩანაწერი: |
| თემატური კატალოგი ადამიანის უფლებები, განათლება|სახელმძღვანელოები |
| თარიღი: 2009 |
| კოლექციის შემქმნელი: სამოქალაქო განათლების განყოფილება |
| აღწერა: Published by the World Health Organization in 2009 under the title Guidelines for the psychosocially assisted pharmacological treatment of opioid dependence © World Health Organization, 2009 The Director General of the World Health Organization has granted translation rights for an edition in Georgian to the Research Institute on Addiction, which is solely responsible for the Georgian edition. This report is published in the frame of the project „Development of Human Resources, Evidence Base and Quality Standards in Addictology in Georgia“, funded by EC, within the TEMPUS funding mechanism 544219-TEMPUS-1-2013-1CZ-TEMPUS-SMHES (2013 – 4566 / 001-001). This project has been funded with support from the European Commission. This publication reflects the views only of the authors, and the Commission cannot be held responsible for any use which may be made of the information contained therein. წინამდებარე გამოცემა დაფინანსებულია ევროკომისიის TEMPUS-ის დაფინანსების მექანიზმის გამოყენებით, პროექტის „ადამიანური რესურსების, მტკიცებულებათა ბაზისა და ხარისხის სტანდარტების განვითარება საქართველოს ადიქტოლოგიაში“ ფარგლებში 544219-TEMPUS-1-2013-1CZ-TEMPUS-SMHES (2013 – 4566 / 001 – 001). ევროკომისიის მიერ ამ გამოცემის მხარდაჭერა არ ნიშნავს მისი შინაარსის გაზიარებას, რომელიც მხოლოდ ავტორების მოსაზრებებს ასახავს. აქედან გამომდინარე, ევროკომისია პასუხს არ აგებს ამ პუბლიკაციის შინაარსზე |
 |
1 * * * |
▲back to top |
ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის სახელმძღვანელოებში განხილულია მეთადონის, ბუპრენორფინის, ნალტრექსონის და კლონიდინის გამოყენება ფსიქოსოციალურ დახმარებასთან ერთად ჰეროინზე ან სხვა ოპიოიდებზე დამოკიდებული ადამიანების მკურნალობისას. ლიტერატურის სისტემატიზებულ მიმოხილვასა და მტკიცებულების ხარისხის შესაფასებლად GRADE-ის მეთოდზე დაყრდნობით ეს სახელმძღვანელოები შეიცავს მკურნალობის სისტემების ორგანიზებასთან, პროგრამების მართვასთან და ოპიოიდებზე დამოკიდებული ადამიანების მკურნალობასთან დაკავშირებულ მრავალ სპეციფიკურ რეკომენდაციას.
სხვადასხვა ქვეყანაში მოღვაწე მსოფლიოში აღიარებული ექსპერტების მიერ შემუშავებული ოპიოიდური დამოკიდებულების ფსიქო-სოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის სახელმძღვანელოები საინტერესო იქნება ჯანდაცვის პოლიტიკის განმსაზღვრელების, პროგრამის მენეჯერების და კლინიცისტებისთვის ყველგან, სადაც ცდილობენ ოპიოიდური დამოკიდებულების ტვირთის შემცირებას.
 |
2 მადლობის სიტყვა |
▲back to top |
ეს სახელმძღვანელო შემუშავდა ჯანდაცვის მსოფლიო ორგანიზაციის (ჯანმო) ფსიქიკური ჯანმრთელობის და წამალდამოკიდებულების დეპარტამენტის მიერ, გაეროს ნარკოტიკებისა და დანაშაულის ოფისთან (UNODC) თანამშრომლობით და მათი ტექნიკური ექსპერტების მონაწილეობით. სახელმძღვანელო შეიქმნა ნარკოტიკების კონტროლის საერთაშორისო საბჭოს (INCB) და ჯანმოს სხვა დეპარტამენტების კონსულტაციების საფუძველზე. ჯანმო მადლობას უხდის UNODC-ს და გაეროს აივ/შიდსის ერთიან პროგრამას (UNAIDS) ამ პროექტისთვის გაწეული ფინანსური დახმარებისთვის და, ასევე,
სახელმძღვანელოზე მომუშავე ჯგუფს:
მარინა დავოლი
მაკოორდინირებელი რედაქტორი, კოკრეინის ჯგუფი ეპიდემიოლოგიის განყოფილება; ლაციოს რეგიონის ეპიდემიოლოგიური განყოფილება; რომი, იტალია
მაიკლ ფარელი
კონსულტანტი ფსიქიატრი; წამალდამოკიდებულების ეროვნული ცენტრი; ფსიქიატრიის ინსტიტუტი და მოდსლის საავადმყოფო; ლონდონი, გაერთიანებული სამეფო
დევიდ ფილინი
მედიცინის ასოცირებული პროფესორი; იელის უნივერსიტეტის მედიცინის სკოლა; ამერიკის შეერთებული შტატები
ლი ჯიანჰუა
დირექტორის მოადგილე; იუნანის წამალდამოკიდებულების ინსტიტუტი, ჩინეთი
რატნა მარდიატი
ფსიქიატრი; სამედიცინო სამსახურის გენერალური დირექტორი; ჯაკარტა, ინდონეზია
რიჩარდ მატიკი
დირექტორი; ნარკოტიკების და ალკოჰოლის კვლევითი ცენტრი; ახალი სამხრეთ უელსის უნივერსიტეტი; სიდნეი, ავსტრალია
ელენა მედინა-მორა
დირექტორი; ეპიდემიოლოგიური და ფსიქოსოციალური კვლევა; ფსიქიატრიის ეროვნული ინსტიტუტი; მეხიკო
ფრედ ოვიტი
კონსულტანტი ფსიქიატრი; ეროუს სამედიცინო ცენტრი; ნაირობი, კენია
აფარინ რაჰიმი-მოვაგარი
წამალდამოკიდებულების კვლევების; ირანის ეროვნული ცენტრი; თეირანის როუს სამედიცინო ცენტრი; ნაირობი, კენია
რაჯატ რეი
წამალდამოკიდებულების მკურნალობის ეროვნული ცენტრის ხელმძღვანელი; ინდოეთის სამედიცინო მეცნიერების ინსტიტუტი; ნიუ დელი, ინდოეთი
ენტონი ჯ. სმიტი
საპატიო პროფესორი; კლინიკური ფარმაკოლოგია; ნიუკასლის საავადმყოფო; ავსტრალია
ამბროს უხტენჰაგენი
საზოგადოებრივი ჯანმრთელობის და ნარკომანიის კვლევითი ინსტიტუტის პრეზიდენტი; ციურიხი, შვეიცარია
დამკვირვებლები
ევროსაბჭო
გაბრიელ ველე-სტრანდი
მთავარი მრჩეველი ჯანმრთელობის და სოციალური საკითხების; ნორვეგიის დირექტორატი; ნორვეგია
ნარკოტიკების კონტროლის საერთაშორისო საბჭოს სამდივნო
პაველ პაჩტა
ნარკოტიკების კონტროლის განყოფილების ხელმძღვანელი; ვენა, ავსტრია
კარმენ სელვა-ბართლომე
ფსიქოტროპების კონტროლის განყოფილების ხელმძღვანელი (2007 წლის სექტემბრამდე); ვენა, ავსტრია
მარგარეტ ერენფელდნერი
ფსიქოტროპული პრეპარატების კონტროლის სექცია (2007 წ. 1 ოქტომბერი); ვენა, ავსტრია
გაერთიანებული ერების ნარკოტიკების და დანაშაულის კონტროლის ოფისის სამდივნო
ხუანა ტომას-როსელო
წამალდამოკიდებულების მკურნალობის მრჩეველი, გლობალური პრობლემების განყოფილება; ვენა, ავსტრია
ჯანმრთელობის მსოფლიო ორგანიზაციის გამგეობა, ფსიქიკური ჯანმრთელობის და წამალდამოკიდებულების დეპარტამენტი
ვლადიმირ პოზნიაკი
კოორდინატორი
ნიკოლას კლარკი
სამედიცინო ოფიცერი
ჰანუ ალჰო
დროებითი მრჩეველი
აივ-ის დეპარტამენტი
ანეტ ვესტერი
ტექნიკური ოფიცერი
ჯანმრთელობის სისტემების დაფინანსების დეპარტამენტი
დან ქიშოლმი
ეკონომისტი
სამედიცინო პოლიტიკის და სტანდარტების დეპარტამენტი
სიუ ჰილი
სამედიცინო ოფიცერი
ნიკოლა მაგრინი
სამედიცინო ოფიცერი
ჯანმო მადლიერებით იხსენიებს სხვა მონაწილეებს და, ასევე, ქვემოთ ჩამოთვლილ სპეციალისტებს მოსამზადებელი მასალების შექმნასა და განხილვაში შეტანილი წვლილისთვის:
ლაურა ამატო, ეპიდემიოლოგიის დეპარტამენტი, Azienda Sanitaria Locale „E“, რომი, იტალია.
მაიკ ეშტონი, მონაცემები ნარკოტიკებისა და ალკოჰოლის შესახებ, გაერთიანებული სამეფო.
ანა მარია ბარგაგლი, ეპიდემიოლოგიის დეპარტამენტი, Azienda Sanitaria Locale „E“, რომი, იტალია.
ჯეიმს ბელი, ნარკომანიის ეროვნული ცენტრი, ლონდონი, გაერთიანებული სამეფო.
ადრიან კარტერი, ქუინსლენდის თავის ტვინის ინსტიტუტი, ქუინსლენდის უნივერსიტეტი, ავსტრალია.
ზანგ კუნმინი, იუნანის ნარკომანიის ინსტიტუტი, კუნმინგი, იუნანი, ჩინეთი.
კრის დორანი, ნარკომანიის და ალკოჰოლიზმის კვლევის ეროვნული ცენტრი, ახალი სამხრეთ უელსის უნივერსიტეტი, ავსტრალია.
კოლინ დრამონდი, სენტ ჯორჯის უნივერსიტეტი, ლონდონი, გაერთიანებული სამეფო.
რალფ ედვარდსი, დირექტორი, უპსალას მონიტორინგის ცენტრი, შვედეთი.
გებრიელ ფიშერი, ვენის სამედიცინო უნივერსიტეტი, ავსტრია.
ენდი გრეი, კუაზულუ-ნატალის უნივერსიტეტი, დურბანი, ჩრდილოეთ აფრიკა.
უეინ ჰოლი, მოსახლეობის ჯანმრთელობის სკოლა, ქუინსლენდის უნივერსიტეტი, ავსტრალია.
ს. კატიმანი, ნარკოდამოკიდებულების მკურნალობის ეროვნული ცენტრი, სრულიად ინდოეთის სამედიცინო მეცნიერებათა ინსტიტუტი, ნიუ დელი, ინდოეთი.
ნინა კოპფი, ფსიქიატრიის დეპარტამენტი, ვენის სამედიცინო უნივერსიტეტი, ავსტრია.
ტ. ლაჟევიჩი, საზოგადოებრივი ჯანმრთელობის და ნარკომანიის კვლევითი ინსტიტუტი, ციურიხის უნივერსიტეტი, შვეიცარია.
ლიზა მარში, ნარკოტიკების მოხმარების და აივ-ის კვლევის ცენტრი, ეროვნული განვითარების და კვლევის ინსტიტუტები, ნიუ იორკი, აშშ.
სილვია მინოზი, ეპიდემიოლოგიის დეპარტამენტი, Azienda Sanitaria Locale „E“, რომი, იტალია.
ლუბომირ ორკულიკა, წამალდამოკიდებულების ინსტიტუტი, წამალდამოკიდებულების მკურნალობის ცენტრი, ბრატისლავა, სლოვაკეთის რესპუბლიკა.
კატერინ პერიმანი, სენტ ჯორჯის უნივერსიტეტი, ლონდონი, გაერთიანებული სამეფო.
კარლო პერუჩი, ეპიდემიოლოგიის დეპარტამენტი, Azienda Sanitaria Locale „E“, რომი, იტალია.
ლი პეიკაი, იუნანის ნარკომანიის ინსტიტუტი, კუნმინგი, იუნანი, ჩინეთი.
იურგენ რემი, საზოგადოებრივი ჯანმრთელობის და ნარკომანიის კვლევითი ინსტიტუტი, ციურიხის უნივერსიტეტი, ნარკომანიის და მენტალური ჯანმრთელობის ცენტრი, ტორონტო, კანადა.
ჰ. კ. შარმა, წამალდამოკიდებულების მკურნალობის ეროვნული ცენტრი, სრულიად ინდოეთის სამედიცინო მეცნიერებათა ინსტიტუტი, ნიუ დელი, ინდოეთი.
სიმონა ვეჩი, ეპიდემიოლოგიის დეპარტამენტი, Azienda Sanitaria Locale „E“, რომი, იტალია.
სახელმძღვანელოზე მომუშავე ჯგუფის ინტერესების დეკლარაცია
მაიკლ ფარელმა გვაცნობა, რომ იგი არის გაერთიანებულ სამეფოში წამალდამოკიდებულების სახელმძღვანელოს ეროვნული ჯგუფის წევრი. გასამრჯელოს იღებს მოგზაურობისა და ხარჯებისათვის Reckitt Benckiser-ის და Schering Plough-ის მიერ ორგანიზებულ შეხვედრებზე (თითოეულ შემთხვევაში <1000 დოლარი) ლექციების წასაკითხად. ასევე, ადელაიდის უნივერსიტეტსა და კალიფორნიის უნივერსიტეტთან თანამშრომლობით Reckitt Benckiser-ისგან იღებს შეუზღუდავ საგანმანათლებლო გრანტს (ადელაიდის უნივერსიტეტის საშუალებით) სამხრეთ-აღმოსავლეთ აზიაში წამალდამოკიდებულების საკითხებისათვის (გრანტიდან ყოველგვარი პირადი ფინანსური სარგებლის გარეშე).
დევიდ ფილინის ინფორმაციით, იგი, როგორც ექსპერტი, კონსულტაციებს უწევს წამალდამოკიდებულების მკურნალობასთან დაკავშირებულ კონგრესის პრესკონფერენციებს და შეერთებული შტატების წამალდამოკიდებულების მკურნალობის ცენტრს ჰონორარის გარეშე აწვდის მიმოხილვებს მეთადონის, ბუპრენორფინის და ბუპრენორფინი/ნალოქსონის შესახებ.
რიჩარდ მატიკმა გვაცნობა, რომ, როგორც ნარკომანიის და ალკოჰოლიზმის ეროვნული კვლევითი ცენტრის დირექტორი, იგი იძლევა კონსულტაციებს და აკეთებს საჯარო განცხადებებს წამალდამოკიდებულების მკურნალობის შესახებ; Reckitt Benckiser-ისგან იღებს დახმარებას თავისი კვლევითი განყოფილებისთვის (დაახლოებით 400 000 ავსტრალიური დოლარი 3 წლის განმავლობაში), მაგრამ პირადი ფინანსური ინტერესის გარეშე; ასევე, წამალდამოკიდებულების კვლევისთვის დაფინანსებას იღებს ავსტრალიის ეროვნული ჯანმრთელობის და სამედიცინო კვლევის საბჭოდან (150 000 ავსტრალიური დოლარი).
რაჯატ რეიმ შეგვატყობინა, რომ იგი არის ინდოეთის ჯანდაცვის სამინისტროს ექსპერტთა ჯგუფის წევრი ოპიატების ჩანაცვლებითი თერაპიის საკითხებში; 2005 წელს წარმოადგინა სამეცნიერო შრომა, რის საფუძველზეც მიიღო დაფინანსება თავისი კვლევითი განყოფილებისთვის Rusan Pharmaceuticals-ისგან (350 000 ავსტრალიური დოლარი), კერძოდ, ბუპრენორფინთან დაკავშირებული კვლევისთვის პირადი ფინანსური დაინტერესების გარეშე.
ამბროს უხტენჰაგენმა გვაცნობა, რომ დაახლოებით 3 წლის წინ მან Schering Plough-ისგან მიიღო დაფინანსება ლიტერატურის მიმოხილვისთვის.
მარინა დავოლის, რატნა მარდიატის, აფარინ რაჰიმი მოვაგარს, ფრედ ოვიტის, ემილის სუბატას, ენტონი სმიტს და გაბრიელე ველე-შტრანდს ინტერესთა კონფლიქტის შესახებ არ განუცხადებიათ.
ორგანიზაციები, რომლებმაც განიხილეს სახელმძღვანელოს პროექტი:
ჯანმოს რეგიონული ოფისები.
ჯანმოს კოლაბორაციული ცენტრები:
- ნარკომანიის კვლევითი ინსტიტუტი, ციურიხი, შვეიცარია;
- ნარკომანიის და ფსიქიკური ჯანმრთელობის ცენტრი, ტორონტო, კანადა;
- წამალდამოკიდებულების პრობლემების ცენტრი, ვერმონტი, შეერთებული შტატები;
- ნარკომანიის და ალკოჰოლიზმის მკურნალობის საბჭო, ადელაიდა, ავსტრალია;
- ჯანმრთელობის მეცნიერების კვლევითი ინსტიტუტი, ბანგკოკი, ტაილანდი;
- ფსიქიკური ჯანმრთელობის ინსტიტუტი, ჰუნანი, ჩინეთი;
- ნარკოტიკების კვლევის ეროვნული ინსტიტუტი, პერტი, ავსტრალია.
სხვა ორგანიზაციები:
- ოპიოიდური დამოკიდებულების ამერიკის ასოციაცია;
- ამერიკის ნეიროფსიქოფარმაკოლოგიის კოლეჯი;
- ამერიკის ნარკოლოგიის საზოგადოება;
- საერთაშორისო ზიანის შემცირების ასოციაცია.
- დამოკიდებულების მკურნალობის პროგრესის საერთაშორისო ცენტრი (ICAAT).
- მეთადონის მომხრეთა ეროვნული ალიანსი, ნიუ იორკი, შეერთებული შტატები.
- წამალდამოკიდებულების ეროვნული ინსტიტუტი, შეერთებული შტატები.
-ჯანმრთელობის და კლინიკური სრულყოფის ეროვნული ინსტიტუტი, გაერთიანებული სამეფო.
- „ხარისხის ძიებაში“, ნიდერლანდები.
- ნივთიერებათა მავნედ მოხმარების საწინააღმდეგო სამსახური, ფსიქიატრიის დეპარტამენტი, ჟენევა.
- სამხრეთ აფრიკის ალკოჰოლსა და ნარკოტიკებზე დამოკიდებულების ეროვნული საბჭო.
- Turning Point-ის ალკოჰოლიზმის და ნარკომანიის ცენტრი, მელბურნი, ავსტრალია.
- ფსიქიატრიის მსოფლიო ასოციაცია.
- სამხრეთ აფრიკის ალკოჰოლიზმის და წამალდამოკიდებულების ეროვნული საბჭო.
 |
3 აბრევიატურები და აკრონიმები |
▲back to top |
6-MAM - 6-მონოაცეტილმორფინი
შიდსი - შეძენილი იმუნოდეფიციტის სინდრომი
ALT - ალანინ-ამინოტრანსფერაზა
AST - ასპარტატ-ამინოტრანსფერაზა
არტ - ანტირეტროვირუსული მკურნალობა
ც-ამფ - ციკლური ადენოზინ-მონოფოსფატი
CBT - კოგნიტური ქცევითი თერაპია
CD4 - დიფერენციაციის კლასტერი 4 (T უჯრედის მარკერი)
CI - საიმედოობის ინტერვალი
CM - გაუთვალისწინებელი სიტუაციების მართვა
CND - ნარკოტიკული პრეპარატების კომისია
COWS - ოპიოიდური აღკვეთის სინდრომის კლინიკური სკალა
CPS - პროსპექტული კონტროლირებული კვლევა
ECOSOC - გაეროს ეკონომიკური და სოციალური საბჭო
გაემ - გამა-ამინოერბოს მჟავა
GCMS - აირ-ქრომატოგრაფია და მას-სპექტრომეტრია
GDP - მთლიანი შიგა პროდუქტი
HCV - C ჰეპატიტის ვირუსი
აივ - ადამიანის იმუნოდეფიციტის ვირუსი
ICD-10 - დაავადებების საერთაშორისო კლასიფიკაცია, მე-10 გადასინჯვა
INCB - ნარკოტიკების კონტროლის საერთაშორისო საბჭო
ITT - მკურნალობის განზრახვა
IV - ინტრავენური
LAAM - ლევო-ალფა-აცეტილმეტადოლი
NAS - ნეონატალური აბსტინენციის სინდრომი
NSAIDs - ანთების საწინააღმდეგო არასტეროიდული პრეპარატები
OOWS - ოპიოიდური აღკვეთის სინდრომის ობიექტური სკალა
RCT - რანდომიზებული კონტროლირებული კვლევა
RR - შეფარდებითი რისკი
SMD - სტანდარტული საშუალო განსხვავება
SOWS - ოპიოიდური აღკვეთის სინდრომის სუბიექტური სკალა
TB - ტუბერკულოზი
UNAIDS - გაეროს აივ/შიდსის ერთობლივი პროგრამა
UNODC - გაეროს ნარკოტიკების და დანაშაულის ოფისი
UROD - ულტრასწრაფი ოპიოიდური დეტოქსიკაცია
ჯანმო - ჯანმრთელობის მსოფლიო ორგანიზაცია
გაერო - გაერთიანებული ერების ორგანიზაცია
 |
4 რეზიუმე |
▲back to top |
 |
4.1 სახელმძღვანელოს შემუშავების წინაპირობები |
▲back to top |
სახელმძღვანელო შეიქმნა გაეროს ეკონომიკური და სოციალური საბჭოს (ECOSOC) რეზოლუციის შედეგად, რომლის თანახმადაც ჯანდაცვის მსოფლიო ორგანიზაციას (ჯანმო), გაეროს ნარკოტიკების და დანაშაულის ოფისთან (UNODC) ერთად, შესთავაზეს „ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის მინიმალური მოთხოვნების შემუშავება და გამოქვეყნება“[1]. ჯანმოს პოლიტიკის თანახმად, ამ სახელმძღვანელოში მოცემული რეკომენდაციები ემყარება არსებული ლიტერატურის სისტემატურ მიმოხილვას და კონსულტაციებს მსოფლიოს სხვადასხვა რეგიონში მოღვაწე ექსპერტებთან. ამ დოკუმენტის №1 დანართში წარმოდგენილია მონაცემთა ცხრილები, სადაც შეჯამებულია ეს მიმოხილვითი სამუშაო.
ვისთვისაა განკუთვნილი სახელმძღვანელო?
სახელმძღვანელო განკუთვნილია ფსიქოსოციალური და ფარმაკოლოგიური მკურნალობის ნებისმიერ დონეზე მომუშავე სპეციალისტებისთვის. კერძოდ, განიხილება სამი დიდი ჯგუფი:
პოლიტიკური კურსის განმსაზღვრელი ოფიციალური და ხელმძღვანელი პირები, რომლებიც იღებენ გადაწყვეტილებებს მედიკამენტების ხელმისაწვდომობის შესახებ, ქვეყანაში და მის ადმინისტრაციულ რეგიონებში მომსახურების სტრუქტურისა და დაფინანსების შესახებ;
მენეჯერები და კლინიკის ხელმძღვანელები, რომლებიც პასუხისმგებელნი არიან სპეციფიკური სამედიცინო მომსახურების ორგანიზებაზე და მის ხარისხზე;
ჯანდაცვის მუშაკები, რომლებიც მკურნალობენ პაციენტებს სამედიცინო დაწესებულებებში.
ოპიოიდური დამოკიდებულების ეპიდემიოლოგია
UNODC-ის შეფასებით მსოფლიოში ნარკოტიკების მომხმარებელთა რიცხვი 25 მილიონამდეა, მათ შორის 15.6 მილიონი ოპიოიდების პრობლემური მომხმარებელია, 11.1 კი - ჰეროინის (მსოფლიოს მოსახლეობის დაახლოებით, 0.3%-ი)[2].1 აივ-ის და შეძენილი იმუნოდეფიციტის სინდრომის (შიდსი) გლობალური ეპიდემიის არსებობასა და გაძლიერებაში მნიშვნელოვანი როლი აქვს უსაფრთხოების წესების დაუცველად ჩატარებულ ინექციებს. სუბსაჰარული აფრიკის გარდა, სწორედ ეს არის მსოფლიოში აივ-ის ახალი შემთხვევების 30%-ის მიზეზი [5]. ამ ეპიდემიის შედეგი არის მილიონობით დაკარგული სიცოცხლე ყოველწლიურად და მილიარდობით დახარჯული დოლარი[6]. აივ ინფექციის პრევენციის ღონისძიებები, ოპიოიდური დამოკიდებულების მკურნალობასთან ერთად, აუცილებლად უნდა მოიცავდეს ოპიოიდების შეყვანისას უსაფრთხოების წესების დაცვის გაძლიერებულ მოთხოვნას [7,11].
სხვა ქრონიკული დაავადებების მსგავსად, ოპიოიდური დამოკიდებულებისთვის დამახასიათებელია რემისიებითა და რეციდივებით მიმდინარეობა.
ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა
ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა გულისხმობს სპეციფიკური ფარმაკოლოგიური და ფსიქოსოციალური ღონისძიებების ერთობლიობას, მიმართულს როგორც ოპიოიდების უკანონო მოხმარების, ისე მათ გამოყენებასთან დაკავშირებული ზიანის შემცირებისკენ და მომხმარებელთა ცხოვრების ხარისხის გაუმჯობესებისკენ. ოპიოიდური დამოკიდებულების დასაძლევი ფსიქოსოციალური ღონისძიებების სპექტრი მრავალფეროვანია, სამკურნალოდ კი მხოლოდ რამდენიმე სპეციფიკური პრეპარატია მოწოდებული.
ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობა გულისხმობს კვალიფიცირებული პროფესიონალის მიერ აღიარებული სამედიცინო პრაქტიკის პირობებში სრულყოფილად შესწავლილი ოპიოიდური აგონისტის დანიშვნას ამგვარი დამოკიდებულების მქონე ადამიანებისთვის მკურნალობის განსაზღვრული მიზნების მისაღწევად [8,9,10]. როგორც მეთადონი, ისე ბუპრენორფინი საკმაოდ გახანგრძლივებული მოქმედების პრეპარატებია, რაც საშუალებას იძლევა, მათი მიღება მოხდეს დღეში ერთხელ, საჭიროებისას - ზედამხედველობით. მათ ყოველდღიურ მიღებას არ მოჰყვება ინტოქსიკაციის და აღკვეთის მდგომარეობის ციკლები, რაც ჩვეულებრივია ხანმოკლე მოქმედების ოპიოიდების, მაგ., ჰეროინის მოხმარებისას. მეთადონის და ბუპრენორფინის გამოყენება კლებითი დოზებითაც შეიძლება ოპიოიდების მოხსნის დროს - პროცესი, რომელსაც ასევე ოპიოიდური დეტოქსიკაცია ეწოდება. მეთადონით და ბუპრენორფინით მკურნალობისათვის მყარი მტკიცებითი საფუძველი არსებობს. ეს პრეპარატები შესულია ჯანმოს ძირითადი მედიკამენტების სიაში [8].
მეორე მიდგომა არის ოპიოიდური დამოკიდებულების მქონე ადამიანების დახმარება ოპიოიდებისგან სრულ გათავისუფლებაში. ამ პროცესს ოპიოიდურ დეტოქსიკაციას უწოდებენ. მეთადონის და ბუპრენორფინის კლებითი დოზებით გამოყენება ამ მიზნითაც შეიძლება ოპიოიდური აღკვეთის სინდრომის სამკურნალოდ.
ალფა-2 ადრენერგული აგონისტები, როგორიცაა კლონიდინი, ასევე შეიძლება გამოყენებულ იქნეს ოპიოიდური დეტოქსიკაციის დროს ოპიოიდური აღკვეთის სიმპტომების სიმძიმის შესამცირებლად.
დეტოქსიკაციის შემდეგ, ოპიოიდების მოხმარების რეციდივის პრევენციისთვის, შესაძლებელია გახანგრძლივებული მოქმედების ოპიოიდური ანტაგონისტის, ნალტრექსონის გამოყენება. ნალტრექსონი თავისთავად არანაირ ოპიოიდურ ეფექტს არ იწვევს და ბლოკავს ოპიოიდების ეფექტს 24-48 საათის განმავლობაში.
ხანმოკლე მოქმედების ოპიოიდური ანტაგონისტი ნალოქსონი შეიძლება გამოვიყენოთ ოპიოიდური ინტოქსიკაციის ეფექტის მოსახსნელად და დოზის გადაჭარბების დროს.
სახელმძღვანელოში გამოყენებული მონაცემების და რეკომენდაციების შეჯამება
მხარდამჭერი ჩანაცვლებითი თერაპია
ოპიოიდური აგონისტებით
მკურნალობის შესწავლილი მეთოდებიდან ყველაზე ეფექტიანი ფსიქოსოციალურ დახმარებასთან კომბინირებული ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა აღმოჩნდა.
დასალევი მეთადონის ხსნარი და სუბლინგვალურად მისაღები ბუპრენორფინის აბები - ეს ის მედიკამენტებია, რომლებიც ყველაზე ფართოდ გამოიყენება აგონისტებით მხარდამჭერი თერაპიისთვის. მაღალი ხარისხის, ზედამხედველობის პირობებში ჩატარებული და კარგად ორგანიზებული მკურნალობით ეს პრეპარატები უზრუნველყოფს ინტოქსიკაციის და აღკვეთის ციკლის დარღვევას, მნიშვნელოვნად ამცირებს ჰეროინის და სხვა უკანონო ოპიოიდების მოხმარებას, დანაშაულს და დოზის გადაჭარბებით გამოწვეული სიკვდილის რისკს.
დეტოქსიკაციასთან და მკურნალობის გარეშე დატოვებასთან შედარებით, მეთადონით მხარდამჭერი თერაპიით (ძირითადად, თხევადი მეთადონის ზედამხედველობის პირობებში მიღება) საგრძნობლად მცირდება ოპიატების და სხვა პრეპარატების გამოყენება, კრიმინალური აქტივობა, აივ-ით ინფიცირების სარისკო ქცევა, მისი გავრცელება და ყველა ამ მიზეზით გამოწვეული სიკვდილიანობა; იგი ასევე ხელს უწყობს პაციენტების მკურნალობის პროცესში დაყოვნებას.
მეთადონის შედარება ბუპრენორფინთან ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის დროს
ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის დროს მეთადონის და ბუპრენორფინის ეფექტიანობის შემფასებელი კლინიკური კვლევების მონაცემების შედარებისას ორივე მედიკამენტმა ძირითადად კარგი შედეგი აჩვენა. საზოგადოდ, მეთადონს, როგორც უფრო ეფექტიანსა და იაფს ბუპრენორფინთან შედარებით, უპირატესობა ენიჭება, თუმცა, ბუპრენორფინს ოდნავ განსხვავებული ფარმაკოლოგიური მოქმედება აქვს; ამდენად, ორივე პრეპარატის ხელმისაწვდომობა უფრო მეტ ადამიანს მოიზიდავს მკურნალობაში ჩასართავად და ხელს შეუწყობს ეფექტიანი მკურნალობის შერჩევას.
მეთადონით მხარდამჭერი ჩანაცვლებითი თერაპია
მეთადონის საწყისი დოზა არ უნდა აღემატებოდეს 20 მგ-ს. ეს დამოკიდებულია ოპიოიდური ტოლერანტობის დონეზე, რაც იძლევა დოზის უსაფრთხო შერჩევის და ზედოზირების თავიდან აცილების საშუალებას. შემდეგ დოზა სწრაფად უნდა დარეგულირდეს ზრდით (თუ ოპიოიდური აბსტინენციის სიმპტომები რჩება) ან კლებით (თუ სედაცია აღინიშნება). ამ ეტაპის შემდეგ უნდა მოხდეს დოზის თანდათანობითი მატება არალეგალური ოპიოიდის მოხმარების შეწყვეტამდე. ეს, ჩვეულებრივ, მიიღწევა დღეში 60-120 მგ მეთადონის მიღებით. დასაწყისში აუცილებელია ზედამხედველობის დაწესება მეთადონის დოზის მიღებაზე. ზედამხედველობის დონე უნდა შეირჩეს ინდივიდუალურად ადგილობრივი რეგულაციების შესაბამისად. სასურველია ბალანსის დაცვა სტაბილურ პაციენტებში
დოზის სიხშირის შემცირებასთან დაკავშირებულ სარგებელსა და მეთადონის ინექციის გაკეთების რისკს ან მის ნარკოტიკების ბაზარზე მოხვედრის რისკს შორის. პაციენტებზე უნდა დაწესდეს მონიტორინგი - კლინიკური შეფასება და ნარკოტიკზე ტესტირება. ფსიქოსოციალური დახმარება ყველა პაციენტს უნდა შევთავაზოთ.
ბუპრენორფინით მხარდამჭერი თერაპია
ბუპრენორფინით მხარდამჭერი თერაპია უნდა დაიწყოს ტოლერანტობის დონის, ოპიოიდის გამოყენების ხანგრძლივობის და ყველაზე ბოლოს მოხმარებული ოპიოიდის დოზის გათვალისწინებით (ჩვეულებრივ 4 მგ). ამის შემდეგ დოზა სწრაფად (მაგ., რამდენიმე დღეში) უნდა გაიზადროს (8-24 მგ ბუპრენორფინი დღეში), სანამ არ მოგვცემს სტაბილურ ეფექტს 24 საათის განმავლობაში; თუ ოპიოიდის მოხმარება გრძელდება, დოზა ისევ უნდა გაიზარდოს. დოზის მიღებაზე ზედამხედველობა და მკურნალობის სხვა ასპექტები უნდა განისაზღვროს ინდივიდუალურად, იმავე კრიტერიუმების გათვალისწინებით, რომლებიც გამოიყენება მეთადონით ჩანაცვლებითი თერაპიის დროს.
აღკვეთის მდგომარეობის მკურნალობა და რეციდივის პრევენცია
ოპიოიდური პრეპარატის მოხსნა (მხარდამჭერი ჩანაცვლებითი მკურნალობისგან განსხვავებით) გრძელვადიან პერსპექტივაში არასახარბიელო გამოსავალთან არის დაკავშირებული; თუმცა, თუ ოპიოიდებისგან სრული გათავისუფლება პაციენტის ინფორმირებული არჩევანია, ჩვენ უნდა დავეხმაროთ მას ამის გაკეთებაში. ოპიოიდების მოხსნა შეიძლება მოხდეს ამბულატორიულად ან სტაციონარის პირობებში მეთადონის, ბუპრენორფინის ან ალფა-2 აგონისტების კლებადი დოზების მიღებით. მეთადონს და ბუპრენორფინს უპირატესობა ენიჭება ოპიოიდური მოხსნის სინდრომის მკურნალობისას, რადგან ეს პრეპარატები უფრო შედეგიანია და მათი გამოყენება შეიძლება ზედამხედველობით როგორც ამბულატორიულ, ისე სტაციონარის პირობებში. სტაციონარული მკურნალობა უფრო ეფექტიანია, მაგრამ, ამასთანავე, უფრო ძვირიც და რეკომენდებულია პაციენტთა მხოლოდ მცირე ნაწილისათვის (მაგ., რამდენიმე ნივთიერებაზე დამოკიდებულების, სომატური ან ფსიქიატრიული თანმხლები დაავადების დროს). უსაფრთხოების პრობლემების გამო რეკომენდებული არ არის აღკვეთის მდგომარეობის დაჩქარებული მეთოდი ოპიოიდური ანტაგონისტების მოხმარებით ღრმა სედაციასთან კომბინაციაში.
ნალტრექსონის გამოყენება რეციდივის თავიდან ასაცილებლად
ნალტრექსონი შეიძლება ეფექტიანი იყოს რეციდივის თავიდან ასაცილებლად პაციენტებისათვის, რომელთაც შეწყვიტეს ოპიოიდების მოხმარება და მოტივირებულები არიან, აღარ გამოიყენონ ოპიოიდები. ოპიოიდების მოხსნის შემდეგ ამგვარ პაციენტებს აუცილებლად უნდა ვურჩიოთ ნალტრექსონით სარგებლობა რეციდივის პრევენციისთვის.
ფსიქოსოციალური მკურნალობა
მკურნალობის შედეგიანობის გაზრდის მიზნით, აგონისტებით მხარდამჭერი თერაპიის და ოპიოიდების აღკვეთის მდგომარეობის მკურნალობისას შესაძლებელია გამოვიყენოთ ფსიქოსოციალური დახმარება - კოგნიტური და ქცევითი მეთოდები და გაუთვალისწინებელი სიტუაციების მართვის ტექნიკა. ფსიქოსოციალური დახმარება ხელმისაწვდომი უნდა იყოს ყველა პაციენტისთვის, თუმცა, მათ, ვინც არ მიიღებს ამ შეთავაზებას, უარი არ უნდა ვუთხრათ ეფექტიან ფარმაკოლოგიურ მკურნალობაზე.
მკურნალობის სისტემები
მკურნალობის სისტემების დაგეგმვის დროს რესურსები იმგვარად უნდა გადანაწილდეს, რომ ეფექტიანი მკურნალობა რაც შეიძლება მეტი ადამიანისთვის იყოს ხელმისაწვდომი. ოპიოიდური აგონისტებით მხარდამჭერი თერაპია ხარჯების მხრივ ყველაზე რენტაბელურ მკურნალობადაა მიჩნეული და, ამდენად, იგი ოპიოიდური დამოკიდებულების მკურნალობის სისტემის საფუძველი უნდა იყოს. ქვეყნებში, სადაც მიღე ბულია ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობის პროგრამები, მათში მონაწილეობა, ჩვეულებრივ, ოპიოიდური დამოკიდებულების მქონეთა 40-50%-ისთვისაა მიმზიდველი. ურბანულ დასახლებებში ეს პროცენტი კიდევ უფრო მაღალია. მაღალი ფასის გამო სტაციონარებში გათვალისწინებული უნდა იყოს სპეციფიკური შემთხვევები, პაციენტთა უმრავლესობას კი, რომელთაც სურთ ოპიოიდების მოხსნა, ამის ცდა ამბულატორიულ პირობებში უნდა შევთავაზოთ.
მკურნალობის ეთიკური პრინციპები
ოპიოიდური დამოკიდებულების მქონე ადამიანების მკურნალობისას კლინიკური კვლევებით მიღებულ მონაცემებთან ერთად აუცილებლად უნდა გავითვალისწინოთ ეთიკური პრინციპები. ყოველთვის უნდა ვცეთ პატივი ოპიოიდური დამოკიდებულების მქონე ინდივიდების უფლებებს. მკურნალობასთან დაკავშირებული გადაწყვეტილებები უნდა ემყარებოდეს სამედიცინო ეთიკის სტანდარტულ პრინციპებს - მკურნალობა და ფსიქოსოციალური დახმარება სწორედ იმ სახით უნდა იყოს ხელმისაწვდომი, რა სახითაც მოცემულ პაციენტს სჭირდება. მკურნალობის დროს გათვალისწინებული უნდა იყოს ინდივიდის თავისუფლება; პაციენტს სრული ინფორმაცია უნდა მიეწოდოს მკურნალობის სხვადასხვა რისკების და სარგებლის შესახებ. მეტიც, პროგრამებმა უნდა შექმნას ხელშემწყობი გარემო და ურთიერთობები მკურნალობის გასაადვილებლად, უზრუნველყოს თანმხლები ფსიქიკური და სომატური დაავადებების კოორდინირებული მკურნალობა და ყურადღება დაუთმოს შესაბამის ფსიქოსოციალურ ფაქტორებს.
რეკომენდაციები
ამ ნაწილში მოცემულია სახელმძღვანელოში შეტანილი ყველა რეკომენდაცია:
რეკომენდაციები პოლიტიკის ან ჯანმრთელობის სისტემებისთვის აღნიშნულია როგორც „მინიმალური“ ან „საუკეთესო პრაქტიკა“.
მინიმალური რეკომენდაციები მოწოდებულია მინიმალური სტანდარტის სახით; ეს უნდა იყოს მინიმალური მოთხოვნა ოპიოიდური დამოკიდებულების მკურნალობის უზრუნველსაყოფად.
საუკეთესო პრაქტიკის რეკომენდაციები ოპიოიდური დამოკიდებულების მკურნალობის უპირატესი სტრატეგიებია საზოგადოების ჯანმრთელობისთვის ოპტიმალური სარგებლის მოსატანად.
ეს დოკუმენტი მოიცავს სისტემატურ მიმოხილვებზე და მეტაანალიზებიდან მიღებულ მონაცემებზე დამყარებულ რეკომენდაციებს სხვა წყაროების, ტექნიკური მოსაზრებების, რესურსების და სხვადასხვა ალტერნატივების რისკის და სარგებლის გათვალისწინებით. GRADE სისტემის მიხედვით, რეკომენდაციები სიძლიერის თვალსაზრისით ორ ჯგუფად არის გაყოფილი - „მყარი“ (მაღალი სანდოობის) ან „სტანდარტული“ რეკომენდაციები.
მყარი (მაღალი სანდოობის) რეკომენდაციები, რომლებიც:
- უმრავლესობამ უნდა მიიღოს იმ პირობით, რომ მათ გასაგები სახით მიეწოდოთ ინფორმაცია დაკავშირებული სარგებლის, ზიანის და ტვირთის შესახებ.
- უმრავლესობისთვის მისაღებია და მხოლოდ მცირე ნაწილმა შეიძლება არ მიიღოს.
- რეკომენდაცია შეიძლება დაუბრკოლებლად იქნეს გამოყენებული პოლიტიკის განმსაზღვრელებისთვის.
სტანდარტულია რეკომენდაციები, რომლებიც:
- დიდი ნაწილისთვის მისაღებია, მაგრამ საკმაოდ ბევრისთვის შეიძლება მიუღებელი იყოს.
- შეიძლება მნიშვნელოვად განსხვავდებოდეს ღირებულებების და უპირატესობების მიხედვით.
პოლიტიკის განსაზღვრას ფართო დებატები და ბევრი მონაწილის ჩართვა სჭირდება.
ზოგიერთი რეკომენდაციის სიძლიერე განსაზღვრული არ არის - ეს ნიშნავს, რომ რეკომენდაცია არ არის შეფასებული.
რეკომენდაციების შემაჯამებელი ცხრილი
რეკომენდაციები ჯანმრთელობის სისტემებისთვის ქვეყანაში და ქვეყნის რეგიონების დონეზე |
||
|
მინიმალური მოთხოვნები |
საუკეთესო პრაქტიკა |
მკურნალობის |
|
უნდა შეიქმნას სტრატეგიული |
საკანონმდებლო |
ფსიქოსოციალურ |
|
მკურნალობის |
მკურნალობა
ოპიოიდური
თანმხლები დაავადებების
მკურნალობის პროგრამის
ფარმაკოლოგიური მკურნალობის |
ოპტიმალური დაფარვის და
ოპიოიდური დამოკიდებულების
ფარმაკოლოგიური მკურნალობის ასარჩევი
ალფა-2 ადრენერგულ |
რეკომენდაციები მკურნალობის პროგრამებისთვის |
||
|
მინიმალური მოთხოვნები |
საუკეთესო პრაქტიკა |
კლინიკური მართვა |
ოპიოიდური დამოკიდებულების |
კლინიკური მართვის პროცესი
ოპიოიდური დამოკიდებულების |
თანხმობა მკურნალობაზე |
პაციენტებისგან მიღებული უნდა |
|
პერსონალის სწავლება |
ოპიოიდური დამოკიდებულების |
ჯანდაცვის სისტემის ხელმძღვანელმა |
სამედიცინო ჩანაწერები |
ყველა პაციენტზე უნდა წარმოებდეს
უზრუნველყოფილი უნდა
პაციენტის მკურნალობაში ჩართული
ჯანდაცვის მუშაკებმა ან
ოპიოიდური აგონისტებით |
|
აფთიაქის ჩანაწერები |
საჭიროა პროცესების დასაბუთება, |
|
კლინიკური ინსტრუქციები |
ოპიოიდური დამოკიდებულების |
კლინიკური ინსტრუქციები უნდა იყოს |
დოზირების პოლიტიკა |
აგონისტებით მხარდამჭერი |
|
დეტოქსიკაციის სერვისი |
|
ოპიოიდების მოხსნის მართვის სერვისის
სტრუქტურა არ უნდა იყოს ცალკე მკურნალობის სხვა სისტემებთან. |
სახლში მისაღები დოზები |
|
სახლში მისაღები დოზები |
მკურნალობის კურსიდან |
|
მკურნალობის კურსიდან |
მკურნალობის |
უნდა ჩატარდეს დეტალური
სოციალური და
კლინიკურ გამოკვლევას
როცა სხვა საშუალებით (მაგ., |
პაციენტის არჩევანი უნდა ეფუძნებოდეს
ფსიქიატრიული და სომატური თანმხლები
ნებაყოფლობითი ტესტირება
ოპიოიდების მოხსნა უნდა |
მომსახურების |
ფარმაკოლოგიური მკურნალობის არჩევანი უნდა
ნალოქსონი ხელმისაწვდომი უნდა |
ფარმაკოლოგიური მკურნალობის არჩევანი |
ფსიქოსოციალური |
ფსიქოსოციალური დახმარება უნდა |
ფსიქოსოციალური დახმარების სხვადასხვა
ამგვარი ჩარევების არასრული სია
მაგ.: ბინა, დასაქმება,
ფსიქიატრიული თანმხლები დაავადებების |
თანმხლები |
უზრუნველყოფილი უნდა |
სადაც ოპიოიდებზე
ტუბერკულოზის, ჰეპატიტის,
ანტიტუბერკულოზური,
ტუბერკულოზით, ჰეპატიტით ან აივ-ით
პაციენტებს თანაბარი მისაწვდომობა |
B ჰეპატიტის ვაქცინის |
|
მკურნალობის პროცესში ოპიოიდებზე |
მკურნალობის შეფასება |
საჭიროა არსებობდეს |
საჭიროა, არსებობდეს ჩატარებული |
რეკომენდაციები ინდივიდუალური პაციენტის მკურნალობისთვის |
|||
|
მინიმალური მოთხოვნები |
რეკომენდაციის |
მტკიცების |
მკურნალობის |
ოპიოიდური დამოკიდებულების ფარმაკოლოგიური |
ძლიერი |
დაბალი-საშუალო |
|
ოპიოიდური დამოკიდებულების მქონე იმ |
სტანდარტული |
დაბალი |
ჩანაცვლებითი მკურნალობა |
ოპიოიდური აგონისტებით |
ძლიერი |
მაღალი |
|
მეთადონით მკურნალობის |
ძლიერი |
ძალიან დაბალი |
|
საშუალოდ, მეთადონით |
ძლიერი |
დაბალი |
|
ბუპრენორფინის ჩანაცვლებითი თერაპიის |
სტანდარტული |
ძალიან დაბალი |
|
მკურნალობის საწყის ეტაპზე |
ძლიერი |
ძალიან დაბალი |
|
სახლში მისაღები დოზა უნდა |
სტანდარტული |
ძალიან დაბალი |
|
ოპიოიდური დამოკიდებულების |
ძლიერი |
მაღალი |
ოპიატების მოხსნის მართვა |
ოპიოიდების მოხსნის |
სტანდარტული |
საშუალო |
|
ოპიოიდების აღკვეთის |
სტანდარტული |
ძალიან დაბალი |
|
ოპიოიდების მოხსნის |
ძლიერი |
დაბალი |
 |
5 1 მიზანი და დანიშნულება |
▲back to top |
ეს სახელმძღვანელო შემუშავებულია გაეროს ეკონომიკური და სოციალური საბჭოს (ECOSOC) რეზოლუციის მიხედვით: ოპიოიდებზე დამოკიდებული პირების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის მეთოდები. ამ რეზოლუციის თანახმად, ჯანდაცვის მსოფლიო ორგანიზაციას (ჯანმო), გაეროს ნარკოტიკების და დანაშაულის ოფისთან (UNODC) ერთად, წევრი ქვეყნებისთვის დახმარების გაწევის მიზნით შესთავაზეს „ოპიოიდებზე დამოკიდებულ პირთა ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის მინიმალური მოთხოვნების, საერთაშორისო მეთოდების შემუშავება და გამოქვეყნება დარგის რეგიონული განვითარების გათვალისწინებით“, [1].
ეს მეთოდები განკუთვნილია ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის ნებისმიერ დონეზე მომუშავე სპეციალისტებისთვის. მე-2 თავში განმარტებულია ამ ინსტრუქციების ფორმულირების დეტალები, მე-3 თავში წარმოდგენილია ინფორმაცია ოპიოიდური დამოკიდებულების შესახებ, მე-4-6 თავები კი, შესაბამისად, ეძღვნება იმ სამ დიდ ჯგუფს, რომელთათვისაც განკუთვნილია ეს დოკუმენტი:
პოლიტიკური კურსის განმსაზღვრელი ოფიციალური და ხელმძღვანელი პირები, რომლებიც იღებენ გადაწყვეტილებებს მედიკამენტების ხელმისაწვდომობის შესახებ, ქვეყანაში და მის ადმინისტრაციულ რეგიონებში მომსახურების სტრუქტურისა და დაფინანსების შესახებ.
მენეჯერები და კლინიკის ხელმძღვანელები, რომლებიც პასუხისმგებელნი არიან სპეციფიკური სამედიცინო მომსახურების ორგანიზებასა და მის ხარისხზე.
ჯანდაცვის მუშაკები, რომლებიც მკურნალობენ პაციენტებს სამედიცინო დაწესებულებებში.
ცენტრალურ და რეგიონულ პროგრამებს და მკურნალობის მეთოდებზე მომუშავე ჯგუფებს შეიძლება სურდეთ ამ დოკუმენტით სარგებლობა ადგილობრივი ადაპტირებული სახელმძღვანელოს შესაქმნელად.
ამ სახელმძღვანელოში განხილული კლინიკური საკითხები შემუშავდა ოპიოიდური დამოკიდებულების მართვის სფეროში მომუშავე სხვადასხვა ქვეყნის კლინიცისტებთან და აკადემიურ პერსონალთან კონსულტაციების საფუძველზე. სახელმძღვანელოში მოცემული საკითხები მოკლედ შეიძლება შემდეგი სახით ჩამოვაყალიბოთ:
რომელი პრეპარატებით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების და აღკვეთის მდგომარეობის მკურნალობისთვის? ამ საკითხთან დაკავშირებული დამატებითი კითხვებია:
* რომელს უნდა მიეცეს უპირატესობა: ოპიოიდური აგონისტებით მხარდამჭერ თერაპიას, დეტოქსიკაციას თუ ანტაგონისტებით მკურნალობას?
* რომელი მედიკამენტი უნდა მოვიხმაროთ თითოეული მეთოდის დროს?
* როგორ უნდა მოხდეს მედიკამენტის მიცემა? (ოპტიმალური დოზა, დოზის ზედამხედველობის დონე და სხვ.)?
რა დონის და ტიპის ფსიქოსოციალური დახმარება უნდა გაეწიოს ოპიოიდებზე დამოკიდებულ პაციენტებს?
რა განსაკუთრებული მკურნალობა უნდა შევთავაზოთ სპეციფიკურ ჯგუფებს (მაგ., ადამიანის იმუნოდეფიციტის ვირუსით (აივ) ინფიცირებულები და ორსულები)?
რა მინიმალური სტანდარტები არსებობს ოპიოიდური დამოკიდებულების მკურნალობისთვის?
სახელმძღვანელოში მოცემული რეკომენდაციები სამ დონეზე მუშაობს:
მკურნალობის სისტემები ქვეყნის და რეგიონულ დონეზე (პოლიტიკა, კანონმდებლობა, დაფინანსება, დაგეგმვა რეგიონული და ქვეყნის მასშტაბით, იხ. თავი 4);
მკურნალობის პროგრამები (მკურნალობის ორგანიზების და უზრუნველყოფის მეთოდები, იხ. თავი 5);
პაციენტის ინდივიდუალური მკურნალობა (იხ. თავი 6).
ინდივიდუალური რეკომენდაციები პაციენტისათვის ემყარება 1-ლ დანართში მოცემულ კლინიკური კვლევების სისტემატურ მიმოხილვებს. ორ დანარჩენ დონეზე გაცემული რეკომენდაციები კი სხვა მონაცემებს, მათ შორის, ექსპერტების მიერ კლინიკური კვლევების შედეგების ექსტრაპოლირებას, ეპიდემიოლოგიურ კვლევებს და სამედიცინო ეთიკის პრინციპებს.
ამ სახელმძღვანელოში განხილული მედიკამენტებია: მეთადონი, ბუპრენორფინი, ნალტრექსონი და ადრენერგული ალფა-2 აგონისტები (კლონიდინი, ლოფექსიდინი და გუანფასინი). მართალია, ოპიოიდური დამოკიდებულების სამკურნალოდ სხვა იმედისმომცემი მედიკამენტებიც არსებობს, მაგრამ ისინი არ არის შეტანილი ამ სახელმძღვანელოში, რადგან მათი ეფექტიანობის სრული ანალიზისთვის არ მოიპოვება საკმარისი მონაცემები. ამდენად, მათი ჩართვა მნიშვნელოვნად გაართულებდა სახელმძღვანელოს. მე-4 დანართში მოცემულია ამ მედიკამენტების მოკლე ფარმაკოლოგიური დახასიათება.
ამ სახელმძღვანელოს მიზანია:
ოპიოიდური დამოკიდებულების ეფექტიანი მკურნალობის გლობალური ბარიერების შემცირება;
ოპიოიდური დამოკიდებულების მტკიცებულებებზე დამყარებული და ეთიკური მკურნალობის პოლიტიკის განვითარების ხელშეწყობა;
ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობის ხარისხის გაუმჯობესება;
მკურნალობის ეფექტიანი პოლიტიკის და ოპიოიდური დამოკიდებულების პროგრამების განხორციელების გაადვილება.
ეს სახელმძღვანელო არ არის:
ოპიოიდური დამოკიდებულების და მისი მკურ ნალობის შესახებ კლინიკური მსჯელობის შემცვლელი უნივერსალური საშუალება;
ოპიოიდური დამოკიდებულების მკურნალობის უზრუნველმყოფი ადგილობრივი რეგულაციების აღწერა.
სახელმძღვანელო მოიცავს ინფორმაციას არა მხოლოდ ოპიოიდური დამოკიდებულების, არამედ ოპიოიდური ზედოზირების და ოპიოიდური აღკვეთის მდგომარეობის მკურნალობის შესახებ.
 |
6 2 რეკომენდაციების ფორმულირების მეთოდი |
▲back to top |
ჯანმოს სახელმძღვანელო „ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა“ მომზადებულია „ჯანმოს სახელმძღვანელო ჯანმოს სახელმძღვანელოსათვის“ (2003) მიხედვით [12] და მოდიფიცირებულია იმგვარად, რომ მაღალი სტანდარტების მტკიცებულებების არარსებობის დროსაც კი მოგვაწოდოს რჩევები მრავალ კომპლექსურ კლინიკურ საკითხზე, რომელთა შესახებ არასაკმარისი მტკიცებულებები არსებობს.
ტექნიკური ექსპერტების ჯგუფი, - მეცნიერები სხვადასხვა ქვეყნიდან, რომელთაც გამოცდილება აქვთ ოპიოიდური დამოკიდებულების და კლინიკური სახელმძღვანელოების შემუშავების სფეროში, - მოწვეულ იქნა 2005 წელს, მოგვიანებით კი - 2006 და 2007 წლებში. დეტალური ინფორმაცია ამ ჯგუფის წევრების შესახებ მოცემულია შესავალ ნაწილში. პირველი შეხვედრის დროს ჯგუფმა განსაზღვრა სახელმძღვანელოში შესატანი მთავარი საკითხები. თითოეული კლინიკური საკითხისთვის სისტემატური მიმოხილვის სახით მოძიებულ იქნა შესაბამისი ლიტერატურა. თუ საკითხთან დაკავშირებით არსებობდა კოქრეინის რევიუ1, მას უპირატესობა მიენიჭა სხვა მიმოხილვებთან შედარებით, ხოლო თუ არ არსებობდა შესაბამისი სისტემატური მიმოხილვა, ის ჯგუფის წევრებმა ჩაატარეს.
2006 წელს ჩატარებული შეხვედრის დროს ჯგუფმა შეაფასა მტკიცებულებები და შეიმუშავა რეკომენდაციები. მტკიცებულების ხარისხი შეფასდა GRADE-ის სამუშაო ჯგუფის[13] მიერ აღწერილი მეთოდის მიხედვით. ეს მეთოდი მოიცავს მოცემულ საკითხთან დაკავშირებული მტკიცებულების ხარისხის შეფასებას - მხედველობაში მიიღება ეფექტის სიდიდე, მონაცემების შესაბამისობა დასმულ კლინიკურ საკითხთან, ნიმუშის მნიშვნელობა შესაბამის კვლევებში, ძიებაში გამოყენებული მეთოდოლოგია და მონაცემების რეპროდუცირებადობა. ამ პროცესის დასაწყისში ჯანმრთელობის თითოეული გამოსავალი შეფასდა 1-დან 9 ქულამდე მისი მნიშვნელობის მიხედვით. GRADE-ის მიხედვით გამოსავლების რეიტინგი ფასდება შემდეგნაირად:
რეიტინგები 7-9 განკუთვნილია ჯანმრთელობის კრიტიკული გამოსავლებისთვის;
რეიტინგები 4-6 განკუთვნილია მნიშვნელოვანი, მაგრამ გადაწყვეტილების მიღებისთვის არა კრიტიკული გამოსავლებისთვის; მათი გამოყენება საჭიროა სარგებელსა და ზიანს შორის ბალანსის დასადგენად და რეკომენდაციებისათვის, მაგრამ არა მტკიცებულებათა საერთო ხარისხის შესახებ მსჯელობის დროს კრიტიკულ გამოსავლებთან მიმართებით.
რეიტინგები 1-3 ჩვეულებრივ, ამოღებულია მტკიცებულებათა დახასიათებიდან და არ განიხილება მტკიცებულების ხარისხის, სარგებელსა და ზიანს შორის ბალანსის დასადგენად ან რეკომენდაციების შესახებ მსჯელობის დროს.
ზოგიერთ შემთხვევაში სისტემატური მიმოხილვის მონაცემების გამოყენებით ჩატარდა დამატებითი მეტაანალიზი შემდეგი მიზნით:
არარანდომიზებული კონტროლირებადი კვლევების გამორიცხვა (სადაც კოქრეინის მიმოხილვებში შეტანილი იყო არარანდომიზებული კვლევები);
ზოგიერთი გამოსავლის შესწორება და ამით მისი მუდმივობის შენარჩუნება (მაგ., პირველადი გამოსავლის საზომად „გამოვარდნით“ სარგებლობა „კვლავმკურნალობის“ საზომის ნაცვლად).
შედარებების თანმიმდევრობის შებრუნება საჭიროების მიხედვით (მაგ., მეთადონი ბუპრენორფინთან შედარებით და არა პირიქით).
დამატებითი გამოსავლის შესწავლა (მაგ., სე როკონვერსიის, როგორც გამოსავლის, დამატება ოპიოიდური აგონისტებით მკურნალობის და აივ ინფექციის მიმოხილვის დროს).
GRADE-ის სისტემაში მტკიცებულების მნიშვნელობა კლასიფიცირდება როგორც: „მაღალი“, „საშუალო“, „დაბალი“ ან „ძალიან დაბალი“, რომლებიც შემდეგნაირად განისაზღვრება:
მაღალი - ძალზე ნაკლებად არის მოსალოდნელი, რომ შემდგომი კვლევა შეცვლის ეფექტის შეფასების საიმედოობას.
საშუალო - შესაძლებელია, რომ შემდგომმა კვლევამ მნიშვნელოვანი გავლენა იქონიოს ეფექტის შეფასების საიმედოობაზე და შეცვალოს ეს შეფასება.
დაბალი - დიდი ალბათობით მოსალოდნელია, რომ შემდგომმა კვლევამ მნიშვნელოვანი გავლენა მოახდინოს ეფექტის შეფასების საიმედოობაზე და შეცვალოს ეს შეფასება.
ძალიან დაბალი - ეფექტის ნებისმიერი შეფასება ძალზე არამყარია.
მიღებული მონაცემები ჩამოთვლილია 1-ლ დანართში.
რეკომენდაციების შესამუშავებლად ტექნიკურმა ექსპერტებმა გაითვალისწინეს ამ მიმოხილვებიდან და მეტაანალიზებიდან მიღებული მტკიცებულებები, სხვა წყაროებიდან მიღებული მონაცემები, ტექნიკური მოსაზრებები, გამოყენებული რესურსები, სხვადასხვა ალტერნატივის რისკები და სარგებელი.
თითოეული რეკომენდაციის ძალა დამყარებულია ჩარევის ეფექტიანობაზე, მტკიცებულების მნიშვნელობაზე, გამოყენებულ რესურსებზე, სარგებელსა და ზიანს შორის არსებულ ბალანსზე, ეთიკური საკითხების გათვალისწინებაზე.
როგორც GRADE-ის სისტემაშია მოცემული, რეკომენდაციები სიძლიერის მიხედვით ორ ჯგუფად იყოფა: „მყარი“ და „სტანდარტული“.
მყარი (მაღალი სანდოობის) რეკომენდაციები, რომლებიც:
- უმრავლესობამ უნდა მიიღოს იმ პირობით, რომ მათ გასაგები სახით მიეწოდოთ ინფორმაცია დაკავშირებული სარგებლის, ზიანის და ტვირთის შესახებ.
- უმრავლესობისთვის მისაღებია და მხოლოდ მცირე ნაწილმა შეიძლება არ გაიზიაროს.
- რეკომენდაცია შეიძლება დაუბრკოლებლად იქნეს გამოყენებული პოლიტიკის განმსაზღვრელებისთვის.
სტანდარტულია რეკომენდაციები, რომლებიც:
- დიდი ნაწილისთვის მისაღებია, მაგრამ საკმაოდ ბევრისთვის შეიძლება მიუღებელი იყოს.
- შეიძლება მნიშვნელოვად განსხვავდებოდეს ღირებულებების და უპირატესობების მიხედვით.
- პოლიტიკის განსაზღვრას ფართო დებატები და ბევრი მონაწილის ჩართვა სჭირდება.
ზოგიერთი რეკომენდაციის სიძლიერე განსაზღვრული არ არის - ეს ნიშნავს, რომ რეკომენდაცია არ არის შეფასებული.
სახელმძღვანელოს პროექტი 2007 წელს კომენტარებისთვის გაეგზავნა გარკვეულ ორგანიზაციებს, ჯანმოს განყოფილებებს, რეგიონულ ოფისებს და ჯანმოსთან მომუშავე ცენტრებს; აგრეთვე, ცაკლეულ ინდივიდებს საკუთარი თხოვნის საფუძველზე. პროექტი კომენტარებთან ერთად განხილული იქნა მესამე შეხვედრაზე, რომელიც 2007 წლის სექტემბერში შედგა.
ამ სფეროში მიმდინარე კვლევის სწრაფი ტემპების, მკურნალობის ალტერნატიული მეთოდების (რომელიც აქ არაა განხილული) სიმრავლის და ნაკლები რესურსების მქონე ქვეყნებში არსებული შედარებით მცირე გამოცდილების გათვალისწინებით, საჭიროა ამ სახელმძღვანელოს უახლოეს მომავალში განახლება. შესაბამისად, რეკომენდაციები ძალაში იქნება მხოლოდ უახლოესი სამი წლის განმავლობაში.
სახელმძღვანელოს განახლებაზე პასუხისმგებლობას იღებს ჯანმოს ფსიქიკური ჯანმრთელობის და ნარკომანიის დეპარტამენტი.
პოლიტიკა და პროგრამასთან დაკავშირებული რეკომენდაციები, არასისტემატიზებულ მიმოხილვებთან ერთად, ემყარება GRADE-ის პროცესით მიღებულ მტკიცებულებებს ტექნიკურ ექსპერტთა ჯგუფის წევრების აზრის გათვალისწინებით. შესაბამისად, ზოგიერთ ნაწილებს არ ახლავს რეკომენდაციების შესაბამისი GRADE-ის ცხრილები.
 |
6.1 2.1 კლინიკური კვლევის მონაცემების ანალიზი |
▲back to top |
ამ სახელმძღვანელოში შეჯამებულია კლინიკური კვლევების მონაცემები. როცა გამოსავლების შედარება ხდება კატეგორიული ცვლადების სახით (მაგ., სიკვდილიანობა, მკურნალობის პროცესში დაყოვნება (ჩართულობა) ან ოპიოიდებისგან თავშეკავება), გამოიყენება ფარდობითი რისკი. ფარდობითი რისკი არის გარკვეული გამოსავლის ალბათობა კონკრეტული ჩარევის ან რისკფაქტორის ზემოქმედების ქვეშ მყოფ პოპულაციაში იმავე გამოსავლის ალბათობასთან შედარებით აღნიშნული რისკფაქტორის ან გამოსავლის ზემოქმედების გარეშე. მაგ., თუ რანდომიზებულმა კონტროლირებულმა კვლევამ ჰეროინის მომხმარებელთა მეთადონზე მყოფი ჯგუფი შეადარა დეტოქსიკაციაზე მყოფ ჯგუფს და აღმოაჩინა, რომ მეთადონის ჯგუფის ჰეროინის მიღების ფარდობითი რისკი 0.32 იყო, ეს ნიშნავს, რომ, საშუალოდ, ოპიოიდური დამოკიდებულების მქონე ადამიანების მეთადონით მკურნალობისას ჰეროინის გამოყენების ალბათობა სამჯერ ნაკლებია დეტოქსიკაციის ჯგუფთან შედარებით.
მუდმივი ცვლადებისთვის (მაგ. ოპიოიდური აღკვეთის მდგომარეობის სიმძიმე ან კვლევის თითოეულ მონაწილეში შარდის ოპიოიდზე დადებითი ტესტების რაოდენობა) საშუალო სტანდარტული სხვაობა (SMD) ან საშუალო შეწონილი სხვაობა გამოიყენება მეტაანალიზის დროს. არაშედარებითი სკალებისთვის გამოყენებული საშუალო სტანდარტული სხვაობა არის განსხვავება ორ საშუალოს შორის გაყოფილი ჯგუფში არსებულ სტანდარტულ გადახრაზე. საშუალო შეწონილი სხვაობა გამოიყენება შედარებითი სკალებისთვის.
ფარდობითი რისკის ან საშუალო სხვაობის 95%-იანი საიმედოობის ინტერვალი გამოხატავს დიაპაზონს, რომელიც დიდი ალბათობით (ანუ 20-დან 19 შემთხვევაში) შეიცავს ნამდვილ ფარდობით რისკს ან საშუალო სხვაობას ხელმისაწვდომ მონაცემებზე დაყრდნობით. მაგ., თუ სიკვდილის ფარდობითი რისკის 95%-იანი საიმედოობის ინტერვალი მეთადონით მკურნალობაზე მყოფ შემთხვევით შერჩეულ პაციენტებში დეტოქსიკაციაზე მყოფ პაციენტებთან შედარებით არის 0.29-დან 0.48-მდე, ეს გულისხმობს, რომ შანსი იმისა, რომ ჭეშმარიტი ფარდობითი რისკი ამ დიაპაზონშია, არის 95%-ი.
 |
7 3 ზოგადი ინფორმაცია |
▲back to top |
 |
7.1 3.1 ოპიოიდური დამოკიდებულება |
▲back to top |
ოპიოიდურ დამოკიდებულებას ახასიათებს კოგნიტური, ქცევითი და ფსიქოსოციალური მახასიათებლების ერთობლიობა. დაავადებების საერთაშორისო კლასიფიკაცია, მე-10 გადასინჯვა (დსკ-10)[14] გამოყოფს ექვს ასეთ მახასიათებელს:
ოპიოიდების მიღების ძლიერი სურვილი ან კომპულსური ლტოლვა;
ოპიოიდების გამოყენების გაკონტროლების სირთულე;
ფიზიოლოგიური აღკვეთის მდგომარეობა;
ტოლერანტობა;
სხვა სიამოვნებების და ინტერესების პროგრესირებადი უგულვებელყოფა ოპიოიდების მოხმარების გამო;
ოპიოიდების მოხმარების გაგრძელება მათ მიერ გამოწვეული აშკარა მავნე ზემოქმედების მიუხედავად.
დსკ-10 ოპიოიდურ დამოკიდებულებას განსაზღვრავს შემდეგნაირად: „[ამ მახასიათებლებიდან] სამი ან მეტის ერთდროულად არსებობა წინა წლის განმავლობაში ერთ მოცემულ დროს“ (დეტალებისთვის იხ. დანართი 3).
ოპიოიდური დამოკიდებულება არ ვითარდება რეგულარული მოხმარების გარეშე, თუმცა მხოლოდ რეგულარული მოხმარება არ არის საკმარისი დამოკიდებულების განვითარებისათვის.
 |
7.2 3.2 ოპიოიდური დამოკიდებულების ნეირობიოლოგიური ასპექტები |
▲back to top |
ოპიოიდების რეგულარული მოხმარება იწვევს ნეიროადაპტაციულ რეაქციებს თავის ტვინის სხვადასხვა ნეირონულ წრეებში, რომლებიც ჩართულია მოტივაციის, მეხსიერების, ქცევის კონტროლის და დაძაბულობის მოხსნის პროცესებში. ამას შედეგად მოჰყვება მზარდი და ხანგრძლივი „წახალისების“, „დაჯილდოების“ ფენომენი, დაკავშირებული ოპიოიდების მოხმარებასთან; გარემოში ჩნდება ოპიოიდების მოხმარებასთან ასოცირებული მინიშნებები; ამავე დროს, აღინიშნება ყოველდღიურ ცხოვრებაში არსებული ბუნებრივი წამახალისებელი ფაქტორებით გამოწვეული „წახალისების“ დაქვეითება [15].
ბოლო ათწლეულის მანძილზე მნიშვნელოვნად გაიზარდა ჩვენი ცოდნა წამალდამოკიდებულების ნეირობიოლოგიური ასპექტების შესახებ [9]. ჩვენ უკვე ვიცით, რომ თავის ტვინის გარკვეულ სტრუქტურებს მნიშვნელოვანი როლი აქვს სიამოვნებასთან დაკავშირებული ქცევების რეგულირებაში. ამ სტრუქტურებისკენ მიმავალი და მათგან გამომავალი ნეირონული გზები ქმნის ე.წ. „წახალისების წრედებს“. ისინი მდებარეობს მეზოკორტიკოლიმბურ დოფამინურ სისტემებში, რომლებიც იწყება ვენტრალურ ტრიგემინურ არეებში და პროეცირდება nucleus accumbens-ზე, ნუშისებრ სხეულზე და პრეფრონტალურ ქერქზე[16].
1970-1980 წლებში გაჩნდა ინფორმაცია სხვადასხვა ოპიოიდური რეცეპტორების შესახებ, ხოლო შემდგომმა ფარმაკოლოგიურმა კვლევებმა გამოყო ოპიოიდური რეცეპტორების სამი კლასი, კერძოდ: მიუ, დელტა და კაპპა რეცეპტორები[17,18]. მას შემდეგ ჩვენი ცოდნა კიდევ უფრო გაღრმავდა და ახლა უკვე ცნობილია, რომ ოპიოიდური რეცეპტორები ეკუთვნის G-პროტეინთან დაკავშირებულ რეცეპტორებს და რომ რეცეპტორების თითოეული კლასი რამდენიმე ქვეტიპს მოიცავს [19].
ანალგეზიის, ეიფორიის და სედაციის ოპიოიდური ეფექტები უპირატესად მიუ რეცეპტორებით ხორციელდება. ოპიოიდები არაპირდაპირ ახდენს დოფამინის გამოთავისუფლების ინდუქციას გამაამინოერბოს მჟავას (გაემ) ინჰიბიციის შემცირებით ვენტრალურ ტრიგემინურ არეში არსებული მიუ რეცეპტორების საშუალებით [20, 21, 22]. ისინი ასევე ახდენს დოფამინის გამოთავისუფლების პირდაპირ ინდუქციას, nucleus accumbens-ში არსებულ ოპიოიდურ რეცეპტორებთან ურთიერთქმედების გზით [23, 24].
ადამიანის ოპიოიდურ რეცეპტორებზე ოპიოიდების ქრონიკული ზემოქმედების ეფექტი კარგად არ არის შესწავლილი. ტოლერანტობა ვითარდება მრავალი მექანიზმით, რომელთა შორისაა ოპიოიდური რეცეპტორის მწვავე დესენსიტიზაცია (რომელიც ოპიოიდის მოხმარებიდან რამდენიმე წუთში ვითარდება და იხსნება რამდენიმე საათში) და ოპიოიდური რეცეპტორის ხანგრძლივი დესენსიტიზაცია (რომელიც გრძელდება ოპიოიდური აგონისტის მოხსნიდან რამდენიმე დღის განმავლობაში). ასევე, ცვლილებები აღინიშნება ოპიოიდური რეცეპტორების რაოდენობაში [25] - კერძოდ, აღინიშნება ციკლური ადენოზინმონოფოსფატის (ცამფ) კომპენსატორული up-რეგულაცია. როცა ოპიოიდი იხსნება, ხდება ცამფ-ის კასკადის ჰიპერაქტივაცია. ეს იწვევს „ნორადრენერგულ შტორმს“, რაც კლინიკურად ოპიოიდური აღკვეთის მდგომარეობის სახით გამოვლინდება და რითაც იქმნება მოტივაცია ნარკოტიკის მიღების განახლებისთვის. ინტენსიური დისფორიული აღკვეთის მდგომარეობისთვის დამახასიათებელია ცრემლდენა, სურდო, მთქნარება, ოფლიანობა, მოუსვენრობა, გაღიზიანებადობა, ტრემორი, გულისრევა, ღებინება, არტერიული წნევის აწევა, შემცივნება, სპაზმები და კუნთების ტკივილი; ეს შეიძლება შვიდი დღის განმავლობაში ან კიდევ უფრო დიდხანს გაგრძელდეს.
ოპიოიდების რეგულარული მოხმარებისას ნეირონულ წრედებში აღინიშნება ხანგრძლივი ცვლილებები, რომლებიც დასწავლის და დამახსოვრების დროს განვითარებული ცვლილებების მსგავსია. ეს ეფექტი ქმნის ოპიოიდების მოხმარების რეციდივის მაღალ რისკს ხანგრძლივი თავშეკავების მდგომარეობის შემდეგაც კი [26].
 |
7.3 3.3 ოპიოიდების უკანონო მოხმარების და დამოკიდებულების ეპიდემიოლოგია |
▲back to top |
ოპიოიდური დამოკიდებულება მთელი მსოფლიოს პრობლემაა, რომელსაც უზარმაზარი ეკონომიკური, პიროვნული და საზოგადოებრივ ჯანდაცვასთან დაკავშირებული შედეგები აქვს. მსოფლიოში ოპიოიდების 15.6 მილიონი უკანონო მომხმარებელია, რომელთაგან 11 მილიონი ჰეროინს იყენებს [2]. ოპიოიდები ძირითადი ნარკოტიკებია აზიაში, ევროპაში და ოკეანიის დიდ ნაწილში. მიჩნეულია, რომ მსოფლიოში ოპიოიდების კლასის ნივთიერებების გამოყენება იზრდება [2].
 |
7.4 3.4 ოპიოიდების მოხმარებით გამოწვეული ზიანი |
▲back to top |
ნარკოტიკის ინექციური მოხმარება მჭიდროდ უკავშირდება აივ-ს - აივ ინფექციის შემთხვევების 30%-ი სუბსაჰარული აფრიკის გარეთ და 80%-მდე აღმოსავლეთ ევროპის და ცენტრალური აზიის ზოგიერთ ქვეყანაში ნარკოტიკების ინექციურ მომხმარებლებზე მოდის [5]. ნარკოტიკის მომხმარებელთა პოპულაციაში აივ-ის მოხვედრისას ინფექცია სწრაფად ვრცელდება. სუბსაჰარულ აფრიკაში ინტრავენური ნარკოტიკების მოხმარებით გამოწვეული ახალი ეპიდემია მძვინვარებს[2]. ამ სიტუაციის მიუხედავად, ინტრავენურ ნარკომანებში აივ ინფექციის პრევენციის ზომები, მათ შორის, ოპიოიდური აგონისტებით ჩანაცვლებითი თერაპია 5%-ზე ნაკლებ შემთხვევაში გამოიყენება [27].
დაუცველი ინექციის პრაქტიკამ, რომელიც ინტრავენურ ნარკოტიკებთან არის დაკავშირებული, C ჰეპატიტის გლობალური ეპიდემია გამოიწვია. C ჰეპატიტით, დაახლოებით, 130 მილიონი ადამიანია ინფიცირებული, მათ შორის, ყოველწლიურად 3-4 მილიონი ახალი შემთხვევა აღინიშნება [28]. ინექციების დაუცველი პრაქტიკა C ჰეპატიტის გადაცემის ძირითადი გზაა და ახალი შემთხვევების დაახლოებით 90%-ს იწვევს.
აივ ინფექციის დაბალი გავრცელების ქვეყნებში ოპიოიდებზე დამოკიდებული ინდივიდების სიკვდილიანობის მაჩვენებელი წელიწადში 2-4%-ია, ანუ მათი ასაკის სხვა ადამიანებზე 13-ჯერ მაღალი [29]. გაზრდილი სიკვდილიანობა ძირითადად დაკავშირებულია ზედოზირებასთან, თვითმკვლელობასთან, მოწევასა და ალკოჰოლთან დაკავშირებულ მიზეზებთან [30, 31, 32]. ქვეყნებში, სადაც აივ ინფექცია ფართოდაა გავრცელებული, შეძენილი იმუნოდეფიციტის სინდრომი (შიდსი) ასევე მნიშვნლოვან გავლენას ახდენს სიკვდილიანობაზე [33].
თავისთავად, ოპიოიდური დამოკიდებულება დაკავშირებულია სიცოცხლის ხარისხის მნიშვნელოვან დაქვეითებასთან, რადგან გონივრული საქმიანობა ჩანაცვლდება ინტოქსიკაციით ან ოპიოიდების ძებნაში დროის ხარჯვით [34]. ინტრავენურ ნარკომანიასთან დაკავშირებულ თანმხლებ დაავადებებთან და ძალადობასთან ერთად, უკანონო ოპიოიდების მომხმარებლებს ფსიქიატრიული დაავადებებიც ხშირად აღენიშნებათ - კერძოდ, დეპრესია და პოსტტრავმული სტრესული აშლილობა [35].
 |
7.5 3.5 ოპიოიდების მოხმარების ეკონომიკური შედეგები |
▲back to top |
ოპიოიდური დამოკიდებულება საზოგადოებას მნიშვნელოვან ეკონომიკურ ტვირთად აწევს არა მხოლოდ პირდაპირი ჯანდაცვის ხარჯების (მაგ. მკურნალობა, პრევენცია და სხვა სამედიცინო მომსახურება), არამედ ბიუჯეტზე სხვა გავლენის გამოც (განსაკუთრებით, სოციალური კეთილდღეობა და კრიმინალური სამსახურები). ოპიოიდურ დამოკიდებულებას ასევე გავლენა აქვს პროდუქტიულობაზე, რადგან იგი ასოცი რებულია უმუშევრობასთან, სამუშაოს გაცდენასთან და ნაადრევ სიკვდილთან.
ინდუსტრიულ ქვეყნებში ჩატარებული კვლევებით იყო მცდელობა ეკონომიკაზე ამ შედეგების გავლენის შეფასებისა, რის შედეგადაც გაირკვა, რომ დანაკარგი ქვეყნის მთლიანი შიგა პროდუქტის 0.2-დან 2%-მდეა [36, 37, 38].
 |
7.6 3.6 ოპიოიდური დამოკიდებულების ისტორია |
▲back to top |
აკრძალულ ოპიოიდებზე დამოკიდებული ადამიანების კოჰორტულმა გამოკვლევებმა უჩვენა, რომ მართალია, დაკვირვების დროს მათი მნიშვნელოვანი ნაწილი (10-40%-ი) არ მოიხმარდა ნარკოტიკს, შემდგომში უმრავლესობა აგრძელებდა აკრძალული ნარკოტიკების მოხმარებას [39, 40, 41, 42]. მკურნალობა ოპიოიდური დამოკიდებულებისგან გათავისუფლების ერთ-ერთი ფაქტორია; სხვა ფაქტორები მოიცავს პიროვნების მოტივაციას, რელიგიას, სულიერებას, ოჯახს და დასაქმებას [41].
 |
7.7 3.7 ოპიოიდური დამოკიდებულება როგორც დაავადება |
▲back to top |
ისტორიულად, ოპიოიდური დამოკიდებულება განიხილებოდა როგორც ნებისყოფის სისუსტე, რაც პიროვნებას უარყოფითად ახასიათებდა. თუმცა, დღესდღეობით, იმ ბიოლოგიური მექანიზმების შესწავლის საფუძველზე, რაც წამალდამოკიდებულების უკან დგას, უკვე მიჩნეულია, რომ ოპიოიდების მიღების მიზეზის მიუხედავად, ოპიოიდური დამოკიდებულების თანმხლები ნეირობიოლოგიური ცვლილებები თავის ტვინის დაავადებას წარმოადგენს. ამდენად, ოპიოიდური დამოკიდებულება შეიძლება განვიხილოთ როგორც ავადმყოფობა რთული სოციალური და ინდივიდუალური განმსაზღვრელი ფაქტორებით. ოპიოიდურ დამოკიდებულებას მრავალი სიმპტომი ახასიათებს, რომელთაც გრძელვადიან პერსპექტივაში პროგნოზული მნიშვნელობა აქვს და რომელთათვისაც დღეს მკურნალობის არჩევანი არსებობს [9].
 |
7.8 3.8 ოპიოიდური დამოკიდებულების მკურნალობა |
▲back to top |
ოპიოიდური დამოკიდებულების მკურნალობა ფარმაკოლოგიური და ფსიქოსოციალური ჩარევის კომპლექსია, რომლის მიზანია შემდეგი:
ოპიოიდების მოხმარების შემცირება ან შეწყვეტა;
მომავალში ოპიოიდების მოხმარებასთან დაკავშირებული ზიანის თავიდან აცილება;
ოპიოიდური დამოკიდებულების მქონე პაციენტის ცხოვრების ხარისხის და კეთილდღეობის გაუმჯობესება.
წამალდამოკიდებულების მკურნალობას მრავალი მიზეზი აქვს. ნარკოტიკების მოხმარების შემცირების გარდა, მას შეუძლია დაეხმაროს ნარკოტიკის მომხმარებელს, სხვა მხრიდან შეხედოს საკუთარ თავს და თავის პრობლემას, გაუძლიეროს საკუთარი თავის რწმენა და მისცეს ძალა, შეცვალოს თავისი ცხოვრება; ასევე მკურნალობას შეუძლია, პაციენტს გაუზარდოს თვითშეფასება და ჩაუნერგოს იმედი; ამავე დროს, მისაწვდომი გახადოს ფიზიკური და ფსიქიატრიული, ასევე სოციალური დახმარება, ხელი შეუწყოს პაციენტის ოჯახს და თავად პაციენტს.
უმრავლეს შემთხვევაში, მკურნალობა საჭიროა ხანგრძლივი დროის განმავლობაში, ან მთელი სიცოცხლის მანძილზეც კი. მკურნალობის მიზანი ამგვარ შემთხვევებში არის არა მხოლოდ ოპიოიდების მოხმარების შემცირება, არამედ ჯანმრთელობის და სოციალური ცხოვრების გაუჯობესება; პაციენტების დახმარება, თავიდან აიცილონ ნარკოტიკის მოხმარების მძიმე შედეგები. მკურნალობის ხანგრძლივი პერიოდი, რომელიც მრავალ დაავადებას ახლავს, არ უნდა განვიხილოთ, როგორც წარუმატებლობა. ეს სიცოცხლის გახანგრძლივების და ცხოვრების ხარისხის გაუმჯობესების ეფექტიანი გზაა (ხარჯების მხრივ), რაც ხელს უწყობს ცვლილებების და გამოჯანმრთელების ბუნებრივ და ხანგრძლივ პროცესს.
ფართო გაგებით, არსებობს ოპიოიდური დამოკიდებულების მკურნალობის ორი მეთოდი: ერთი - ოპიოიდების მოხსნაზე დამყარებული და მეორე - აგონისტებით მხარდამჭერი თერაპია.
 |
7.8.1 3.8.1 ოპიოიდების მოხსნის მართვა |
▲back to top |
ოპიოიდების მოხსნის ფარმაკოლოგიური მართვა, ჩვეულებრივ, ქვემოთ ჩემოთვლილი ერთერთი მეთოდით ხდება:
ოპიოიდური აგონისტების (მაგ. მეთადონის) მიღების თანდათანობით შეწყვეტა;
ნაწილობრივი აგონისტის (მაგ. ბუპრენორფინის) ხანმოკლე მოხმარება;
ოპიოიდის უეცარი შეწყვეტა და ალფა-2 ადრენერგული აგონისტების მოხმარება აღკვეთის სიმპტომების შესამსუბუქებლად.
პრაქტიკაში, პაციენტების უმრავლესობა ოპიოიდების მიღებას ოპიოიდების მოხსნის დაწყებიდან ექვს თვეში განაახლებს [43, 44]; ეს ნიშნავს, რომ დეტოქსიკაციის ერთი ეპიზოდი არ უნდა იქნეს მიჩნეული ეფექტიან მკურნალობად.
 |
7.8.2 3.8.2 მხარდამჭერი მკურნალობა აგონისტებით |
▲back to top |
აგონისტებით მხარდამჭერი მკურნალობა, ჩვეულებრივ, გულისხმობს ოპიოიდური აგონისტის (მაგ. მეთადონი) ან ნაწილობრივი აგონისტის (მაგ. ბუპრენორფინი) ყოველდღე მიღებას. მიღებული ოპიოიდური ეფექტის სტაბილური დონე დამოკიდებული მომხმარებლის მიერ აღიქმება, როგორც არა ინტოქსიკაცია ან აღკვეთა, არამედ როგორც „ნორმალური“ მდგომარეობა. აგონისტებით ჩანაცვლებითი მკურნალობის მიზნებია:
აკრძალული ოპიოიდების მოხმარების შემცირება ან შეწყვეტა;
ინექციების და მათთან დაკავშირებული სისხლით გადამდები ვირუსების გადაცემის რისკის შემცირება ან სრული აღკვეთა;
ზედოზირების რისკის შემცირება;
კრიმინალური აქტივობის შემცირება;
ფსიქოლოგიური და ფიზიკური ჯანმრთელობის გაუმჯობესება.
პრაქტიკულად, პაციენტების უმრავლესობა, რომლებიც იწყებენ ოპიოიდური აგონისტებით ჩანაცვლებით მკურნალობას, წყვეტს ჰეროინის მოხმარებას, ან იშვიათად იყენებს მას. ჰეროინის რეგულარული მოხმარება დაფიქსირებულია შემთხვევათა მხოლოდ 20-30%-ში [43, 45]. თუმცა, აგონისტებით მხარდამჭერი მკურნალობის შეწყვეტის შემდეგ ხშირია ჰეროინის გამოყენების რეციდივი [46, 47, 48]. არსებული მონაცემები არასაკმარისია იმისათვის, თუ ვინ, როდის და როგორ უნდა შეწყვიტოს ოპიოიდური აგონისტებით მხარდამჭერი თერაპია.
 |
7.8.3 3.8.4 ფსიქოსოციალური დახმარება |
▲back to top |
ფსიქოსოციალური დახმარება ოპიოიდური დამოკიდებულების მკურნალობის დროს შეიძლება მრავალმხრივი იყოს. იგი გულისხმობს, რომ პროფესიულ თუ სხვა სფეროში საზოგადოებას შეუძლია დაეხმაროს ოპიოიდების მომხმარებელს ფსიქოლოგიური ჯანმრთელობის და სოციალური გარემოს გაუმჯობესებაში, სიცოცხლის ხარისხის და ხანგრძლივობის გაზრდაში. დახმარება შეიძლება იყოს მარტივი (საკვების და თავშესაფრის უზრუნველყოფა) და კომპლექსური (მაგ., სტრუქტურირებული ფსიქოთერაპია); ეს საკითხი განხილულია მე-6 თავში.
 |
8 4 სახელმძღვანელო ჯანმრთელობის სისტემისთვის ქვეყნის ცენტრალურ და რეგიონულ დონეზე |
▲back to top |
ჯანმოს კონსტიტუციით [49] ჯანმრთელობა განსაზღვრულია, როგორც „სრული ფიზიკური, ფსიქიკური და სოციალური კეთილდღეობის მდგომარეობა და არა უბრალოდ დაავადების ან უძლურების არარსებობა“. მასში გაცხადებულია, რომ ჯანმრთელობის ყველაზე მაღალი შესაძლო სტანდარტით სარგებლობა ყველა ადამიანის ერთ-ერთი ფუნდამენტური უფლებაა რასის, რელიგიის, პოლიტიკური მრწამსის, ეკონომიკური და სოციალური პირობების მიუხედავად. კონსტიტუციაში ასევე ნათქვამია, რომ ყველა ადამიანის ჯანმრთელობა ფუნდამენტური პირობაა მშვიდობისა და უსაფრთხოების მისაღწევად და დამოკიდებულია ადამიანებსა და სახელმწიფოებს შორის ფართო თანამშრომლობაზე. ამის მსგავსად, ოტავას ქარტიაში
[50] განმარტებულია კავშირი ჯანმრთელობასა და უფრო ფართო სოციალურ პოლიტიკას და ჯანმრთელობის სისტემებს შორის; ხაზგასმით არის აღნიშნული ჯანდაცვის სისტემის დონეზე განხორციელებული ქმედებების მნიშვნელობა.
ეს სახელმძღვანელო მოიცავს ორი სახის რეკომენდაციებს ჯანდაცვის სისტემის დონეზე სამოქმედოდ - „მინიმალურს“ და „ოპტიმალურს“. რეკომენდაციები, რომლებიც აღნიშნულია როგორც „მინიმალური“, ყველა შემთხვევაში მიჩნეულია როგორც მინიმალური სტანდარტი; ისინი უნდა განიხილებოდეს როგორც მინიმალური მოთხოვნილება ოპიოიდური დამოკიდებულების მკურნალობის უზრუნველსაყოფად. „ოპტიმალური“ რეკომენდაციები კი წარმოადგენს საუკეთესო პრაქტიკას ოპიოიდური დამოკიდებულების მკურნალობით საზოგადოებრივი ჯანმრთელობის მაქსიმალური სარგებლის მისაღებად.
 |
8.1 4.1 საერთაშორისო რეგულაციები |
▲back to top |
სახელმწიფოები საერთაშორისო რეგულაციების სივრცეში მუშაობენ; მეთადონი და ბუპრენორფინი საერთაშორისო კონტროლს დაქვემდებარებული მედიკამენტებია. 1961 წლის კონვენცია ნარკოტიკების შესახებ (რომელშიც შესწორებები 1972 წელს შევიდა) და 1971 წლის კონვენცია ფსიქოტროპული ნივთიერებების შესახებ განსაზღვრავს კონტროლის სპეციფიკურ მოთხოვნებს ამ ნივთიერებების მიმართ (ამ კონვენციების მოთხოვნების დეტალები მოცემულია მე-7 დანართში). კონვენციები ასევე მოიცავს მოთხოვნებს ნარკოტიკებზე ან ფსიქოტროპულ ნივთიერებებზე დამოკიდებული ადამიანების მკურნალობაზე ხელმისაწვდომობის შესახებ. ამ კონვენციების ორი ძირითადი მიზანი არის ნარკოტიკების და ფსიქოტროპული ნივთიერებების (მათ შორის ოპიოიდების) ხელმისაწვდომობის უზრუნველყოფა მხოლოდ სამედიცინო და სამეცნიერო მიზნებისათვის და მათი სხვა მიზნით გამოყენების თავიდან აცილება.
შესაბამისი პასუხისმგებლობის მქონე ადამიანები უნდა გაეცნონ ოპიოიდების მოწოდების, განაწილების, შენახვის და გამოწერის საერთაშორისო და საკანონმდებლო რეგულაციებს. თუ ქვეყანას არ აქვს აგონისტებით მხარდამჭერი თერაპიის მედიკამენტების გამანაწილებელი და უზრუნველმყოფი რეგულაციები, საჭიროა მათი დროული შემუშავება არსებული კონვენციების თანახმად. კანონები და რეგულაციები უნდა იძლეოდეს პაციენტებისთვის გამოწერილი მეთადონის და ბუპრენორფინის მიცემის საშუალებას ადვილად მისაწვდომი დანაწილების პუნქტებიდან - ზედამხედველობით ან სახლში წასაღები დოზის სახით. ამავდროულად, თავიდან უნდა ავიცილოთ მათი მოხმარება არასამედიცინო დანიშნულებით.
ისინი, ვინც მკურნალობას ატარებენ, უნდა ეცნობოდნენ ქვეყნის და რეგიონების მასშტაბით არსებულ მოთხოვნებს და უზრუნველყოფდნენ ჩატარებული მკურნალობის შესაბამისობას არსებულ კანონებთან და რეგულაციებთან.
ადამიანის უფლებების დაცვის პასუხისმგებლობების განმსაზღვრელი საერთაშორისო შეთანხმებები ასევე ვრცელდება ოპიოიდების მკურნალობაზეც (იხ. ეთიკური საკითხები).
 |
8.2 4.2 ოპიოიდური დამოკიდებულება როგორც ჯანმრთელობის პრობლემა |
▲back to top |
ოპიოიდური დამოკიდებულება თავისთავად უნდა განვიხილოთ, როგორც ჯანმრთელობის და არა სამართლებრივი პრობლემა. ოპიოიდურ დამოკიდებულებასთან დაკავშირებული მრავალი სამედიცინო პრობლემის და ფარმაკოლოგიური მკურნალობის ბუნების გათვალისწინებით, ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობის უზრუნველყოფა ჯანდაცვის პრიორიტეტი უნდა იყოს. ეს გაცხადებულია 1961 წლის კონვენციაში ნარკოტიკების შესახებ, რომელიც მოუწოდებს ყველა მონაწილე მხარეს, განსაკუთრებული ყურადღება მიაქციოს და ყველა პრაქტიკული ზომა მიიღოს ნარკოტიკების მავნედ მოხმარების თავიდან აცილებისა და მკურნალობისათვის. კონვენციაში ასევე გამოთქმულია მოსაზრება, რომ ნარკომომხმარებლებში, რომელთაც ჩადენილი აქვთ დასჯადი დანაშაული, მკურნალობა შეიძლება ხელმისაწვდომი იყოს როგორც დაპატიმრების ან დასჯის ალტერნატივა (ან განხორციელდეს მათთან ერთად).
 |
8.3 4.3 მკურნალობის ეროვნული პოლიტიკა |
▲back to top |
როცა მკურნალობის სისტემა ამა თუ იმ ქვეყანაში მუშავდება, იგი უნდა დაიგეგმოს როგორც საზოგადოების საერთო რესურსების ნაწილი, რომელიც იხარჯება ჯანმრთელობასა და სოციალურ პრობლემებზე (ჯანმოს ექსპერტთა კომისიის 30-ე ანგარიში) [10, 50].
პოლიტიკა უნდა განსაზღვრავდეს ოპიოიდური დამოკიდებულების პრობლემის თავიდან აცილების და მკურნალობის მეთოდს/მიდგომას. იგი უნდა ეფუძნებოდეს ეპიდემიოლოგიურ მონაცემებს, ინფორმაციას მკურნალობის ეფექტიანობის შესახებ, ქვეყნის რესურსებს და საზოგადოების ღირებულებებს.
მკურნალობის საჭიროების შეფასება მნიშვნელოვანია ამ სერვისის დაგეგმვისთვის და მისი ხელმისაწვდომობის განსაზღვრისთვის მოსახლეობის სხვადასხვა ჯგუფებში. ოპიოიდებზე დამოკიდებული ადამიანების რაოდენობის განსაზღვრა პოპულაციაში (ოჯახების მიმოხილვითი კვლევების მიხედვით) სირთულეებთან არის დაკავშირებული, რადგან ეს ინფორმაცია ფართო ეპიდემიოლოგიურ კვლევებში საკმარისად არ არის წარმოდგენილი. ალტერნატიული მეთოდები, რომლებიც შეიძლება უფრო ეფექტიანი იყოს, არის capture-recapture, უკუპროეცირება და გავრცელების კოეფიციენტის მეთოდები [51]. ჯანმოს შემუშავებული აქვს სახელმძღვანელო ოპიოიდებზე დამოკიდებული ადამიანების რაოდენობის განსაზღვრის შესახებ [52].
მკურნალობის საჭიროება შეიძლება განისაზღვროს მკურნალობის (მათ შორის, პირველადი მკურნალობის) მონიტორინგის სისტემებით. თუმცა, იმ ადამიანების რაოდენობის განსაზღვრისას, რომლებსაც მკურნალობა ესაჭიროებათ, ზოგიერთი პოპულაცია შეიძლება საკმარისად არ იყოს წარმოდგენილი; ამგვარი ჯგუფები მოიცავს ქალებს, ახალგაზრდებს, ქუჩის ბავშვებს, დევნილებს, ღარიბებს და ეთნიკური და რელიგიური უმცირესობის წარმომადგენლებს.
მკურნალობის პროცესში ჩართული პაციენტების რაოდენობის შესახებ ინფორმაციის შეგროვება შესაძლოა ეფექტიანი იყოს მკურნალობის ტიპების მიხედვით. მონაცემები ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაზე მყოფი პაციენტების რაოდენობის შესახებ შეიძლება მივიღოთ იმ „სამკურნალო ცენტრებიდან ან აფთიაქებიდან, საიდანაც ნაწილდება მეთადონი და ბუპრენორფინი. ინფორმაცია გროვდება კონკრეტულ მომენტში ან პერიოდულად. უფრო რთულია ინფორმაციის მიღება იმ პაციენტების რაოდენობაზე, რომელთა მკურნალობის მიზანი ოპიოიდების აღკვეთაა. ეს მოითხოვს მონაცემების თავმოყრას საცხოვრებელი ადგილიდან, ამბულატორიული დაწესებულებებიდან და ჯანდაცვის პირველადი ცენტრებიდან. გრძელვადიანი გამოსავლის შესაფასებელი შედარებით იაფი მეთოდია მიღებული ინფორმაციის შედარება მოსახლეობის აღწერის მონაცემებთან (სიკვდილიანობა).
საჭიროებების შეფასება ფორმალური სისტემატური მცდელობაა საჭირო მომსახურებასა და არსებულ მომსახურებას შორის შეუთავსებლობის განსაზღვრისათვის. შეფასება უზრუნველყოფს რეალურ და სასურველ გამოსავლებს შორის არსებული შეუთავსებლობის დასაბუთებას. შემდეგ მიიღება გადაწყვეტილება ამ შეუთავსებლობების გამოსასწორებლად.
ოპიოიდებზე დამოკიდებული ადამიანებისთვის ფარმაკოლოგიური მკურნალობის დაგეგმვისა და შემუშვებისას უნდა შევაფასოთ საზოგადოებრივი ჯანდაცვის არსებული და პოტენციური პრობლემები, რომლებიც დაკავშირებულია ოპიოიდურ დამოკიდებულებასთან და მკურნალობის მოცვასთან.
რეკომენდაცია (საუკეთესო პრაქტიკა) სტრატეგიულ დოკუმენტში გამოხატული უნდა იყოს მთავრობის პოლიტიკა ოპიოიდური დამოკიდებულების მკურნალობასთან დაკავშირებით. სტრატეგია მიმართული უნდა იყოს სათანადო მოცვის, ხარისხის და მკურნალობის უსაფრთხოებისკენ. |
 |
8.4 4.4. ეთიკური საკითხები |
▲back to top |
 |
8.4.1 4.4.1 სავალდებულო და იძულებითი მკურნალობა |
▲back to top |
დამოუკიდებლობის (ავტონომიურობის) პრინციპის თანახმად (თუ სხვა ეთიკური პრინციპი არ გადაწონის), პაციენტებმა თავად უნდა გააკეთონ მკურნალობის არჩევანი. მაგ., დამოუკიდებლობის პრინციპი შეიძლება გადაიწონოს, როცა ადამიანი უნარშეზღუდულია ფსიქიკური დაავადების გამო და აღარ შეუძლია საკუთარი თავის მოვლა ან როცა ადამიანი საფრთხეს უქმნის სხვებს. ქვეყნების უმრავლესობაში არსებობს შესაბამისი კანონმდებლობა ფსიქიკური ჯანმრთელობის შესახებ, რითაც საჭიროებისამებრ შეიძლება ვისარგებლოთ ოპიოიდური დამოკიდებულების მქონე პაციენტებში. თუმცა, უმეტეს შემთხვევაში, არ მიიჩნევა, რომ ვინც ოპიოიდების მოხმარებას ვერ აკონტროლებს, სხვა მხრივ არ შეუძლია საკუთარი თავის მოვლა.
სიტუაციებში, როდესაც ოპიოიდებზე დამოკიდებული ინდივიდები მსჯავრდებულები არიან ოპიოიდების მოხმარებასთან დაკავშირებული დანაშაულის გამო, სასჯელის ალტერნატივად მათ შეიძლება ოპიოიდური დამოკიდებულების მკურნალობა შესთავაზონ. ამგვარი მკურნალობა არ უნდა იყოს იძულებითი. მკურნალობაზე უარის თქმის ან წარუმატებელი მკურნალობის გამო პაციენტი არ უნდა ისჯებოდეს. ანალოგიურად, შესაძლებელია სასამართლო პროცედურები გადაიდოს მკურნალობის გარკვეული პერიოდის დამთავრებამდე მკურნალობის შედეგების მხედველობაში მისაღებად. ამგვარი პროგრამები, რომლებსაც ოპიოიდებზე დამოკიდებული პაციენტები კრიმინალური სამართლის სისტემიდან გამოჰყავს და მკურნალობას უქვემდებარებს, შეიძლება განხორციელდეს დაპატიმრებისას ან სასამართლომდე. ამ პროგრამებს ზოგჯერ „გადაყვანის“ (diversion) პროგრამებს უწოდებენ. მათი შეფასებისას ვლინდება წარმატებული მკურნალობის მაღალი და რეციდივის დაბალი მაჩვენებელი [53, 54].
რეკომენდაცია (მინიმალური სტანდარტი) ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა არ უნდა იყოს იძულებითი. |
 |
8.4.2 4.4.2 პაციენტების ცენტრალური რეგისტრაცია |
▲back to top |
პაციენტებს უნდა ჰქონდეთ პირადი ინფორმაციის დაცვის უფლება. მათი კონფიდენციალურობა გათვალისწინებულ უნდა იქნეს პაციენტების ცენტრალური რეგისტრაციის სისტემის აწყობისას. ცენტრალურ რეგისტრაციას შემდეგი უპირატესობები აქვს:
თავიდან აგვაცილებს პაციენტების მიერ მეთადონის ან ბუპრენორფინის მიღებას ერთზე მეტი წყაროდან;
შეიძლება გამოვიყენოთ სხვა კონტროლირებულ მედიკამენტებთან (მაგ., სხვა ოპიოიდები) ხელმისაწვდომობის შეზღუდვისთვის, მათზე ცენტრალური ნებართვის მოთხოვნით;
შესაძლებელია უფრო ზუსტი მონაცემების მიღება მკურნალობაში ჩართულ პაციენტთა რაოდენობის შესახებ, ვიდრე იმ შემთხვევებში, როდესაც ცენტრალური რეგისტრაცია არ გამოიყენება.
თუმცა, ცენტრალური რეგისტრაციისას უფრო ადვილად შეიძლება მოხდეს კონფიდენციალურობის დარღვევა და ამის გამო ზოგიერთმა პაციენტმა თავი შეიკავოს მკურნალობაში ჩართვისგან. ასევე, ამან შესაძლოა გამოიწვიოს მკურნალობის დაწყების გადავადება.
ოპიოიდური დამოკიდებულების უსაფრთხო და ეფექტიანი მკურნალობა შეიძლება მოხერხდეს ცენტრალური რეგისტრაციის გარეშეც, რადგან კონფიდენციალურობის დარღვევის შემთხვევაში მას შეუძლია ზიანი მიაყენოს პაციენტს. ის უნდა გამოვიყენოთ მხოლოდ მაშინ, თუ სამთავრობო სტრუქტურებს აქვს კონფიდენციალურობის დაცვის ეფექტიანი სისტემები.
 |
8.5 4.5 დაფინანსება |
▲back to top |
შესაბამისი მკურნალობის მეთოდისთვის ყველა ქვეყანაში მობილიზებული უნდა იყოს დაფინანსება და მკურნალობის თანაბარი ხელმისაწვდომობა. ზოგადად, ეს ნიშნავს ხარჯების მხრივ ყველაზე ეფექტიანი და საყოველთაოდ ხელმისაწვდომი მკურნალობის უზრუნველყოფას.
ოპიოიდური დამოკიდებულების მკურნალობის ღირებულება გავლენას ახდენს მკურნალობის შედეგზე. თუ ფასი ძალიან მაღალია, მკურნალობა არ იქნება ხელმისაწვდომი მოსახლეობის დაბალი ფენებისთვის. ბევრი ოპიოიდდამოკიდებული პაციენტი ვერ ფარავს მკურნალობის ხარჯებს და არ გააჩნია დაზღვევა. როდესაც პაციენტები იხდიან მკურნალობის საფასურს, მკურნალობის გაგრძელების და ჯანმრთელობის გაუმჯობესების მაჩვენებლები უარესია, ვიდრე მაშინ, როცა მკურნალობა უფასოა [55]. მკურნალობაზე პაციენტის მხრიდან მცირედი დანახარჯიც კი შეიძლება მნიშვნელოვანი ხელისშემშლელი ფაქტორი გახდეს.
მკურნალობის ხარჯების დაფარვის მექანიზნებს შეიძლება უნებლიე გავლენა ჰქონდეს შედეგებზე. მაგ., თუ მეთადონის და ბუპრენორფინის მაღალი დოზები უფრო ძვირია, ვიდრე დაბალი, პაციენტმა შეიძლება დაბალი დოზის მიღება აირჩიოს, რაც ცუდი შედეგის მიზეზი ხდება. ამის საპირისპიროდ, თუ პაციენტი იმავეს იხდის დოზის მიუხედავად, მან შეიძლება, საჭიროზე მეტი დოზა მოითხოვოს და ჭარბი მარაგი გაყიდოს. ამის გამო, სამედიცინო პერსონალმა შეიძლება თავი შეიკავოს მედიკამენტის დოზის გაზრდისგან, როცა პაციენტი ამას მოითხოვს.
ასევე მნიშვნელოვანია მედიკამენტის გაცემის ღირებულება. თუ პაციენტი აფთიაქს ან კლინიკას გაცემის საფასურს უხდის მედიკამენტის მიღების ყოველ ჯერზე, შეიძლება არჩიოს, იშვიათად მივიდეს მედიკამენტის მისაღებად.
მართალია, შეუძლებელია, თავიდან ავიცილოთ ყველა უარყოფითი წამაქეზებელი ფაქტორი (მაგ., რომელთაც მოულოდნელი და არასასურველი ეფექტები აქვს), მაგრამ უფასო და ყველასთვის ხელმისაწვდომი მკურნალობა მინიმუმამდე ამცირებს მათ.
იმ ქვეყნებში, სადაც უნივერსალური ჯანდაცვის სისტემა მოქმედებს, იგი უნდა მოიცავდეს ოპიოიდური დამოკიდებულების მკურნალობასაც. თუ ქვეყანას დაზღვევის სისტემა აქვს, ისიც უნდა მოიცავდეს ოპიოიდური დამოკიდებულების მკურნალობას, იმის გათვალისწინებით, რომ ბევრ შემთხვევაში საჭირო იქნება ხანგრძლივი მკურნალობა.
მკურნალობის დაფინანსების მეორე ასპექტი არის მდგრადობა. უმეტესწილად, ოპიოიდური დამოკიდებულების მკურნალობის დასაწყისში გამოიყენება პილოტური დაფინანსება. თუმცა, თუ მკურნალობის გაგრძელების რეალური პერსპექტივა არ არსებობს და პილოტური ფაზის დამთავრების შემდეგ პაციენტს მკურნალობის ფარმაკოთერაპიის გაგრძელება არ შეუძლია, არასასურველია ხანმოკლე დაფინანსების გამოყენება.
ოპიოიდური დამოკიდებულების მკურნალობის სამსახურის შემუშავება და შენარჩუნება უნდა მოხდეს ჯანდაცვის დაფინანსების და უზრუნველყოფის ფართო სისტემების ჩართვით. იმის განსაზღვრა, თუ როგორ ხდება ჯანდაცვისთვის თანხების მობილიზება და გამოყოფა, მნიშვნელოვანია ოპიოიდური დამოკიდებულების მკურნალობის სერვისის სათანადო დაგეგმვისთვის. ბევრ შედარებით მცირე რესურსის მქონე ქვეყანაში მკურნალობის ერთ-ერთი მნიშვნელოვანი ბარიერია ძირითადი ხარჯების გაღება პაციენტის ოჯახის ბიუჯეტიდან. გადასახადებზე დაფუძნებული ჯანმრთელობის დაზღვევის სქემები უკეთეს მექანიზმს ქმნის სამედიცინო მომსახურების ხარჯების დასაფარად, ასევე იქმნება უფრო შესაბამისი საფუძველი ოპიოიდური დამოკიდებულების მკურნალობის მდგრადი სისტემების შექმნისთვის.
ოპიოიდური დამოკიდებულების მკურნალობის დაწყებისა და შენარჩუნებისთვის საჭირო საერთო რესურსების და მასთან დაკავშირებული ღირებულებების განსაზღვრა სტრატეგიული დაგეგმვის მთავარი ელემენტი უნდა იყოს. მართალია, ოპიოიდური დამოკიდებულების მკურნალობის მთელი რიგი პროგრამებისთვის გაკეთებულია ხარჯების შეფასება [56, 57, 58, 59, 60, 61, 62, 63], მაგრამ ისინი ძირითადად შემოიფარგლება მაღალშემოსავლიანი ქვეყნებით, სადაც ჯანმრთელობის დაფინანსების ღირებულება და დონე შეიძლება მნიშვნელოვნად განსხვავდებოდეს დაბალი და საშუალო შემოსავლის მქონე ქვეყნებისგან. მაგ., რესურსების დაგეგმვისას ყველა შემთხვევაში უნდა გავითვალისწინოთ სამედიცინო პერსონალი, მაგრამ ეს ხარჯი დაბალი და საშუალო შემოსავლის მქონე ქვეყნებში საერთო ხარჯის გაცილებით მცირე ნაწილი იქნება (დაბალი ხელფასის გამო); და პირიქით, ამგვარ ქვეყნებში ფინანსების დიდი ნაწილი დაიხარჯება მედიკამენტების შესყიდვასა და გაცემაზე, საწვავზე და აღჭურვილობაზე. ჯანმოს აქვს მეთოდები და საშუალებები, რომლებიც შეიძლება გამოვიყენოთ რესურსების დაგეგმვის და პროგრამის ღირებულების შეფასებისას ცენტრალურ დონეზე [64].
რეკომენდაცია (მინიმალური სტანდარტი) მკურნალობა ხელმისაწვდომი უნდა იყოს მოსახლეობის არაპრივილეგირებული ფენებისთვის. რეკომენდაცია (მინიმალური სტანდარტი) მკურნალობის დაწყებისას უნდა არსებობდეს სერვისის ფინანსური ხელმისაწვდომობის რეალური პერსპექტივა. |
რეკომენდაცია (საუკეთესო პრაქტიკა) ოპტიმალური დაფარვის და მკურნალობის კარგი შედეგების მისაღწევად, ოპიოიდური დამოკიდებულების მკურნალობა უნდა იყოს უფასო ან იფარებოდეს საზოგადოებრივი ჯანდაცვის დაზღვევით. |
 |
8.6 4.6 მკურნალობის მოცვა |
▲back to top |
ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობა ხელმისაწვდომი უნდა იყოს ყველასთვის, ვისაც ის სჭირდება, მათ შორის, ციხეებში (ამ შემთხვევაში ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის ეფექტიანობა კარგად უნდა იყოს დასაბუთებული) და სხვა ჩაკეტილ დაწესებულებებში [65, 66, 67]. ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა არ უნდა შეფერხდეს თავისუფლების აღკვეთის დაწესებულებებში პაციენტის მოხვედრის ან იქიდან გათავისუფლების თუ სხვა დაწესებულებაში გადაყვანის შემთხვევაში.
მკურნალობის პროგრამები უნდა იყოს მაქსიმალურად კომფორტული; მაგ., ფიზიკურად იოლად ხელმისაწვდომი, მოსახერხებელი დროის თვალსაზრისით, უაზრო შეზღუდვების გარეშე; შესაძლებელი უნდა იყოს მათი გაფართოება მოთხოვნის შესაბამისად. პროგრამას უნდა ჰქონდეს შესაბამისი დაწესებულებები, დაფიქსირებული მიღების საათები, რაც შესაძლებელს გახდის პერსონალის და პაციენტის კონფიდენციალურობის და უსაფრთხოების დაცვას; მედიკამენტი უნდა გაიცეს შესაბამისი და ხელმისაწვდომი დაწესებულებებიდან, მედიკამენტების შენახვა უნდა მოხდეს საიმედოდ და უსაფრთხოდ.
რეკომენდაცია (მინიმალური სტანდარტი) ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობა უნდა იყოს ფართოდ ხელმისაწვდომი, რაც შეიძლება მოიცავდეს მკურნალობას პირველადი ჯანდაცვის დაწესებულებებში. თანმხლები დაავადებების მკურნალობა შეიძლება ჩატარდეს პირველადი ჯანდაცვის დაწესებულებებში, თუ ხელმისაწვდომია შესაბამისი სპეციალისტის კონსულტაცია. რეკომენდაცია (საუკეთესო პრაქტიკა) ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობა ხელმისაწვდომი უნდა იყოს ყველასთვის, ვისაც ის ესაჭიროება, მათ შორის, ციხეში და სხვა დახურულ დაწესებულებებში მყოფი პაციენტებისთვის. |
 |
8.6.1 4.6.1 პირველადი დახმარება |
▲back to top |
მიუხედავად იმისა, რომ ოპიოიდური დამოკიდებულების მკურნალობის ინტეგრაცია პირველადი ჯანდაცვის სისტემაში ხელმისაწვდომობის გაზრდის ერთ-ერთი გზაა, ეს ყოველთვის არ არის შესაძლებელი. პირველადი ჯანდაცვის ექიმებს, ჩვეულებრივ, დახმარება სჭირდებათ სპეციალისტებისგან რჩევების მიღების, სწავლების, კონსულტაციის და მათთან პაციენტების გაგზავნის სახით. ამგვარი დახმარების პირობებში უსაფრთხოდ შეიძლება პირველადი ჯანდაცვის დაწესებულებებში თანმხლები დაავადების მქონე მრავალი პაციენტის მკურნალობა.
ყოველივე ზემოთქმულის გათვალისწინებით სათანადო გარემოში ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა, ოპიოიდების აღკვეთის მართვა და რეციდივის პრევენცია სრულიად განხორციელებადია ამგვარ დაწესებულებებში.
რამდენიმე კლინიკურ კვლევაში ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა პირველადი ჯანდაცვის დაწესებულებაში ჩატარდა [68, 69, 70]. ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაში ზოგადი პროფილის ექიმების ჩართვა მნიშვნელოვნად ზრდის სერვისის შესაძლებლობებს. მკურნალობაში ჩართული პაციენტების რაოდენობა სწრაფად გაიზარდა ქვეყნებში, სადაც ეს მეთოდი იქნა მიღებული [71]. პირველადი ჯანდაცვის დაწესებულებებში მკურნალობას ის უპირატესობაც აქვს, რომ ნარკომანიის სამედიცინო და ფსიქიატრიული მკურნალობა იქცევა ძირითადი სამედიცინო მომსახურების ნაწილად, მცირდება ნარკომანიასთან დაკავშირებული სტიგმა და სამედიცინო პერსონალის პროფესიული იზოლაცია. ინტეგრაცია ასევე ამცირებს პრობლემებს იმ კლინიკებში, სადაც ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაში ჩართული ბევრი პაციენტი გროვდება. კლინიკაში პაციენტებს შორის კონტაქტმა შეიძლება ხელი შეუწყოს მათ შორის ნარკოტიკების გასაღებას და მკურნალობისთვის არახელსაყრელი გარემოს შექმნას. კლინიკის გარეთ ნარკოტიკების მომხმარებელთა ჯგუფი სავარაუდოდ იმ ადამიანების სამიზნე გახდება, რომლებისთვისაც მიუღებელია ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა.
ამრიგად, ოპიოიდების მოხსნის მართვა და რეციდივის პრევენციის უზრუნველყოფა პირველადი ჯანდაცვის დაწესებულებებში იმავე ეფექტითაა შესაძლებელი, როგორც სპეციალურ კლინიკებში, მაგრამ ნაკლები ღირებულებით [72,73].
 |
8.6.2 4.6.2 საპყრობილეები |
▲back to top |
სათანადო სამედიცინო დახმარება პატიმრებს არ უნდა მოაკლდეთ ციხეში ყოფნის გამო. ეს, ჩვეულებრივ, გულისხმობს, რომ საპყრობილეს გარეთ არსებული მკურნალობის არჩევანი ხელმისაწვდომი უნდა იყოს საპყრობილეშიც. ციხის პირობებში შესაძლებელი უნდა იყოს ოპიოიდების აღკვეთის მდგომარეობის მართვა, აგონისტებით მხარდამჭერი თერაპია და ნალტრექსონით მკურნალობა. პატიმრებს არ უნდა აიძულებდნენ რომელიმე კონკრეტულ მკურნალობას.
ოპიოიდური აგონისტებით მკურნალობა ციხეებში
სარგებელი, რომელიც მოაქვს ციხეებში ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას, მოიცავს საინექციო ნარკოტიკების მოხმარების შემცირებას ციხეში, ზრდის მკურნალობის გაგრძელების შანსს ციხის დატოვებისას და ამცირებს ციხეში დაბრუნების მაჩვენებელს. პოტენციური ზიანი მოიცავს მედიკამენტის არადანიშნულებისამებრ მოხმარებას, აივ-ის გავრცელებას ამგვარი მედიკამენტის ინექციისას დაბინძურებული საინექციო ინვენტარით სარგებლობის გამო. პოტენციური ზიანის თავიდან ასაცილებლად ციხის პირობებში რეკომენდებული არ არის დოზების მიცემა ზედამხედველობის გარეშე. რისკის შემცირება შეიძლება მეთადონის განზავებით და მეთადონის მომხმარებელი პაციენტების სხვა პატიმრებისგან იზოლაციით დოზის მიღებიდან 30 წუთის განმავლობაში.
რადგან ბუპრენორფინი ენის ქვეშ მისაღები ტაბლეტია, რომლის გახსნას 15 წუთი სჭირდება, მასზე ზედამხედველობა ციხის პირობებში რთულია; ზოგჯერ პაციენტებზე არის ზეწოლა სხვა პატიმრებისგან მედიკამენტის არადანიშნულებისამებრ გამოყენების მიზნით [74]. ზედამხედველობის ეფექტიანობის გაზრდის მეთოდები მოიცავს ტაბლეტის დაფშვნას ან გარსით დაფარვას; პაციენტს უნდა ვთხოვოთ, დოზის მიღებისას ხელები უკან წაიღოს, დოზის მიღების შემდეგ კი უნდა დავათვალიეროთ პაციენტის პირის ღრუ. თუ ბუპრენორფინზე მკაცრი ზედამხედველობა რთულდება, შესაძლოა უმჯობესი იყოს მეთადონის გამოყენება.
მკურნალობის პოლიტიკის განმსაზღვრელებმა და ციხის ადმინისტრატორებმა უნდა უზრუნველყონ საჭირო კავშირი ციხის ჯანმრთელობის სამსახურსა და ციხის გარეთ არსებულ აგონისტებით მხარდამჭერი თერაპიის სისტემას შორის. მკურნალობის უწყვეტობის მცირე შეფერხებაც კი ძალიან მძიმეა პაციენტისთვის და იზრდება აკრძალული ოპიოიდების მიღების განახლების რისკი. ამდენად, ოპიოიდების აგონისტებით მხარდამჭერი მკურნალობა არ უნდა შეწყდეს ციხის დატოვებისას. ეს ნიშნავს, რომ ციხიდან გამოსვლის დღიდანვე უნდა გაგრძელდეს ციხის გარეთ ოპიოიდური აგონისტებით მხარდამჭერი თერაპია.
პატიმრებს, რომლებიც არ არიან ჩართულნი მკურნალობაში, უნდა მიეცეთ თერაპიის მეთადონით ან ბუპრენორფინით დაწყების შესაძლებლობა მაშინაც კი, თუ მათ სასჯელის მოხდამდე ცოტა დრო აქვთ დარჩენილი. ციხეში ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის დაწყება ამცირებს დოზის გადაჭარბების და სიკვდილის მაღალ რისკს ციხის დატოვების შემდეგ, ასევე - ციხეში ხელახლა მოხვედრის რისკსაც.
 |
8.7 4.7 რა სახის მკურნალობა უნდა იყოს ხელმისაწვდომი |
▲back to top |
თუ სხვადასხვა ქვეყნებს შესწევს ამის ძალა, სასურველია ოპიოიდური აგონისტებით მხარდამჭერი თერაპია ხელმისაწვდომი იყოს როგორც მეთადონით, ისე ბუპრენორფინით. როდესაც პაციენტს აღენიშნება გვერდითი მოვლენები ერთი პრეპარატისგან, ან რომელიმე მათგანით მკურნალობას შედეგი არ მოჰყვება, ორივე მედიკამენტზე ხელმისაწვდომობა ალტერნატივის საუკეთესო საშუალებაა. ყოველივე ეს ზრდის ოპიოიდური დამოკიდებულების მქონე მკურნალობაში ჩართული ადამიანების რიცხვს და მკურნალობის ეფექტიანობას მოცემული პაციენტისთვის შესაბამისი მკურნალობის შერჩევის შესაძლებლობის გამო. დამატებით, ალფა-2 ადრენერგულ აგონისტებზე ხელმისაწვდომობა ოპიოიდების აღკვეთის მდგომარეობის მართვისთვის ზრდის არჩევანს მათთვის, ვისაც მაქსიმალურად სწრაფად სურს ოპიოიდებისგან გათავისუფლება ან ოპიოიდების მოხსნის შემდეგ ნალტრექსონის მიღების დაწყება. ნალტრექსონზე ხელმისაწვდომობა ოპიოიდური აღკვეთის მდგომარეობიდან გამოსვლის შემდეგ ასევე ღირებული დამატებითი არჩევანია, რადგან იგი ამცირებს რეციდივის რისკს.
რეკომენდაცია (მინიმალური სტანდარტი) ფარმაკოლოგიური მკურნალობის აუცილებელ არჩევანში უნდა შედიოდეს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა და ოპიოიდების მოხსნის მართვის სერვისი. სულ მცირე, ეს უნდა მოიცავდეს მეთადონს ან ბუპრენორფინს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობისთვის და მოსხნის ამბულატორიული მართვისთვის. რეკომენდაცია (საუკეთესო პრაქტიკა) ფარმაკოლოგიური მკურნალობის არჩევანი უნდა მოიცავდეს როგორც მეთადონს, ისე ბუპრენორფინს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობისთვის და ოპიოიდის მოხსნის მართვისთვის, ალფა-2 ადრენერგულ აგონისტებს - ოპიოიდების მოხსნისთვის, ნალტრექსონს - რეციდივის პრევენციისთვის და ნალოქსონს ზედოზირების მკურნალობისთვის. |
 |
8.8 4.8 ზედამხედველობა დოზირებაზე მეთადონით და ბუპრენორფინით მხარდამჭერი მკურნალობის დროს |
▲back to top |
ეს ნაწილი უნდა წაიკითხოთ ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის ნაწილთან ერთად (ნაწილი 6.4). დოზაზე ზედამხედველობის გარეშე მეთადონი და ბუპრენორფინი შეიძლება მოხმარებულ იქნეს უკანონოდ, რაც ზრდის ზედოზირების, ინექციის და სისხლით გადამდები ვირუსების გავრცელების რისკს. თუმცა, ყოველ დოზაზე ზედამხედველობა ძალზე ზღუდავს პაციენტს და ამცირებს მკურნალობის ხელმისაწვდომობას. დოზებზე ინტენსიური ზედამხედველობა შემაწუხებელია, მაგრამ არც ისე დამთრგუნველია პაციენტისთვის. პირიქით, მკურნალობის საწყის ფაზაში შეიძლება სასარგებლოც იყოს.
რეგულაციები და კანონები მეთადონის და ბუპრენორფინის დოზაზე ზედამხედველობის შესახებ უნდა შეესაბამებოდეს საერთაშორისო შეთანხმებებს და ასახავდეს საზოგადოებისთვის მისაღებ თანაფარდობას მკურნალობის მისაწვდომობასა და მედიკამენტის არამიზნობრივად გამოყენების რისკს შორის. პროგრამები, სადაც პრეპარატის შავ ბაზარზე მოხვედრის დიდი რისკი არსებობს, არ არის სასარგებლო პაციენტისთვის. სამედიცინო პერსონალს შეუძლია, შეარჩიოს მედიკამენტის არასათანადო დანიშნულებით გამოყენების ნაკლები რისკის მატარებელი პაციენტები და მათზე დოზები ნაკლები ზედამხედველობით გაანაწილოს (ნაწილი 4.6).
უმეტესწილად, პერსონალის სწავლება, სახლში მისაღები დოზების ადეკვატურად გაცემა და ნორმალური საკანონმდებლო შეზღუდვები მინიმუმამდე ამცირებს პრეპარატის სხვა დანიშნულებით მოხმარებას. პროგრამები უფრო მდგრადი იქნება, თუ იარსებებს სისტემები პრეპარატების არადანიშნულებით მოხმარების თავიდან ასაცილებლად და ეს სისტემები მონიტორინგს გაუწევს მკურნალობის დადებით ეფექტს. სულ მცირე, ეს უნდა მოიცავდს სისტემებს, რომლებიც შეისწავლის პრეპარატების არადანიშნულებით მოხმარების სიხშირეს (ნაწილი 5.7).
 |
9 5 სახელმძღვანელო პროგრამის მენეჯერებისა და კლინიკის ხელმძღვანელებისთვის |
▲back to top |
ეს ნაწილი უპირველესად განკუთვნილია კლინიკის ხელმძღვანელების და ადმინისტრატორებისთვის, რომელთა მოვალეობაა ოპიოიდური დამოკიდებულების მკურნალობის ორგანიზება, განხორციელება და მომსახურების სტანდარტის უზრუნველყოფა.
 |
9.1 5.1 კლინიკური მართვა |
▲back to top |
კლინიკური მართვა გულისხმობს კლინიკური გამოსავლის ანგარიშგების მექანიზმს. ჩვეულებრივ, ეს კლინიკის ხელმძღვანელის, ადმინისტრატორის ან ორივეს მოვალეობაა. მათ უნდა უზრუნველყონ:
პერსონალის ადეკვატურად შერჩევა, მათი სწავლება და მათზე ზედამხედველობა;
სათანადო კლინიკური პროტოკოლები და პროცედურები:
- მკურნალობის სერვისის სტრუქტურის განსაზღვრისათვის;
- ხარისხის შეფასების და გაუმჯობესების მექანიზმების შემუშავებისთვის;
- პრაქტიკის არსებულ კანონებთან და პროფესიულ მოთხოვნილებებთან შესაბამისობის უზრუნველსაყოფად.
ოპიოიდური დამოკიდებულების მკურნალობის მინიმალური სტანდარტების უზრუნველსაყოფად, სულ მცირე, საჭიროა კლინიკური მართვის პროცესის ორგანიზება. იდეალურ შემთხვევაში, კარგად განვითარებული კლინიკური მართვის პროცესი განაპირობებს ოპიოიდური დამოკიდებულების უსაფრთხო და ეფექტიან მკურნალობას.
როცა მკურნალობა ტარდება ჯანდაცვის სისტემის გარეთ (მაგ. ციხეში) და არა სამედიცინო პერსონალის პასუხისმგებლობით, საჭიროა ანგარიშგების დასაბუთებული ჯაჭვი ჯანმრთელობის გამოსავლების გასაცნობად.
საუკეთესო პრაქტიკაა, როდესაც მკურნალობის პირველად პასუხისმგებლობას იღებს ჯანდაცვის სისტემა, რადგან ამ დროს უფრო ადვილია კლინიკური ანგარიშგების დაწესება და შენარჩუნება.
რეკომენდაცია (მინიმალური სტანდარტი) ოპიოიდური დამოკიდეულების მკურნალობის მინიმალური სტანდარტების უზრუნველსაყოფად მკურნალობის სამსახურს უნდა ჰქონდეს კლინიკური მართვის სისტემა კლინიკური ანგარიშგების ჯაჭვით. რეკომენდაცია (საუკეთესო პრაქტიკა) ოპიოიდური დამოკიდებულების მკურნალობა უნდა ჩატარდეს ჯანდაცვის სისტემაში. საჭიროა კლინიკური მართვის პროცესის არსებობა, რათა მიღწეულ იქნეს ოპიოიდური დამოკიდებულების უსაფრთხო და ეფექტიანი მკურნალობა. პროცესი უნდა იყოს გამჭვირვალე და განმარტებული კლინიკური მართვის დოკუმენტში. |
 |
9.2 5.2 ეთიკური პრინციპები და თანხმობა |
▲back to top |
ეკონომიკური, სოციალური და კულტურული უფლებების საერთაშორისო კონვენციის [75] მე-12 მუხლში განმარტებული დამოუკიდებელი გადაწყვეტილების და ჯანმრთელობის ყველაზე მაღალი შესაძლო სტანდარტის მიღების უფლების შესაბამისად, ადამიანს უნდა ჰქონდეს თავისუფალი არჩევანის უფლება, მიიღოს თუ არა მონაწილეობა მკურნალობაში.
ჯანმო-ის „ფსიქიკური ჯანმრთელობის, ადამიანის უფლებების და კანონმდებლობის რესურსების წიგნში“ [76] ნათქვამია, რომ თანხმობა რომ ძალაში იყოს, იგი უნდა აკმაყოფილებდეს შემდეგ კრიტერიუმებს:
„ადამიანს/პაციენტს, რომელიც იძლევა თანხმობას, უნდა ჰქონდეს ამისათვის შესაბამისი კომპეტენცია; კომპეტენტურობა იგულისხმება, თუ ამის საპირისპირო რაიმე მონაცემი არ არის;
თანხმობა მიღებულ უნდა იქნეს დამოუკიდებლად, მუქარის და არასათანადო ზეწოლის გარეშე;
საჭიროა ინფორმაციის ადეკვატურად მიწოდება. ინფორმაცია უნდა მივაწოდოთ შეთავაზებული მკურნალობის მიზნის, მეთოდის, სავარაუდო ხანგრძლივობის და მოსალოდნელი სარგებლის შესახებ; ასევე, შესაძლო ტკივილის, დისკომფორტის, შეთავაზებული მკურნალობის რისკის და გვერდითი მოვლენების შესახებ. უნდა მოხდეს ამ ინფორმაციის განხილვა პაციენტთან;
კარგი კლინიკური პრაქტიკის მიხედვით, თუ შესაძლებელია, პაციენტს უნდა შევთავაზოთ მკურნალობის ალტერნატიული მეთოდები, განსაკუთრებით, რომლებიც ნაკლებად ინვაზიურია;
ინფორმაცია უნდა მივაწოდოთ პაციენტისთვის გასაგებ ენაზე;
პაციენტს უნდა ჰქონდეს უფლება, უარი თქვას მკურნალობაზე ან შეწყვიტოს ის;
პაციენტს უნდა განვუმარტოთ მკურნალობაზე უარის შედეგები საავადმყოფოდან გაწერის ჩათვლით;
თანხმობა დასაბუთებული უნდა იყოს პაციენტის სამედიცინო ჩანაწერებში;
მკურნალობაზე თანხმობის უფლება გულისხმობს, რომ არსებობს მკურნალობაზე უარის თქმის უფლებაც. თუ მიგვაჩნია, რომ პაციენტს შეუძლია განაცხადოს თანხმობა, უარის დროსაც უნდა ვცეთ პატივი მის გადაწყვეტილებას“.
ოპიოიდური დამოკიდებულების მქონე პაციენტებისგან ინფორმირებული თანხმობის მიღებისას უნდა გავითვალისწინოთ, რომ ინტოქსიკაციის ან ოპიოიდური აღკვეთის მდგომარეობის დროს ისინი შეიძლება არ იყვნენ ადეკვატურნი ინფორმირებული თანხმობისათვის. ამ შემთხვევაში, მკურნალობა შეიძლება დავიწყოთ და თანხმობა პაციენტისგან მკურნალობის დაწყების შემდეგ მივიღოთ (როგორც კი მას მოეხსნება ინტოქსიკაციის ან ოპიოიდური აღკვეთის მდგომარეობის სიმპტომები). ზოგიერთ შემთხვევაში, ეს შეიძლება ნიშნავდეს მკურნალობის მეთოდის (ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის ოპიოიდების მოხსნით ან პირიქით) შეცვლას.
როცა განვიხილავთ რისკებს პაციენტებისთვის (რომლებიც იწყებენ ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას) ინფორმირებული თანხმობის მიღების პროცესში, მნიშვნელოვანია გავითვალისწინოთ ზედოზირების გაზრდილი რისკი მკურნალობის პირველ კვირებში და ოპიოიდური აღკვეთის მდგომარეობის სიმპტომები, რომლებიც პაციენტს შეიძლება აღენიშნებოდეს ოპიოიდური აგონისტებით მკურნალობის შეწყვეტისას. პაციენტები, რომლებიც ირჩევენ ოპიოიდების მოხსნას და თავშეკავებაზე ორიენტირებულ მკურნალობას, განსაკუთრებით უნდა გავაფრთხილოთ ოპიოიდების მიღების განახლებისას ზედოზირების რისკის არსებობაზე.
რეკომენდაცია (მინიმალური სტანდარტი) პაციენტებისგან უნდა მივიღოთ ინფორმირებული თანხმობა მკურნალობაზე. |
 |
9.3 5.3 პერსონალი და ტრენინგი |
▲back to top |
ჯანდაცვის პერსონალის დახმარებისა და სწავლებისათვის საჭიროა მუდმივი ძალისხმევა და განსაკუთრებული ყურადღება, რაც კომპეტენტური სამუშაო ძალის შექმნას და შენარჩუნებას განაპირობებს. ტრენინგი, სულ მცირე, უნდა მოიცავდეს ოპიოიდური დამოკიდებულების თავისებურებებს, შეფასებას და დიაგნოზს, ფარმაკოლოგიურ და ფსიქოსოციალურ მკურნალობას, ინტოქსიკაციის, ზედოზირებისა და რთული ქცევების მართვას.
რეკომენდაცია (მინიმალური სტანდარტი) ოპიოიდური დამოკიდებულების მკურნალობა უნდა ჩაატაროს სამედიცინო პერსონალმა, რომელსაც გავლილი აქვს სათანადო სწავლება. ტრენინგის დონე უნდა განისაზღვროს სპეციფიკური ფუნქციების შესასრულებლად პასუხისმგებლობის დონით და ქვეყანაში მოქმედი რეგულაციებით. რეკომენდაცია (საუკეთესო პრაქტიკა) ჯანდაცვის სისტემის ხელმძღვანელებმა უნდა უზრუნველყონ მკურნალი პერსონალის შესაბამისი უნარი და კვალიფიკაცია კონტროლს დაქვემდებარებული ნივთიერებების სათანადოდ გამოსაყენებლად. ეს მოთხოვნა შეიძლება მოიცავდეს უწყვეტ განათლებას დიპლომის აღების შემდეგ, სერტიფიცირებას, ლიცენზირებას და თანხების გამოყოფას მონიტორინგისა და შეფასებისთვის. |
 |
9.3.1 5.3.1 სამედიცინო პერსონალი |
▲back to top |
პროგრამების უმრავლესობაში ოპიოიდური დამოკიდებულების სამკურნალოდ საჭიროა საექიმო პერსონალი როგორც კლინიკური შეფასების, ისე ფარმაკოთერაპიის დანიშვნისათვის. ზოგიერთ მათგანში ექიმთა სიმცირის გამო, ეს პასუხისმგებლობები შეიძლება დაეკისროს ექთანს ან სხვა სამედიცინო პერსონალს (ადგილობრივი ინსტრუქციების შესაბამისად).
სპეციალიზირებულ კლინიკებში სამედიცინო პერსონალს ზედამხედველობას უნდა უწევდეს ექიმი, შესაძლოა ფსიქიატრი, რომელიც სპეციალიზირებულია ნივთიერებებზე დამოკიდებულების მკურნალობაში. ზოგჯერ პოლიციამ შესაძლოა მოითხოვოს სამედიცინო ჩანაწერების ნახვა. ამის გაკეთება არ შეიძლება პაციენტის თანხმობის გარეშე, გარდა იმ შემთხვევებისა, რასაც ითვალისწინებს შესაბამისი საკანონმდებლო მოთხოვნები და პროცედურები.
ფართო პროფილის დაწესებულებებში ზოგადი პრაქტიკის ექიმებს და სხვა სამედიცინო პერსონალს გავლილი უნდა ჰქონდეთ საბაზისო სწავლება ოპიოიდური დამოკიდებულების დიაგნოსტიკასა და მკურნალობაში. ვინაიდან მეთადონს და ბუპრენორფინს, არასწორად დანიშვნის შემთხვევაში, პაციენტისათვის ზიანის მიყენება შეუძლია, ბევრ ქვეყანაში არსებობს სამედიცინო პერსონალის ლიცენზირების სისტემა, რომელიც ექიმს უფლებას აძლევს, დანიშნოს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა. ტრენინგის პროგრამებში გათვალისწინებული უნდა იყოს ადგილობრივი კლინიკური მეთოდები და ინსტრუქციები.
საჭიროა, არსებობდეს ნარკომანიის სფეროში მომუშავე სამედიცინო პერსონალის კლინიკური ზედამხედველობის სისტემა, რაც შეიძლება განხორციელდეს კოლეგების, უფროსი კოლეგების ან პროფესიონალი ხელმძღვანელების მიერ. ეს დაგვეხმარება, თავიდან ავიცილოთ პრეპარატების არასათანადო გამოწერა და უზრუნველვყოთ სამედიცინო პერსონალის პროფესიონალიზმი პაციენტებთან ურთიერთობისას.
 |
9.3.2 5.3.2 აფთიაქის პერსონალი |
▲back to top |
მეთადონის და ბუპრენორფინის მიმწოდებელი პერსონალი ძირითადად აფთიაქის თანამშრომლები არიან, თუმცა, წამალი ექიმმა და ექთანმაც შეიძლება გასცეს (ქვეყანაში მოქმედი კანონების მიხედვით). პერსონალს, რომელიც გასცემს მეთადონს და ბუპრენორფინს, გავლილი უნდა ჰქონდეს სწავლება ოპიოიდური დამოკიდებულების მკურნალობის შესახებ. ტრენინგი უნდა მოიცავდეს ოპიოიდური დამოკიდებულების ბუნებას, მკურნალობის მიზნებს, თერაპიულ შედეგს, ოპიოიდური აღკვეთის მდგომარეობის და ინტოქსიკაციის ამოცნობას და რეაგირებას პაციენტის რთულ ქცევაზე. ასევე ტრენინგი უნდა ეხებოდეს კონტროლირებადი პრეპარატების სათანადო შენახვას და მედიკამენტების არადანიშნულებისამებრ მოხმარების თავიდან აცილების მეთოდებს.
 |
9.3.3 5.3.3 ფსიქოსოციალური დახმარების აღმომჩენი პერსონალი |
▲back to top |
პროფესიონალიზმის და მომსახურების სტანდარტიზაციის უზრუნველსაყოფად რეკომენდებულია საბაზისო სწავლება წამალდამოკიდებულების მკურნალობის შესახებ. შემდგომი სწავლების აუცილებლობა დამოკიდებულია პაციენტისათვის შეთავაზებულ ფსიქოსოციალური ჩარევის ბუნებაზე. სასურველია არსებობდეს პერსონალზე ზედამხედველობის სისტემა, ადეკვატური დახმარება და სტანდარტიზებული სამოქმედო ინსტრუქციები ინტოქსიკაციის მკურნალობის, რთული ქცევის და სხვა გადაუდებელი მდგომარეობების მართვისას.
 |
9.4 5.4 კლინიკური ჩანაწერები |
▲back to top |
ყოველი კონტაქტი სამედიცინო სამსახურსა და პაციენტს შორის დაფიქსირებული უნდა იყოს სამედიცინო ჩანაწერებში. ჩანაწერები უნდა იყოს განახლებული და იკითხებოდეს ადვილად. თითოეული ჩანაწერი უნდა იყოს ხელმოწერილი და დათარიღებული.
ზოგიერთ შემთხვევაში, პროფესიული სტანდარტები კონფიდენციალურობის დარღვევას მოითხოვს, მაგ., თუ რისკის ქვეშ არის ბავშვის უსაფრთხოება. ამგვარ სიტუაციებში პროფესიულმა პერსონალმა უნდა აწონ-დაწონოს პაციენტის უფლება მისი კონფიდენციალურობის დაცვაზე და ადამიანის დაცვის პროფესიული მოვალეობა და თუ მაინც ვერ იღებს გადაწყვეტილებას, რჩევა პროფესიულ ორგანოს უნდა დაეკითხოს. როგორც წესი, კონფიდენციალურობის დარღვევა ამგვარ პირობებში კანონით დაშვებულია; უფრო მეტიც, ზოგიერთ შემთხვევაში ეს კანონის მოთხოვნაც არის.
როგორც წესი, პაციენტებისთვის ხელმისაწვდომი უნდა იყოს თავისი სამედიცინო ჩანაწერები. იმ შემთხვევაში, თუ პაციენტის ინტერესებში არ არის საკუთარი ჩანაწერების ნახვა, ეს წესი იზღუდება.
თუ ქვეყანაში არსებობს იდენტიფიკაციის სისტემები, როგორებიცაა: საიდენტიფიკაციო მოწმობები, საბანკო ან სოციალური დაზღვევის ბარათები, საჭიროების შემთხვევაში ისინი პაციენტების იდენტიფიკაციისათვის უნდა გამოვიყენოთ. ამგვარი სისტემის არარსებობისას, მათ, ვინც მკურნალობას ატარებს, უნდა მონახონ ალტერნატიული გზები პაციენტის იდენტიფიკაციისათვის. ამის ძირითადი მიზანი არის ოპიოიდების პოტენციურად ლეტალური დოზების შეცდომით სხვა პაციენტზე გაცემის თავიდან აცილება. თუ ცენტრალური რეგისტრაციის სისტემა არსებობს (ნაწილი 4.2), მისი ეფექტიანობისათვის საჭიროა მონაწილეთა ზუსტი იდენტიფიკაცია.
რეკომენდაცია (მინიმალური სტანდარტი) ყველა პაციენტზე უნდა იწარმოებოდეს სამედიცინო ჩანაწერები, რომლებიც, სულ ცოტა, უნდა მოიცავდეს ანამნეზს, კლინიკურ გამოკვლევას, დიაგნოსტიკურ გამოკვლევებს, დიაგნოზს, ჯანმრთელობის და სოციალურ სტატუსს, მკურნალობის გეგმებს და მათ ცვლილებებს, ინფორმაციას თანხმობის შესახებ, დანიშნულ მედიკამენტებს და სხვა ჩარევებს. |
რეკომენდაცია (მინიმალური სტანდარტი) საჭიროა პაციენტის სამედიცინო ჩანაწერების კონფიდენციალურობის დაცვა. რეკომენდაცია (მინიმალური სტანდარტი) ქვეყანაში მოქმედი რეგულაციების თანახმად, ინდივიდუალური პაციენტის მკურნალობაში ჩართული სამედიცინო პერსონალისთვის, ასევე თვით პაციენტისთვისაც, ხელმისაწვდომი უნდა იყოს პაციენტის სამედიცინო მონაცემები. რეკომენდაცია (მინიმალური სტანდარტი) ჯანდაცვის მუშაკებმა ან მკურნალობაში ჩართულმა სხვა პერსონალმა ინფორმაცია პაციენტის შესახებ მისი თანხმობის გარეშე არ უნდა მიაწოდონ (თუ კანონი არ მოითხოვს) პოლიციას და სხვა სამართალდამცავ სტრუქტურებს. რეკომენდაცია (მინიმალური სტან არტი) სამედიცინო პერსონალს უნდა შეეძლოს ოპიოიდური აგონისტებით მკურნალობაში ჩართული პაციენტების იდენტიფიკაცია. |
 |
9.5 5.5 სამედიცინო უსაფრთხოება |
▲back to top |
ქვეყნების უმრავლესობაში არსებობს საკანონმდებლო წესები, რომლებიც განსაზღვრავს მედიკამენტების შეძენას, შენახვას, გაცემას და დოზირებას; ამ წესებში ხშირად შეტანილია სპეციალური პირობები ოპიოიდების და სხვა ნარკოტიკული ნივთიერებებისთვის. საკანონმდებლო წესები, ჩვეულებრივ, გულისხმობს მეთადონის და ბუპრენორფინის ჩაკეტილ ადგილზე შენახვას; პრეპარატების გაცემა/მიღება უნდა ხდებოდეს ორი თანამშრომლის თანდასწრებით. ამგვარი ზომები ამცირებს პრეპარატის მოპარვის საფრთხეს, განსაკუთრებით, პერსონალის მიერ მისი არადანიშნულებისამებრ გაცემის რისკს.
მეთადონი და ბუპრენორფინი შეიძლება სასიკვდილო იყოს, თუ დოზა არასწორია ან შეცდომით სხვა პაციენტზე გაიცა. შესაძლებელია სხვადასხვა სისტემით სარგებლობა შესაბამის პაციენტზე სწორი დოზის გაცემის უზრუნველსაყოფად. ამგვარი სისტემები აუცილებლად მოიცავს პაციენტის იდენტურობის და რეცეპტის სისწორის შემოწმებას. სისტემა შეიძლება არ მოითხოვდეს მაღალ ტექნოლოგიებს (მაგ., გაცემის ადგილზე არის პაციენტის ფოტო და დოზის მიღებას პაციენტი ხელმოწერით ადასტურებს). არსებობს მაღალტექნოლოგიური სისტემებიც (კომერციული სისტემები, რომლებშიც ბადურის სკანირების მონაცემები დაკავშირებულია მეთადონის ტუმბოსთან).
რეკომენდაცია (მინიმალური სტანდარტი) საჭიროა დოკუმენტირების პროცესების დაწესება მედიკამენტების, განსაკუთრებით, მეთადონის და ბუპრენორფინის უსაფრთხო და კანონიერი მოწოდების, შენახვის, გაცემისა და დოზირების უზრუნველსაყოფად. |
 |
9.6 5.6 მკურნალობის პირობები |
▲back to top |
 |
9.6.1 5.6.1 კლინიკური ინსტრუქციები |
▲back to top |
კლინიკური ინსტრუქციები მკურნალობის ხარისხის გასაუმჯობესებელი ერთ-ერთი მექანიზმია. არსებობს ოპიოიდური დამოკიდებულების მკურნალობის მკაფიო, მტკიცებულებებზე დაფუძნებული ინსტრუქციები და საჭიროა, რომ სულ მცირე, ეს მასალა ხელმისაწვდომი იყოს სამედიცინო პერსონალისთვის. იდეალური იქნება, თუ ქვეყანაში ან რეგიონულ დონეზე შემუშავდება ადგილობრივი ინსტრუქციები ადგილობრივი კანონების, პოლიტიკისა და პირობების გათვალისწინებით. ეს ინსტრუქციები განსხვავებული იქნება მეთადონსა და ბუპრენორფინზე ზედამხედველობის ღირებულების და მოთხოვნების მიხედვით. ადგილობრივ ინსტრუქციებში წარმოდგენილი უნდა იყოს მკურნალობის მიღებული სტანდარტი კონკრეტულ ადგილას, რომელიც გარკვეულწილად ასახავს საზოგადოების და მისი პროფესიული ნაწილის ფასეულობებს და წეს-ჩვეულებებს.
რეკომენდაცია (მინიმალური სტანდარტი) კლინიკის პერსონალისთვის ხელმისაწვდომი უნდა იყოს კლინიკური ინსტრუქციები ოპიოიდური დამოკიდებულების მკურნალობისთვის. რეკომენდაცია (საუკეთესო პრაქტიკა) კლინიკური ინსტრუქციები უნდა იყოს დეტალური, გასაგებად გადმოცემული, მტკიცებულებებზე დაფუძნებული და შემუშავებული ცენტრალურ ან უფრო დაბალ დონეზე, რათა მათში ასახული იყოს ადგილობრივი კანონები, პოლიტიკა და პირობები. |
 |
9.6.2 5.6.2 მკურნალობის პრინციპები |
▲back to top |
საჭიროა, შემუშავდეს მიზნების, ჩვენებების, პროგრამების, დოზირების სქემების და მკურნალობის წესების (მათ შორის, მკურნალობის შეწყვეტის მიზეზები) პოლიტიკა და მოხდეს მისი ნათლად გაცნობა მშობლებისა და პერსონალისთვის. ეს ეხება ოპიოიდური დამოკიდებულების მკურნალობას ოპიოიდური დეტოქსიკაციით, ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას და ნალტრექსონით მკურნალობას.
სასურველია (თუ შესაძლებელია) შემუშავდეს კავშირი სამედიცინო, ფსიქიატრიულ, სოციალურ და ზიანის შემცირების სამსახურებს შორის; თუმცა, ფსიქოსოციალური დახმარება, მათ შორის, კონსულტაციები, შეიძლება ადგილზე არ იყოს ხელმისაწვდომი.
მამაკაცების და ქალების მკურნალობა შეიძლება ერთი და იმავე დაწესებულებაში იმ პირობით, თუ ეს მოცემული კულტურისთვის მისაღებია და სქესისთვის სპეციფიკური საკითხები მოგვარებულია.
რეკომენდაცია (მინიმალური სტანდარტი) აგონისტებით მხარდამჭერი მკურნალობის პროგრამების, უსაფრთხოების და ეფექტიანობის მაქსიმალურად გაზრდისთვის, რეგულაციებმა ხელი უნდა შეუწყოს დოზირების მოქნილ სტრუქტურას, დაბალი დოზით დაწყებას და მაღალ შემანარჩუნებელ დოზებს; დოზის სიდიდეზე და მკურნალობის ხანგრძლივობაზე შეზღუდვები არ უნდა იყოს. რეკომენდაცია (საუკეთესო პრაქტიკა) ოპიოიდების აღკვეთის მდგომარეობის მართვა ისე უნდა იყოს დაგეგმილი, რომ აღკვეთის მკურნალობა იყოს არა ცალკე მდგომი მომსახურება, არამედ ინტეგრირებული მკურნალობის სხვა ვარიანტებთან. რეკომენდაცია (საუკეთესო პრაქტიკა) სახლში დოზების გატანების რეკომენდირება შესაძლებელია, როცა დოზა და სოციალური სიტუაცია სტაბილურია, და როცა უკანონო მიზნებისთვის მედიკამენტის გამოყენების რისკი დაბალია. რეკომენდაცია (საუკეთესო პრაქტიკა) მკურნალობის კურსიდან არანებაყოფლობითი გარიცხვა გამართლებულია პერსონალის და სხვა პაციენტების უსაფრთხოების უზრუნველსაყოფად, მაგრამ მხოლოდ პროგრამის წესების შეუსრულებლობა არ უნდა გახდეს მკურნალობიდან არანებაყოფლობითი გარიცხვის მიზეზი. გარიცხვამდე, საჭიროა სათანადო ზომები მივიღოთ სიტუაციის გასაუმჯობესებლად, მათ შორის, მკურნალობის გამოყენებული მეთოდის ხელახალი შეფასება. |
 |
9.6.3 5.6.3 არანებაყოფლობითი გარიცხვა |
▲back to top |
მკურნალობიდან და ქცევის დასაშვები ფარგლების დადგენის სხვა ფორმები სამკურნალო სამსახურის ერთ-ერთი უპირველესი პასუხისმგებლობაა პერსონალის და პაციენტების დაცვა ზიანისგან. სიტუაციაში, როდესაც პაციენტის ადრინდელი საქციელი მიუთითებს სხვა პაციენტების და პერსონალის დაზიანების მნიშვნელოვან რისკზე, სამკურნალო სამსახურმა უნდა მიიღოს ზომები ამ რისკის შესამცირებლად, რასაც შესაძლოა პაციენტის მკურნალობის კურსიდან გარიცხვაც მოჰყვეს. პოტენციურად, ამგვარი სიტუაციის თავიდან აცილება შესაძლებელია, თუ ადრეულ სტადიაში მოხდება პაციენტის ქცევის იდენტიფიცირება და მიიღება სათანადო ზომები. მკურნალობის ეფექტიანი სერვისი მკვეთრ ზღვარს უნდა აწესებდეს მისაღებ და მიუღებელ ქცევას შორის და ეს ზღვარი ყველა პაციენტისთვის დაცულ უნდა იქნეს მუდმივად და გამჭვირვალედ (სიტუაციას ზოგჯერ მოიხსენიებენ, როგორც „ლიმიტების დაწესება“). იმისათვის, რომ არ განმეორდეს საზოგადოების პაციენტისადმი დამოკიდებულება და პაციენტი არ გაირიყოს, საჭიროა ზღვრის დაწესებასთან დაკავშირებული რეაქციის განსაზღვრა:
დადებითი რეაქცია „კარგი“ საქციელისთვის;
მოზომილი რეაქცია მიღებული ქცევის მცირე დარღვევებისთვის (მაგ., გაფრთხილება, სახლში მისაღები დოზების პრივილეგიის შემცირება, უფრო ხშირი ვიზიტი ექიმთან, უარი ინტოქსიკაციისას დოზის გაცემაზე ან გადავადება);
საბოლოო რეაქცია (მაგ., მკურნალობიდან გარიცხვა და, თუ საჭიროა, პოლიციის გამოძახება) მიღებული ქცევის ნორმების მნიშვნელოვანი დარღვევისთვის.
გადაჭარბებული ზომების მიღება წესების მცირე დარღვევისთვის მკურნალობის კურსიდან ბევრი პაციენტის გარიცხვას გამოიწვევს, მაშინ, როდესაც მათ შეეძლოთ მკურნალობის გაგრძელება და ამით სარგებლის მიღება. ამავდროულად, მნიშვნელოვან დარღვევებზე სათანადო რეაგირების არქონამ შეიძლება ზიანი მიაყენოს პაციენტებს და პერსონალს და ეს არ იქნება დახმარება მოცემული წესების დამრღვევი პაციენტისთვის.
თითოეულმა სამსახურმა თავად უნდა განსაზღვროს წესები და საზღვრები; ეს დამოკიდებულია კულტურულ ნორმებზე, მკურნალობის მიზნებზე და იმ პოლიტიკურ გარემოზე, რომელიც იძლევა მკურნალობის გაგრძელების საშუალებას.
მკურნალობის წესები ძალიან განსხვავებული იქნება ოპიოიდების აღკვეთის მდგომარეობის მკურნალობაზე მომუშავე დაწესებულებაში (სადაც მიზანი არის ოპიოიდის სრული მოხსნა) და ოპიოიდური აგონისტებით მხარდამჭერ თერაპიაზე მომუშავე დაწესებულებაში (რომლის მიზანია ოპიოიდურ დამოკიდებულებასთან დაკავშირებული სიკვდილიანობის და ავადობის შემცირება და ცხოვრების ხარისხის გაუმჯობესება).
იმის მიუხედავად, თუ რა საზღვრებია დაწესებული, ისინი მუდმივად უნდა დაიცვას მკურნალმა პერსონალმა. ამ გზით, პაციენტები სწრაფად ისწავლიან და უფრო იოლად მიიღებენ დასაშვები საქციელის დაწესებულ საზღვრებს. თუ პერსონალი ამ საზღვრებს სხვადასხვაგვარად აწესებს, ზოგი პაციენტი შეეცდება მათ შეცვლას. ასეთი ე.წ. „გახლეჩა“ იწვევს მკურნალ პერსონალთან დაპირისპირებას, რაც ცუდ შედეგს გვაძლევს პაციენტებში.
მაშინაც კი, როცა ინციდენტი საკმარისად სერიოზულია და მკურნალობის კურსიდან დაუყოვნებლივ გარიცხვას მოითხოვს, დაწესებულებამ უნდა განიხილოს ეს შემთხვევა და განსაზღვროს, გაკეთდა თუ არა ყველაფერი ამგვარი ქცევის გამოწვევის ან დაშვების თავიდან ასაცილებლად. სამკურნალო სამსახურს უნდა ჰქონდეს ინციდენტების შეტყობინების მექანიზმი, მათ შორის „დოზის გამოტოვება“ და მოულოდნელი უარყოფითი შედეგი. ანგარიშები რეგულარულად უნდა განიხილოს ჯგუფმა, რომელშიც შედის სამსახურის კლინიკურ მართვაზე პასუხისმგებელი პირი.
ინიციატივები ამგვარი ქცევის შესამცირებლად შეიძლება მოიცავდეს პერსონალის სწავლებას არაგანსჯად და არაკონფრონტაციულ კომუნიკაციაში; პაციენტისთვის ლოდინის დროის შემცირებას, მისი მკურნალობის ხშირად გადახედვას, ოჯახის და სამუშაო ატმოსფეროს გამოყენებას, დაცვის სამსახურის არსებობას.
თუ პერსონალის და სხვა პაციენტების უსაფრთხოების უზრუნველყოფის მიზნით სიტუაცია არ მოითხოვს დაუყოვნებლივ გარიცხვას მკურნალობის კურსიდან, უნდა ვცადოთ, რომ სიტუაცია გარიცხვის გარეშე განიმუხტოს, განსაკუთრებით, თუ დასჯის ეს ზომა გამორიცხავს მკურნალობის გაგრძელებას. პაციენტს უნდა ესმოდეს, რას მოითხოვენ მისგან, ნათლად უნდა იყოს გარკვეული, როგორი საქციელია მიუღებელი და რას ნიშნავს დაწესებული ზღვარის დარღვევა. როცა არჩევანი მისაღები არ არის ან ყველა ალტერნატივა ამოწურულია, უნდა ვცადოთ პაციენტის გადაყვანა სხვა სამკურნალო დაწესებულებაში, რადგან შედეგი არანებაყოფლობითი გარიცხვის დროს ყოველთვის ცუდია - ჰეროინის მოხმარების განახლება პაციენტების 75%-ში აღინიშნება.
 |
9.6.4 5.6.4 მკურნალობის ინდივიდუალური გეგმები |
▲back to top |
ინდივიდუალური მკურნალობის პირველი სტადია ამომწურავად აფასებს და განსაზღვრავს სპეციფიკურ ფსიქოსოციალურ მოთხოვნილებებს და პაციენტის მოტივაციას, ადასტურებს ოპიოიდური დამოკიდებულების დიაგნოზს და მკურნალობის მანამდე ჩატარებული კურსების შედეგებს (ნაწილი 6.1). ყოველივე ამაზე დაყრდნობით მუშავდება მკურნალობის ინდივიდუალური კურსი. შეძლებისდაგვარად, კონკრეტული საჭიროებების საპასუხო ჩარევა უნდა ეფუძნებოდეს მტკიცებულებებს, ითვალისწინებდეს ინდივიდუალურ არჩევანს და მკურნალობის წარსულ გამოცდილებას.
ხანგრძლივად მიმდინარე სხვა დაავადებების მსგავსად, მკურნალობის პირველ ეტაპზე პაციენტი არ უნდა განვიხილოთ როგორც „განკურნებული“. დაკვირვების განსახორციელებლად საჭიროა გარკვეული პირობები. მკურნალობის პროგრამებს იმგვარი სტრუქტურა უნდა ჰქონდეთ, რომ ისინი პაციენტს დიდი ხნის განმავლობაში დაეხმარონ.
რეკომენდაცია (მინიმალური სტანდარტი) საჭიროა ჩატარდეს დეტალური ინდივიდუალური შეფასება: ანამნეზი (წარსულში მკურნალობის გამოცდილება; სამედიცინო და ფსიქიატრიული ისტორია; ცხოვრების პირობები; ნასამართლობა; პროფესიული სიტუაცია და დასაქმება; სოციალური და კულტურული ფაქტორები, რომელთაც შეიძლება გავლენა მოახდინონ ნარკოტიკების მოხმარებაზე); კლინიკური გასინჯვა (ინტოქსიკაციის/ აღკვეთის მდგომარეობის შეფასება, ინექციის კვალი) და, თუ საჭიროა, დიაგნოსტიკური კვლევები (როგორებიცაა: შარდის შემოწმება ნარკოტიკზე, აივ-ი, C და B ჰეპატიტები, ტუბერკულოზი, ღვიძლის ფუნქციები). რეკომენდაცია (საუკეთესო პრაქტიკა) საწყისი შეფასების ნაწილი უნდა იყოს შემოწმება ფსიქიატრიულ და სომატურ დაავადებებზე. რეკომენდაცია (საუკეთესო პრაქტიკა) ინდივიდუალურად შერჩეული მკურნალობა უნდა ემყარებოდეს მკურნალობის საჭიროების დეტალურ შეფასებას, მკურნალობის შესაბამისობის განსაზღვრას (შესაბამისობის შეფასება უნდა იყოს მტკიცებებზე დაფუძნებული), პაციენტის თანხმობას და მკურნალობის ხელმისაწვდომობას. რეკომენდაცია (საუკეთესო პრაქტიკა) მკურნალობის გეგმა უნდა იყოს გაწერილი ხანგრძლივი დროის განმავლობაში. რეკომენდაცია (საუკეთესო პრაქტიკა) ოპიოიდური დეტოქსიკაცია უნდა დაიგეგმოს მიმდინარე მკურნალობასთან ერთად. |
 |
9.6.5 5.6.5 მომსახურების დიაპაზონი |
▲back to top |
იმისათვის, რომ მომსახურება პაციენტის მოთხოვნებზე იყოს მორგებული, მას პროგრამამ ამ მომსახურების სრული სპექტრი უნდა შესთავაზოს (მიუხედავად იმისა, რომ ყველა პროგრამა მკუნალობის სხვადასხვა კურსს ითვალისწინებს).
თითოეული სამკურნალო დაწესებულების სამედიცინო პერსონალმა უნდა უზრუნველყოს ნალოქსონის გამოყენება ოპიოიდური ზედოზირების სამკურნალოდ. ამისათვის აუცილებელია პრეპარატის მარაგი და საინექციო მასალა. აღმოჩნდა, რომ მოსახლეობაში ზედოზირებით სიკვდილიანობის შემცირების ერთ-ერთი მეთოდია ოპიოიდების მომხმარებლების და მათი ოჯახებისთვის ნალოქსონის დარიგება და ზედოზირებისას მისი გამოყენების სწავლება [78, 79, 80], ეს კონცეფცია ალერგიული რეაქციების მქონე პაციენტების და მათი ოჯახებისთვის ადრენალინის დარიგების მსგავსია.
რეკომენდაცია (მინიმალური სტანდარტი) ფარმაკოლოგიური მკურნალობის აუცილებელი არჩევანი უნდა მოიცავდეს ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას და ოპიოიდების აღკვეთის მდგომარეობის მართვას. რეკომენდაცია (მინიმალური სტანდარტი) ოპიოიდების დოზის გადაჭარბების სამკურნალოდ ხელმისაწვდომი უნდა იყოს ნალოქსონი. რეკომენდაცია (საუკეთესო პრაქტიკა) ფარმაკოლოგიური მკურნალობა უნდა სთავაზობდეს როგორც მეთადონს, ისე ბუპრენორფინს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობისთვის და ოპიოიდების აღკვეთის მდგომარეობის მართვისთვის; ალფა-2 ადრენერგულ აგონისტებს - ოპიოიდების აღკვეთის მდგომარეობის სამკურნალოდ, ნალტრექსონს - რეციდივის პრევენციისთვის და ნალოქსონს - დოზის გადაჭარბების მკურნალობისთვის. |
 |
9.6.6 5.6.6 თანმხლები დაავადებების მკურნალობა |
▲back to top |
ოპიოიდდამოკიდებული პაციენტებს ხშირად სხვა სომატური და ფსიქიატრიული დაავადებებიც აქვთ, რაც სოციალური პრობლემებით არის დამძიმებული. ოპტიმალური მიდგომა ამ დროს არის ინტეგრირებული სრული მკურნალობის უზრუნველყოფა არსებული პრობლემების მოსაგვარებლად და მომავალი პრობლემების თავიდან ასაცილებლად. პრაქტიკაში, ეს ნიშნავს შეფასების პროცესში სომატური, ფსიქიატრიული და სოციალური პრობლემების გამოვლენას და მათი ერთდროულად და ადგილზევე მოგვარების საშუალებების არსებობას. ეს შეიძლება ნიშნავდეს მრავალგვარი უნარ-ჩვევების მქონე პერსონალს ან სხვადასხვა პროფილის პროფესიონალებთან კოორდინირებულ მუშაობას.
 |
9.6.7 5.6.7 ფსიქოსოციალური და ფსიქიატრიული დახმარება |
▲back to top |
ოპიოიდური დამოკიდებულების მკურნალობა მედიკამენტების ეფექტიანად გამოყენებას გულისხმობს. თუმცა, მედიკამენტების მიცემა ფსიქოსოციალური დახმარების გარეშე ნიშნავს ოპიოიდური დამოკიდებულების კომპლექსური ბუნების არცნობას. იკარგება ოპტიმალური ჩარევის უზრუნველყოფის შესაძლებლობა, კლინიკის პერსონალს კი არ აქვს საშუალება, დააკმაყოფილოს პაციენტის ყველა მოთხოვნილება. მკურნალობა მიზნად უნდა ისახავდეს ყველა პაციენტისთვის ინტეგრირებული, მისაღები ფსიქოსოციალური დახმარების ადგილზე გაწევას. თუ ფსიქოსოციალური დახმარების გაწევა შეუძლებელია, ან თუ პაციენტი უარს ამბობს მასზე, მკურნალობა ეფექტიანი მედიკამენტებით მაინც უნდა ჩატარდეს. სულ მცირე, უნდა იყოს პაციენტის ფსიქოსოციალური საჭიროებების შეფასების და შეძლებისდაგვარი დახმარების გაწევის მცდელობა. დამატებითი დახმარების საჭიროებისას უნდა გააგზავნონ სხვა დაწესებულებებში.
რეკომენდაცია (მინიმალური სტანდარტი) ფსიქოსოციალური დახმარება ხელმისაწვდომი უნდა იყოს ყველა ოპიოიდდამოკიდებული პაციენტისთვის ოპიოიდური დამოკიდებულების ფარმაკოლოგიურ მკურნალობასთან ერთად. სულ მცირე, იგი უნდა მოიცავდეს ფსიქოსოციალური პრობლემების შეფასებას, დამხმარე კონსულტაციებს და კავშირს ოჯახთან და საზოგადოებასთან. რეკომენდაცია (საუკეთესო პრაქტიკა) ხელმისაწვდომი უნდა იყოს სხვადასხვა სახის ფსიქოსოციალური დახმარება პაციენტის საჭიროებების შესაბამისად. ამგვარი დახმარების არასრული სია მოიცავს სხვადასხვა ფორმის კონსულტაციებსა და ფსიქოთერაპიას, დახმარებას სოციალური პრობლემების მოგვარებაში (საცხოვრებელი, დასაქმება, განათლება, კეთილდღეობა და პრობლემები კანონთან).. რეკომენდაცია (საუკეთესო პრაქტიკა) თანმხლები ფსიქიატრიული დაავადებების მქონე პაციენტებისთვის ფსიქოსოციალური და ფსიქიატრიული მკურნალობა უზრუნველყოფილი უნდა იყოს ადგილზე. |
 |
9.6.8 5.6.8 ტუბერკულოზი, ჰეპატიტი და აივ ინფექცია |
▲back to top |
მიუხედავად აივ/შიდსის მქონე ოპიოიდებზე დამოკიდებული პირების დიდი რაოდენობისა, არსებობს დამაჯერებელი მონაცემები, რომ ამ პაციენტებისთვის ნაკლებად ხელმისაწვდომია ანტირეტროვირუსული მედიკამენტები და აივ/შიდსის სხვა მკურნალობა არაწამალდამოკიდებულ პაციენტებთან შედარებით. ოპიოიდების მოხმარება განსაზღვრულია როგორც რეგულარული ანტირეტროვირუსული მკურნალობის ერთ-ერთი ხელისშემშლელი ფაქტორი, რაც იწვევს პრეპარატის მიმართ ვირუსული რეზისტენტობის განვითარების რისკს [81].
მეორე მხრივ, ობსერვაციული კვლევები მიუთითებს, რომ მაღალაქტიური ანტირეტროვირუსული თერაპიის გავლენა CD4-ის რაოდენობაზე პაციენტებში, რომლებიც აგრძელებენ ჰეროინის ან სხვა ნარკოტიკის მოხმარებას, საკმაოდ დიდია და მნიშვნელოვნად არ განსხვავდება არანარკომან პაციენტებში მიღებული შედეგებისგან [82]. შესანიშნავი შედეგების მიღება შეიძლება პაციენტებში, რომლებიც იმყოფებიან ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაზე [83].
იგივე ვრცელდება ტუბერკულოზის და ჰეპატიტის მკურნალობაზე, იმ განსხვავებით, რომ კლინიკებში, სადაც არიან ტუბერკულოზით დაავადებული პაციენტები, გათვალისწინებულ უნდა იქნეს ტუბერკულოზის სხვა პაციენტებზე გავრცელების რისკი, განსაკუთრებით იმუნოკომპრომეტირებული პაციენტების ტუბერკულოზით დაავადებულ პაციენტებთან კონტაქტის დროს. გადატვირთულ კლინიკებში ტუბერკულოზის გავრცელების რისკის გათვალისწინებით, ოპიოიდებზე დამოკიდებულების მკურნალობის დროს ამ საკითხს ყურადღება უნდა მიექცეს ტუბერკულოზის ადგილობრივ ექსპერტებთან კონსულტაციებით. საჭიროა ოთახის განიავება, კლინიკის პაციენტებით გადატვირთვის თავიდან აცილება და ხველების მქონე პაციენტების მკურნალობა.
C ჰეპატიტის და ოპიოიდური დამოკიდებულების კომბინირებული მკურნალობა ოპიოიდური აგონისტების მხარდაჭერით და ანტივირუსული პრეპარატებით შეიძლება ძალიან შედეგიანი იყოს [84, 85, 86, 87].
მრავალმა რანდომიზებულმა კონტროლირებულმა კვლევამ აჩვენა, რომ წამალდამოკიდებული პაციენტები უფრო დიდი ალბათობით იტარებენ სხვა დაავადების მკურნალობას, თუ იგი ადგილზე ხორციელდება; ამის მიღწევა მინიმალური დამატებითი დანახარჯებით არის შესაძლებელი [88, 89, 90, 91, 92, 93]. შეიძლება ასევე გამოვიყენოთ ალტერნატიული მიდგომა - ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა სამედიცინო კლინიკებში [94].
რეგულარული მკურნალობის უზრუნველსაყოფად საჭიროა აივ-ის და ტუბერკულოზის ზედამხედველობით მკურნალობა ინტეგრირებული იყოს ოპიოიდური აგონისტებით ჩანაცვლებით მკურნალობასთან და ჩატარდეს ერთსა და იმავე ადგილას.
ამგვარი ინტეგრირებული მკურნალობის სხვადასხვა მოდელი არსებობს:
თანმხლები დაავადებების მკურნალობა შეიძლება ჩაირთოს ოპიოიდებზე დამოკიდებულების მკურნალობის არსებულ პროგრამებში [84].
ამ თანმხლები დაავადებების პროგრამებმა შეიძლება შეითავსონ ოპიოიდური დამოკიდებულების მკურნალობა [85].
შესაძლოა შეიქმნას ახალი სპეციალიზებული მომსახურება ნარკოტიკების მომხმარებლებისთვის, სადაც უმკურნალებენ ოპიოიდურ დამოკიდებულებას, ტუბერკულოზს, აივ-ს და ჰეპატიტს.
ოპიოიდური დამოკიდებულების და აივ/ტუბერკულოზის მკურნალობა შეიძლება ჩატარდეს პირველადი ჯანდაცვის დაწესებულებებში [87].
ოპიოიდური დამოკიდებულების მკურნალობა კომბინირებული უნდა იყოს ტუბერკულოზის, აივ-ის და ჰეპატიტის მკურნალობასთან ადგილობრივი პირობების გათვალისწინებით. ამისათვის ყველაზე მარტივი გზაა, რომ სამედიცინო პერსონალი მზად იყოს ხვადასხვა დაავადების მკუნალობისათვის. რადგან ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის კურსში ჩართული პაციენტები ისედაც ყოველდღე დადიან დისპანსერში, აივ-ის მკურნალობასთან ინტეგრირება ქმნის ეფექტიან მექანიზმს აივ-ის მკურნალობაზე პირდაპირი დაკვირვებისთვის, რაც მკურნალობის გაგრძელების მეტ გარანტიას იძლევა. თუ ინტეგრირებული მკურნალობა შესაძლებელი არ არის, უნდა დამყარდეს კავშირი წამალდამოკიდებულების მკურნალობის სამსახურსა და აივ-ის, ტუბერკულოზის და ჰეპატიტების მკურნალობის სამსახურებს შორის, რათა გაიზარდოს მიმართვები ამ სამსახურებისადმი და წარმატებული მკურნალობის ალბათობა.
აქტიური ტუბერკულოზი ხასიათდება გადადების მაღალი საფრთხით, ამიტომ დაავადებული პაციენტები მკურნალობის ადრეულ სტადიაზე, განსაკუთრებით ანტიტუბერკულოზური მკურნალობის პირველი ორი კვირის განმავლობაში, რაც შეიძლება იზოლირებულნი უნდა იყვნენ სხვა პაციენტებისგან.
ნარკოტიკის ყველა ინექციური მომხმარებლისთვის ხელმისაწვდომი უნდა იყოს აივ-ის გავრცელების შემცირების ზომები, მათ შორის, სუფთა საინექციო აღჭურვილობა, პრეზერვატივები, ანტირეტროვირუსული და სხვა მკურნალობა, ფსიქოსოციალური დახმარება და თანმხლები დაავადებების მკურნალობა. მართალია, პაციენტებში, რომელთაც მკურნალობის დაწყებამდე შეწყვიტეს ჰეროინის მოხმარება, უფრო მაღალია ანტირეტროვირუსული მკურნალობის კურსის რეგულარულად ჩატარების მაჩვენებელი, პაციენტები, რომელთაც არ შეუწყვეტიათ ნარკოტიკის მოხმარება, ასევე ემორჩილებიან მკურნალობას. ამიტომ, პაციენტებს, რომელთაც ანტირეტროვირუსული მკურნალობა სჭირდებათ, მკურნალობის დაწყებამდე უალტერნატივოდ არ უნდა მოეთხოვოთ ნარკოტიკების მოხმარების შეწყვეტა.
რეკომენდაცია (მინიმალური სტანდარტი) საჭიროა თანამშრომლობა აივ-ის, ჰეპატიტის და ტუბერკულოზის სამკურნალო დაწესებულებებთან (თუ ისინი არსებობს). რეკომენდაცია (საუკეთესო პრაქტიკა) თუ დიდია იმ პაციენტების რაოდენობა, რომლებსაც ოპიოიდური დამოკიდებულების მკურნალობასთან ერთად ესაჭიროებათ აივ-ის, ჰეპატიტის ან ტუბერკულოზის მკურნალობა, ოპიოიდური და მოკიდებულების მკურნალობა ინტეგრირებული უნდა იყოს ამ თანმხლები დაავადებების მკურნალობასთან. რეკომენდაცია (საუკეთესო პრაქტიკა) ოპიოიდებზე დამოკიდებულ პაციენტებს, რომელთაც აქვთ ტუბერკულოზი, ჰეპატიტი, ან აივ ინფექცია, ოპიოიდური აგონისტები უნდა დაენიშნოთ სხვა დაავადებების მკურნალობასთან ერთად; არ არის საჭირო, დაველოდოთ ოპიოიდების მიღების შეწყვეტას იმისათვის, რომ დავიწყოთ ანტიტუბერკულოზური, ჰეპატიტის ან ანტირეტროვირუსული მკურნალობა. რეკომენდაცია (საუკეთესო პრაქტიკა) ტუბერკულოზით, ჰეპატიტით ან აივ ინფექციით დაავადებული ოპიოიდებზე დამოკიდებული პაციენტებისთვის ისეთივე ხელმისაწვდომი უნდა იყოს ამ დაავადებებზე მკურნალობა, როგორც ოპიოიდური დამოკიდებულების მკურნალობა. |
 |
9.6.9 5.6.9 B ჰეპატიტის საწინააღმდეგო ვაქცინაცია |
▲back to top |
B ჰეპატიტის საწინააღმდეგო ვაქცინაცია რეკომენდებულია ოპიოიდებზე დამოკიდებული ყველა პაციენტისთვის [95]. იდეალურ შემთხვევაში B ჰეპატიტის საწინააღმდეგო ვაქცინაცია უნდა გაკეთდეს სამ ეტაპად, სულ ცოტა, ოთხი კვირის ინტერვალით. ვირუსისგან საკმაოდ ძლიერი დაცვის უზრუნველყოფა შესაძლებელია ვაქცინაციის სხვა ცხრილითაც. მკურნალობის ყველა სამსახურს შეუძლია ჰქონდეს ღირებულებაზე და სეროლოგიურ ტესტირებაზე დამყარებული ვაქცინაციის საკუთარი პრინციპი. ვაქცინისთვის საჭიროა ცივი ჯაჭვის უზრუნველყოფა. უნდა გავითვალისწინოთ B ჰეპატიტის გავრცელება და პაციენტების რევაქცინაციაზე დაბრუნების ალბათობა. პაციენტების რევაქცინაციაზე მოყვანის სირთულის და ვაქცინის შედარებით იაფი ფასის გამო, ხარჯების მხრივ საუკეთესო გამოსავალია პაციენტის ვაქცინაცია წინასწარი სეროლოგიური ტესტირების გარეშე, მაშინაც კი, თუ კურსის დასრულება გარანტირებული არ არის. ზოგიერთმა კვლევამ აჩვენა, რომ უფასო ვაქცინაცია, პერსონალის სწავლება, ანაზღაურება, ადგილზე ვაქცინაცია და დაჩქარებული ცხრილი ხელს უწყობს მოსახლეობაში ვაქცინაციის მაჩვენებლის ზრდას [96, 97, 98].
მეორე მხრივ, კარგი იქნება, თუ განისაზღვრება B ჰეპატიტის საწინააღმდეგო პოსტვაქცინური ანტისხეულები, რადგან ადამიანების საკმაოდ დიდ რაოდენობას ადეკვატური იმუნური პასუხი არ უვითარდება [99, 100, 101]; ამგვარ შემთხვევაში უნდა გაკეთდეს ვაქცინაციის დამატებითი დოზები.
ბევრი ოპიოიდდამოკიდებული პაციენტისთვის მიზანშეწონილია A ჰეპატიტის საწინააღმდეგო ვაქცინაცია [102].
რეკომენდაცია (საუკეთესო პრაქტიკა) მკურნალობის სამსახურმა ოპიოიდებზე დამოკიდებულ ყველა პაციენტს უნდა შესთავაზოს B ჰეპატიტის საწინააღმდეგო ვაქცინაცია. |
 |
9.7 5.7 მკურნალობის შეფასება |
▲back to top |
ოპიოიდური აგონისტებით მხარდამჭერ პროგრამებში მკურნალობის მინიმალური სტანდარტის უზრუნველსაყოფად საჭიროა დაკვირვება არასათანადო გამოყენებასთან დაკავშირებულ პოტენციურ ზიანზე, ზედოზირებაზე და სხვა გვერდით ეფექტებზე. მარტივი შეფასების მეთოდი, რომელიც შეიძლება გამოყენებულ იქნეს პრეპარატების არასათანადო მიზნით გამოყენების აღმოსაჩენად, არის მაგ., ინფორმაციის შეგროვება მედიკამენტის არასათანადო მოხმარების შესახებ.
მკურნალობის დროს გვერდითი მოვლენების აღმოჩენის და დაფიქსირების სისტემა (რომელსაც მოჰყვება რეგულარული განხილვა და სათანადო ზომების მიღება), უსაფრთხოების უზრუნველყოფაში დაგვეხმარება. ამ მხრივ მნიშვნელოვანია იმ პაციენტებზე დაკვირვება, რომლებიც მკურნალობას ტოვებენ.
მკურნალობის ოპტიმალური შეფასების დროს განისაზღვრება მისი უსაფრთხოება, ეფექტიანობა და მიმდინარეობა. ეფექტიანობა შეიძლება შეფასდეს ადგილზე, გამოსავლის შესაფასებელი ცვლადების რუტინულად შეგროვებით და მკურნალობის კურსიდან გასულ პაციენტებზე დაკვირვებით; ან გარეთ, გარეშეფასების ჯგუფის ან ერთი სპეციალისტის მიერ.
შეფასების შესახებ დამატებითი დეტალები შეგიძლიათ ნახოთ ჯანმო-ის მასალებში ოპიოიდური მხარდამჭერი თერაპიის პროგრამების შეფასების შესახებ [103].
რეკომენდაცია (მინიმალური სტანდარტი) საჭიროა არსებობდეს მკურნალობის უსაფრთხოების მონიტორინგის სისტემა, რომელიც მოიცავს მედიკამენტის არასათანადო მოხმარების სიხშირის განსაზღვრას. რეკომენდაცია (საუკეთესო პრაქტიკა) საჭიროა ჩატარებული მკურნალობის პროცესის და შედეგების პერიოდული ან მიმდინარე შეფასება. |
 |
10 6. სახელმძღვანელო კლინიცისტებისთვის |
▲back to top |
ბოლო წლებში გაიზარდა მკურნალობის არჩევანი ოპიოიდური დამოკიდებულების მქონე პაციენტებისთვის. მართალია, ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა (მეთადონი და ბუპრენორფინი) სულ უფრო მეტად მიიჩნევა მკურნალობის ყველაზე ეფექტიან სტრატეგიად, განიხილება სხვა ვარიანტებიც: ოპიოიდების აღკვეთა და რეციდივის პრევენცია. მკურნალობისას ყველა პაციენტისათვის შესაბამისი მეთოდი უნდა შეირჩეს. ბევრი პაციენტი მკურნალობის სხვადასხვა მეთოდის რამდენიმე ეპიზოდს გაივლის, ვიდრე მკურნალობის მისთვის შესაბამის მეთოდს მიაგნებს. არჩევანი მკურნალობის მეთოდებს შორის კლინიცისტმა და პაციენტმა ერთად უნდა გააკეთონ; მხედველობაში უნდა იქნეს მიღებული პაციენტის არჩევანი, სამედიცინო ეთიკა, მონაცემები მკურნალობის ეფექტიანობის შესახებ და ინდივიდუალური ფაქტორები, როგორიცაა წარსულში მკურნალობის ისტორია.
ამ ნაწილში განხილულია მკურნალობის სამი სხვადასხვა მეთოდი:
ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა;
ოპიოიდების აღკვეთა;
ოპიოიდების აღკვეთა და პერორალური ნალტრექსონის დანიშვნა.
ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობისას უნდა გავითვალისწინოთ შემდეგი:
მეთადონის და ბუპრენორფინის შედარება ჩანაცვლებითი მკურნალობისას;
მეთადონის და ბუპრენორფინის ოპტიმალური დოზები;
დამატებითი ფსიქოსოციალური დახმარება.
ოპიოიდების აღკვეთასთან დაკავშირებით უნდა გავითვალისწინოთ შემდეგი საკითხები:
პრეპარატის არჩევა - მეთადონი, ბუპრენორფინი ან ალფა-2 ადრენერგული აგონისტები (მაგ. კლონიდინი და ლოფექსიდინი);
ოპიოიდების დაჩქარებული აღკვეთის მდგომარეობის სამკურნალო მეთოდები ოპიოიდური ანტაგონისტების (ნალოქსონი და ნალტრექსონი) გამოყენებით, მინიმალური ან მძიმე სედაციით;
პერორალური ნალტრექსონის გამოყენება ოპიოიდების მოსხნის შემდეგ რეციდივის
თავიდან ასაცილებლად;
ფსიქოსოციალური დახმარების გამოყენება ზემოთ მოცემულ მედიკამენტურ მკურნალობასთან ერთად;
არჩევანი სტაციონარულ და ამბულატორიულ დეტოქსიკაციას შორის.
 |
10.1 6.1 ოპიოიდური დამოკიდებულების დიაგნოსტიკა და შეფასება |
▲back to top |
შეფასებისთვის საჭიროა პაციენტსა და მკურნალ პერსონალს შორის ინფორმაციის თავისუფალ გაცვლაზე დაფუძნებული ურთიერთობის დამყარება. დასაწყისში, პაციენტს ალბათ მხოლოდ მკურნალობის პროცესის დასაწყებად საჭირო ინფორმაციის მიღება ენდომება. თუმცა, მას შემდეგ, რაც პაციენტსა და პერსონალს შორის ნდობა დამყარდება, შესაძლებელია მეტი ინფორმაციის გაზიარებაც. ამით მკურნალ პერსონალს უკეთესად შეეძლება მკურნალობის მორგება ინდივიდუალურ პაციენტზე.
პაციენტის ფიზიკური, ფსიქოლოგიური და სოციალური საჭიროებები შეფასების მნიშვნელოვანი ნაწილია. შეფასება ასევე უნდა მოიცავდეს ფაქტორებს, რომელთაც შესაძლოა გავლენა იქონიონ ნარკოტიკების გამოყენებაზე. ასეთი ფაქტორებია: წარსულში მკურნალობის გამოცდილება, ცხოვრების პირობები, კანონთან დაკავშირებული საკითხები, დასაქმება და სოციალურკულტურული გარემო.
კლინიცისტმა უნდა შეაგროვოს ნარკოტიკების მოხმარების ანამნეზი, რათა ზუსტად შეაფასოს შემდეგი:
რომელი ფსიქოაქტიური ნივთიერებები გამოიყენებოდა წარსულში და რომლები გამოიყენება ამჟამად;
თითოეული ნივთიერების მოხმარების პატერნი, მათ შორის, ინფორმაცია გამოყენების რაოდენობაზე და სიხშირეზე;
ნეიროადაპტაციის დონე თითოეული ნივთიერების მიმართ;
ნარკოტიკებით გამოწვეული ჯანმრთელობის და სოციალური პრობლემები;
მანამდე ჩატარებული მკურნალობის და სხვა ჩარევების შედეგი;
რა კრიტერიუმებს აკმაყოფილებს პაციენტი - საზიანო მოხმარების თუ დამოკიდებულების;
როგორ აღიქვამს პაციენტი მის მიერ ნარკოტიკის მოხმარებას;
ფაქტორები, რომლებიც ხელს უწყობდა და უწყობს პაციენტის მიერ ფსიქოაქტიური ნივთიერებების მოხმარებას.
პაციენტის მიერ დასახული ხანმოკლე, საშუალო და გრძელვადიანი მიზნები; რამ მოიყვანა პაციენტი ამჯერად სამკურნალო დაწესებულებაში.
კლინიცისტმა უნდა განასხვავოს წამალდამოკიდებულება და ნარკოტიკის მოხმარება დამოკიდებულების გარეშე, რადგან ამ კატეგორიების გარჩევა მნიშვნელოვანია მკურნალობის სტრატეგიის სწორად შერჩევისთვის.
პაციენტის გამოკვლევისას ინტოქსიკაციის და აღკვეთის მდგომარეობის ხარისხის ინტერპრეტაცია უნდა მოხდეს იმის მიხედვით, თუ ბოლოს როდის მიიღო პაციენტმა ნარკოტიკი.2 თუ ანამნეზში ინტრავენური შეყვანა ფიქსირდება, ნანემსარები უნდა ჩანდეს და შეესაბამებოდეს ანამნეზს (როგორც წესი, ჩანს როგორც ახალი, ისე ძველი ნანემსარები).
 |
10.1.1 6.1.1 შარდში ნარკოტიკის შემოწმება |
▲back to top |
თუ ხელმისაწვდომი და ფინანსურად შესაძლებელია, მკურნალობის დაწყებისას უნდა მოხდეს შარდის (ან სხვა ბიოლოგიური სითხის) ნარკოტიკებზე რუტინულად გამოკვლევა. იმისათვის, რომ ტესტირება მკურნალობისთვის შესაბამისად იქნეს მიჩნეული, საჭიროა მან უკანასკნელ პერიოდში ოპიოიდის მოხმარების ფაქტი დაადასტუროს. თუ შარდის გამოკვლევა ძვირია, ის მაშინ მაინც უნდა ჩატარდეს, როდესაც ბოლო პერიოდში ოპიოიდების მოხმარების ფაქტი სხვაგვარად ვერ დასტურდება (მაგ. ოპიოიდური აღკვეთის მდგომარეობა ან ინტოქსიკაცია). ნარკოტიკზე შარდის გამოსაკვლევი ტესტის უარყოფითი პასუხისა და აღკვეთის მდგომარეობის სიმპტომების არარსებობის კომბინაცია გამორიცხავს ამ ეტაპზე ოპიოიდების მიმართ ნეიროადაპტაციის არსებობას; თუმცა, არ გამორიცხავს ოპიოიდებზე დამოკიდებულებას ბოლო 12 თვის განმავლობაში. ამრიგად, დამოკიდებულების დიაგნოზი მხოლოდ შარდის ანალიზის შედეგზე დაყრდნობით არ უნდა დაისვას, მაგრამ შარდში ნარკოტიკის არსებობაზე უარყოფითი ტესტი და აღკვეთის მდგომარეობის სიმპტომების არარსებობა ეჭვქვეშ აყენებს ოპიოიდების და სხვა სედატიური პრეპარატების მოხმარებას.
შარდის გამოკვლევა, ანამნეზთან ერთად, ასევე სასარგებლოა ბოლო პერიოდში მოხმარებული სხვა ნივთიერებების იდენტიფიცირებისათვის. თუ სხვა, უკვე არსებული მონაცემები მიუთითებს დიაგნოზზე, შესაბამისი მკურნალობის დასაწყებად არ უნდა დაველოდოთ შარდის ტესტის შედეგს.
ნეიროადაპტაციის დასადასტურებლად ნალოქსონის ტესტის რუტინულად გამოყენება მიზანშეწონილი არ არის, რადგან მას შეუძლია ძლიერი აღკვეთის მდგომარეობის ეფექტის გამოწვევა. ჩვეულებრივ, იმავე ინფორმაციის მიღება შეიძლება პაციენტის ანამნეზის შეგროვებით, გასინჯვით და შარდის ანალიზის ინტერპრეტაციით. იმ პირობით, რომ პაციენტს წინაწარ მიეწოდება ინფორმაცია გვერდითი მოვლენების შესახებ, ნალოქსონის ტესტის გამოყენება შეიძლება შარდის გამოსაკვლევი ტესტის ალტერნატივის სახით ნეიროადაპტაციის არარსებობის დასადასტურებლად (მაგ. როცა წყდება საკითხი ოპიოიდური ანტაგონისტით ჩანაცვლებითი თერაპიის დაწყების შესახებ). ამ სიტუაციაში, შემთხვევით დადებითი რეაქცია გაცილებით უფრო მსუბუქია, ვიდრე რეაქცია, რომელიც ნეიროადაპტაციის დროს აღინიშნება.
 |
10.1.2 6.1.2 გამოკვლევა ინფექციურ დაავადებებზე |
▲back to top |
აივ-ის, C ჰეპატიტის და ხშირი ინფექციური დაავადებების ნებაყოფლობითი ტესტირება პაციენტს უნდა შევთავაზოთ, როგორც ინდივიდუალური შეფასების ნაწილი, რასაც თან ახლავს კონსულტაცია ტესტის ჩატარებამდე და მის შემდეგ. იმ რეგიონებში, სადაც აივ ინფექცია ფართოდაა გავრცელებული, პაციენტებს უნდა მოვუწოდოთ, ჩაიტარონ აივ ტესტირება. ასევე რეკომენდებულია სეროლოგიური ტესტირება და ვაქცინაცია B ჰეპატიტზე. როგორც ზემოთ იყო განხილული (ნაწილი 5.6), ზოგიერთ შემთხვევაში შეიძლება უფრო ეფექტიანი იყოს B ჰეპატიტზე ვაქცინაცია ტესტირებამდე და ვაქცინაციის დაჩქარებული ცხრილის გამოყენება.
შეფასების დროს ასევე უნდა განვიხილოთ ტუბერკულოზი და სქესობრივად გადამდები დაავადებები.
ორსულობის ტესტი ყველა ქალს უნდა შევთავაზოთ, განსაკუთრებით მათ, ვინც ფიქრობს ოპიოიდების მოხსნაზე, რადგან ამ ტესტის შედეგმა შეიძლება გავლენა იქონიოს მკურნალობის არჩევანზე.
 |
10.1.3 6.1.3 პაციენტის იდენტიფიცირება |
▲back to top |
ზოგიერთ შემთხვევაში, შეიძლება აუცილებელი იყოს პაციენტის იდენტურობის დადგენა, განსაკუთრებით, თუ მოსალოდნელია მკურნალობის დაწყება კონტროლირებადი პრეპარატებით. თუ პაციენტს საიდენტიფიკაციო საბუთი არ გააჩნია, სასურველია ფოტოს გადაღება და მისი ჩაკვრა ჩანაწერში, რომელსაც ხელს აწერს მკურნალი ექიმი, რათა მოხდეს პაციენტის იდენტიფიცირება ამ კლინიკაში. პაციენტის ვინაობა უნდა იყოს კონფიდენციალური და არ უნდა გამჟღავნდეს პაციენტის თანხმობის გარეშე. ინფორმაციის შეგროვების და ჩაწერისას პაციენტს უნდა ეცნობოს, რომ დაცული იქნება ამ ინფორმაციის კონფიდენციალურობა.
 |
10.1.4 6.1.4 შეფასების დასრულება |
▲back to top |
ზოგჯერ შესაძლებელი არ არის საწყისი შეფასების ერთ დღეში დასრულება. მაგ., პაციენტს შეიძლება ჰქონდეს ინტოქსიკაცია, აღკვეთის მდგომარეობა ან კრიზისი. ამგვარ შემთხვევებში, შეიძლება აუცილებელი იყოს საწყის შეფასებაზე დამყარებული გეგმის შემუშავება, რაც მოიცავს უფრო ღრმა შეფასებას და საწყის მკურნალობაზე პაციენტის რეაქციის შესწავლას.
 |
10.1.5 6.1.5 დიაგნოსტიკური კრიტერიუმები |
▲back to top |
ოპიოიდური დამოკიდებულების დიაგნოზს დიდი მნიშვნელობა აქვს პროგნოზის და მკურნალობის შერჩევისთვის. ოპიოიდური დამოკიდებულების მქონე პაციენტს აქვს მძიმე დაავადებების ან გარდაცვალების დიდი რისკი ოპიოიდურ დამოკიდებულებასთან დაკავშირეული ქცევის გამო.
დაავადებების საერთაშორისო კლასიფიკაცია, მე-10 გადასინჯვა (დსკ-10) ოპიოიდურ დამიკიდებულებას შემდეგნაირად განსაზღვრავს: „ფიზიოლოგიურ, ქცევით და კოგნიტურ ფენომენთა ერთობლიობა, რომლის დროსაც ოპიოიდების მოხმარებას მოცემული ინდივიდისთვის გაცილებით მეტი პრიორიტეტი აქვს, ვიდრე სხვა ქცევებს, რომელთაც უწინ დიდი მნიშვნელობა ჰქონდა“. დამოკიდებულების სინდრომის მთავარი მახასიათებელია ლტოლვა (ხშირად ძლიერი, ზოგჯერ დაუძლეველი) ოპიოიდების (მათ შორის სამედიცინო მიზნით დანიშნული ოპიოიდების) მიმართ. როცა ადამიანი ოპიოიდებზე დამოკიდებულია, ნარკოტიკის მოხმარების ხელახლა დაწყება აღკვეთის მდგომარეობის პერიოდის შემდეგ უფრო სწრაფად იწვევს სინდრომის ნიშნების გამოვლენას, ვიდრე არადამოკიდებულ ინდივიდებში [104].
დსკ-10-ის მიხედვით, ოპიოიდებზე დამოკიდებულების დიაგნოსტიკური კრიტერიუმებია:
ოპიოიდების მიღების ძლიერი კომპულსიური სურვილი;
სირთულეები ოპიოიდის მოხმარებასთან დაკავშირებული ქცევების კონტროლთან დაკავშირებით;
ფიზიოლოგიური აღკვეთის მდგომარეობა ოპიოიდის მოხმარების შეწყვეტის ან დოზის შემცირების დროს, რაც გამოვლინდება ქვემოთ ჩამოთვლილთაგან ერთ-ერთით:
- დამახასიათებელი აღკვეთის სინდრომი;
- ოპიოიდების (ან მონათესავე ნივთიერებების) მოხმარება აღკვეთის მდგომარეობის სიმპტომების შემსუბუქების ან თავიდან აცილების მიზნით;
ტოლერანტობის განვითარება, რაც ნიშნავს, რომ უწინ დაბალი დოზებით მიღწეული ეფექტის მისაღებად საჭირო ხდება ოპიოიდების მზარდი დოზები;
ოპიოიდების მოხმარების გამო სხვა სიამოვნების ან ინტერესების პროგრესირებადი უგულებელყოფა;
უფრო და უფრო მეტი დროის დაკარგვა ოპიოიდების მოპოვებაზე და უფრო და უფრო ძნელად გათავისუფლება მათი ეფექტებისგან;
ოპიოიდების მოხმარების გაგრძელება მიუხედავად მათი აშკარად გამოხატული მავნე შედეგებისა, როგორიცაა დეპრესიული გუნება-განწყობა ნარკოტიკის გამოყენების შემდეგ ან კოგნიტური ფუნქციის ნარკოტიკებთან დაკავშირებული დარღვევა (საჭიროა განისაზღვროს, იცოდა ან შეიძლებოდა თუ არა სცოდნოდა მომხმარებელს ყოველივე ამასთან დაკავშირებული ზიანის ბუნება და მასშტაბი).
ოპიოიდების მოხმარების პატერნების პირადი რეპერტუარის შემცირება ასევე დამოკიდებულების დამახასიათებელი ნიშანია.
ოპიოიდური დამოკიდებულება არ ვითარდება რეგულარული გამოყენების პერიოდის გარეშე, თუმცა მხოლოდ რეგულარული მოხმარება დამოკიდებულების განვითარებისათვის საკმარისი არ არის.
დამოკიდებულების საბოლოო დიაგნოზი, ჩვეულებრივ, უნდა დაისვას მხოლოდ მაშინ, თუ ბოლო წლის განმავლობაში დროის რომელიმე მონაკვეთში აღინიშნა სამი ან მეტი დიაგნოსტიკური კრიტერიუმის არსებობა.
 |
10.1.6 6.1.6 დიაგნოზის დასმა |
▲back to top |
ოპიოიდური დამოკიდებულების დიაგნოზი ძირითადად პაციენტის მიერ მოწოდებული ანამნეზის საფუძველზე ისმება. ზოგჯერ პაციენტი შეიძლება მოტივირებული იყოს, გააზვიადოს ან დააკნინოს მის მიერ ნარკოტიკის მოხმარება. ამდენად, ჩვეულებრივ, დიაგნოზის სწორად დასასმელად აუცილებელია პაციენტის ანამნეზი გამყარდეს ფიზიკური გამოკვლევის და დიაგნოსტიკური ტესტების შედეგებით, ზოგჯერ კი - ახლობლებისგან შეკრებილი ანამნეზით. მართალია, ოპიოიდური დამოკიდებულების წინასწარი დიაგნოზის დასმა შესაბამისი სწავლების შემდეგ ჯანდაცვის ნებისმიერ მუშაკს შეუძლია, მაგრამ ვიდრე ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობა დაიწყება, საჭიროა დიაგნოზი სამედიცინო პერსონალმა დაადასტუროს.
ნანემსარები
ნანემსარების დათვალიერებამ შეიძლება სასარგებლო ინფორმაცია მოგვცეს საინექციო ნარკოტიკების გამოყენების დროისა და ხანგრძლივობის შესახებ. ბოლო პერიოდის ნანემსარები პატარა და წითელია, ზოგჯერ ანთებითი, ან შემოფარგლულია მცირე სისხლნაჟღენთით. ძველი ინექციის ადგილი, ჩვეულებრივ, ანთებითი არ არის, მაგრამ ზოგჯერ ახასიათებს შეცვლილი პიგმენტაცია (უფრო მუქი ან ღია), კანი შეიძლება იყოს ატროფიული - გარეგნულად გამოიყურება როგორც ჩავარდნილი ადგილი. მოცემულ პერიოდში ნეიროადაპტაციის მქონე პაციენტს ჩვეულებრივ, აქვს ახალი და ძველი ნანემსარები. ინექციისთვის შეიძლება ბევრი ადგილი იქნეს გამოყენებული, თუმცა, იდაყვის ფოსო (იდაყვის სახსრის შიგნითა ზედაპირი) და საზარდული ინექციის ყველაზე ხშირი ადგილებია.
შარდში ნარკოტიკის გამოსაკვლევი ტესტის ინტერპრეტაცია
შარდში ნარკოტიკის გამოსაკვლევი ტესტი გვაძლევს ინფორმაციას ბოლო პერიოდში ნარკოტიკის მოხმარების შესახებ; ეს ინფორმაცია ავსებს შეფასებას. ტესტის შედეგის ზუსტი ინტერპრეტაცია დამოკიდებულია სპეციფიკურ კომერციულ ტესტზე ან გამოყენებულ რეაქტივზე. ზოგადად, ოპიოიდების კლასის პრეპარატზე დადებითი შედეგი მიუთითებს უკანონო ან რეცეპტით გამოწერილი ოპიოიდის მოხმარებაზე ბოლო რამდენიმე დღის განმავლობაში. თუმცა, დადებითი რეაქცია შეიძლება მოგვცეს დიდი რაოდენობით ყაყაჩოს თესლის მიღებამ. ბევრი კომერციული რეაქტივი ვერ ამოიცნობს ბუპრენორფინს, მაგრამ ეს სიტუაცია იცვლება; ამიტომ, ყველაზე კარგი გამოსავალია, ლაბორატორიაში დავაზუსტოთ, თუ რა რეაქტივი გამოიყენება. ზოგიერთი გამოკვლევა, როგორიცაა გაზქრომატოგრაფია და მასსპექტრომეტრია (GCMS), განსაზღვრავს სპეციფიკურ ოპიოიდს. ჰეროინი იშლება 6-მონოაცეტილმორფინად (6-MAM), შემდეგ მორფინად და შემდეგ კოდეინად; ამრიგად, 6-MAM-ის არსებობა, ჩვეულებრივ, სპეციფიკურად ადასტურებს ჰეროინის მოხმარებას ბოლო 24 საათის განმავლობაში. მორფინი, კოდეინის მცირე რაოდენობით ან მის გარეშე, შეიძლება მიუთითებდეს ბოლო რამდენიმე დღის განმავლობაში ჰეროინის ან მორფინის გამოყენებაზე. მორფინის მცირე რაოდენობის არსებობა კოდეინის დიდ რაოდენობასთან ერთად შეიძლება ნიშნავდეს კოდეინის დიდი დოზების მიღებას, რადგან კოდეინს შეუძლია მორფინად მეტაბოლიზება, თუმცა მისი დიდი ნაწილი სხვა გზით მეტაბოლიზდება.
ოპიოიდური ინტოქსიკაციის და აღკვეთის მდგომარეობის ინტენსივობა
ოპიოიდური ინტოქსიკაციის ნიშნები მოიცავს შემდეგს: ქუთუთოების დაშვება, შევიწროებული გუგები, სუნთქვის სიხშირის შემცირება, თავის ქინდვრა, ქავილი და ნაკაწრები (ჰისტამინის გამოყოფის გამო).
ოპიოიდური აღკვეთის მდგომარეობის ნიშნები მოიცავს შემდეგს: მთქნარება, შფოთვა, კუნთების ტკივილი, აბდომინური სპაზმები, თავის ტკივილი, გაფართოებული გუგები, უძილობა, ღებინება, დიარეა, ბატის კანი, აჟიტირებულობა, მიოკლონიები, მოუსვენრობა, დელირიუმი, გულყრები, აჩქარებული სუნთქვა, მომატებული არტერიული წნევა და პულსი. მე-10 დანართში მოცემულია ეფექტიანი სკალები ოპიოიდური აღკვეთის მდგომარეობის სიმძიმის შესაფასებლად.
 |
10.2 6.2 მკურნალობის მეთოდის არჩევა |
▲back to top |
უნდა მიენიჭოს თუ არა უპირატესობა აგონისტებით მხარდამჭერ მკურნალობას (ანუ მეთადონით ან ბუპრენორფინით მხარდამჭერი თერაპია) ნარკოტიკის მოხსნასა და შემდგომ ანტაგონისტებით პერორალურ მკურნალობასთან (ნალტრექსონი) ან მხოლოდ მოხსნასთან შედარებით?
იხ. მონაცემები 1-ლ დანართში: ნაწილი A1.1 და A1.2 მეთადონი მოხსნასთან შედარებით ნაწილი A1.3 ბუპრენორფინი მოხსნასთან ან პლაცებოსთან შედარებით ნაწილი A1.11 ნალტრექსონი პლაცებოსთან შედარებით |
ეფექტიანობა
მეთადონი მოხსნასთან შედარებით
კოქრეინის ახლახან განახლებული მიმოხილვა [105], რომელიც ეხება მეთადონით მხარდამჭერ მკურნალობას ოპიოიდების ჩანაცვლების გარეშე მკურნალობასთან შედარებით, განიხილავს სამ რანდომიზებულ კონტროლირებულ კვლევას, რომლებშიც მეთადონი შედარებულ იქნა ოპიოიდების მოხსნასა და პლაცებოსთან [106, 107, 108]. კვლევებმა უჩვენა, რომ ოპიოიდების მოხსნასთან ან პლაცებოსთან შედარებით, მეთადონით ჩანაცვლებითი მკურნალობა მნიშვნელოვნად ამცირებს ოპიოიდების უკანონო გამოყენების სიხშირეს (ფარდობითი რისკი (RR 0.32; 95%-იანი საიმედოობის ინტერვალი [CI] 0.23-0.44, მაღალი ხარისხის მტკიცებულება) და ზრდის მკურნალობის პროგრამაში დაყოვნებას (RR 3.05; 95%-ი CI 1.75-5.35). დაკვირვების მეთოდით ჩატარებული კვლევები გვიჩვენებს, რომ სიკვდილიანობის დონე მეთადონით მკურნალობის დროს დაახლოებით სამჯერ ნაკლებია, ვიდრე იმ პაციენტებში, ვინც არ იტარებს მკურნალობას (RR 0.37; 95%-ი CI 0.29-0.48, დაბალი ხარისხის მტკიცებულება).
მეთადონი აივ ინფექციის რისკს დაახლოებით 50%-ით ამცირებს (RR 0.45, 95% -ი CI 0.35-0.59, საშუალო ხარისხის მტკიცებულება). ასევე ნაკლებია სეროკონვერსიის მაჩვენებელი (RR 0.36, 95%-ი CI 0.19-0.66, დაბალი ხარისხის მტკიცებულება) მოხსნასთან ან მკურნალობის გარეშე დატოვებასთან შედარებით. კვლევები, სადაც შედარებული იქნებოდა მეთადონით და ნალტრექსონით მკურნალობა, ვერ მოიძებნა.
ბუპრენორფინი მოხსნასთან ან პლაცებოსთან შედარებით
კოქრეინის მიმოხილვა ბუპრენორფინის შესახებ განიხილვას ერთ კვლევას, სადაც ბუპრენორფინი შედარებულია პლაცებოსთან [109] და ერთ კვლევას, სადაც 1 მგ დღეში შედარებულია უფრო მაღალ დოზებთან [110]. პლაცებოსთან შედარებით (1 მგ პლაცებოს გამოყენებით) ბუპრენორფინი იწვევს ჰეროინის გამოყენების დოზადამოკიდებულ შემცირებას და აუმჯობესებს პაციენტის მკურნალობის პროგრამაში დაყოვნების მაჩვენებელს. ბუპრენორფინის 16 მგ (პლაცებოსთან შედარებით) მკურნალობის პროგრამაში დაყოვნების მაღალ მაჩვენებელთან (RR 1.52, 95%-ი CI 1.23-1.88) და მორფინზე დადებითი შარდის ნაკლებ შემთხვევებთან არის დაკავშირებული (სტანდარტიზებული საშუალო სხვაობა (SMD) - 0.65, 95% -ი CI - 0.86-0.44).
ნალტრექსონი პლაცებოსთან შედარებით
კოქრეინის მიმოხილვა ოპიოიდური დამოკიდებულების რეციდივის პრევენციისთვის ნალტრექსონის გამოყენების შესახებ განიხილავს 6 კვლევას, რომლებშიც სულ 249 პაციენტი მონაწილეობდა [170]. პაციენტებში, რომლებმაც გაიარეს დეტოქსიკაცია, ნალტრექსონი უფრო ეფექტიანია, ვიდრე პლაცებო, ჰეროინის გამოყენების შემცირების თვალსაზრისით (RR 0.72, 95%-ი CI 0.58-0.90, დაბალი ხარისხის მონაცემი), მაგრამ არ ახდენს გავლენას პაციენტის მკურნალობის პროგრამაში დაყოვნებაზე (RR 1.08, 95% -ი CI 0.67-1.34).
უსაფრთხოება
მეთადონით ჩანაცვლებითი თერაპია დაკავშირებულია სიკვდილიანობის გაზრდილ მაჩვენებელთან მკურნალობის პირველი ორი კვირის განმავლობაში სუნთქვის დათრგუნვის გამო [111]. ამ დროის გავლის შემდეგ აღინიშნება სიკვდილიანობის
მაჩვენებლის შემცირება და ეს ეფექტი ძალაშია მკურნალობის შეწყვეტამდე. პაციენტების უმრავლესობა რაღაც ეტაპზე განაახლებს ოპიოიდის მოხმარებას. ოპიოიდების მოხსნის გამო მათ მიმართ ტოლერანტობის შემცირებამ შეიძლება გამოიწვიოს ოპიოიდების ზედოზირება.
ფარმაკოლოგიური კვლევები მიუთითებს, რომ ბუპრენორფინს მეთადონთან შედარებით ზედოზირების ნაკლები რისკი აქვს, მაგრამ ზედოზირების შემთხვევები მაინც აღწერილია სხვა სედატიურ ნივთიერებეთან ერთად ბუპრენორფინის მიღებისას.
ნალტრექსონით მკურნალობამ შეიძლება გაზარდოს სედატიური ნივთიერებებით ზედოზირების რისკი პრეპარატის შეწყვეტის შემდგომ პერიოდში. ოპიოიდების მოხსნის ზოგიერთი დაჩქარებული მეთოდი, რომელიც გამოიყენება პაციენტში ნალტრექსონით მკურნალობის და საწყებად, - განსაკუთრებით ანტაგონისტების გამოყენება ღრმა სედაციასთან ერთად, - ასევე ზრდის ფატალური გართულებების რისკს.
ოპიოიდური აგონისტებით მკურნალობის კურსში ჩართული პაციენტების მნიშვნელოვან რაოდენობას უვითარდება გვერდითი მოვლენები (იხ. ნაწილი 6.5). მეთადონი იწვევს QT ინტერვალის მცირედ გაზრდას (ანუ გულის ელექტრონულ ციკლში დრო Q კბილის დაწყებასა და T კბილის დამთავრებას შორის), რამაც შეიძლება გამოიწვიოს სიცოცხლისათვის საშიში არითმიების განვითარების გაზრდილი შანსი, თუმცა, რისკის ზრდის მაჩვენებლის ზუსტი განსაზღვრა რთულია. ბუპრენორფინი და ნალტრექსონი QT ინტერვალს არ ახანგრძლივებს.
ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობის უკუჩვენებებს, ასევე სიტუაციებს, როდესაც ეს მკურნალობა სიფრთხილით უნდა დაინიშნოს, მიეკუთვნება ღვიძლის დეკომპენსირებული დაავადებები (როგორებიცაა სიყვითლე და ასციტი, რადგან ამგვარ სიტუაციაში ოპიოიდებს შეუძლია ღვიძლისმიერი ენცეფალოპათიის განვითარების დაჩქარება), აგრეთვე მწვავე ასთმა და სუნთქვის უკმარისობის სხვა მიზეზები.
ფსიქიატრიული დაავადების, ოპიოიდებისადმი ნეიროადაპტაციის დაბალი დონის (მაგ. ცოტა ხნის წინ ციხეში მოხვედრა, რადგან ბევრი წამალდამოკიდებული ციხეში მოხვედრის შემდეგ არ მოიხმარს ოპიოიდებს იმ რაოდენობით, რაც ოპიოიდებისადმი მისი დამოკიდებულების დონეს შეესაბამება) და მნიშვნელოვანი თანმხლები სომატური დაავადებების დროს ოპიოიდური აგონისტებით მკურნალობა და ოპიოიდური დეტოქსიკაციისას მრავალი მედიკამენტის გამოყენება სიფრთხილით უნდა განხორციელდეს.
ოპიოიდების აღკვეთის მდგომარეობის მართვისას სიფრთხილეა საჭირო ორსულობის (რადგან მოხსნამ შეიძლება აბორტი გამოიწვიოს) და სერიოზული მწვავე ფიზიკური ან ფსიქიატრიული დაავადებების (რადგან აღკვეთის მდგომარეობამ შეიძლება გამოიწვიოს თანმხლები დაავადებების დამძიმება ან მათი მკურნალობის გართულება) დროს.
ხარჯების ეფექტიანობა
ბოლოდროინდელ კვლევაში ჯანმოს წევრ სხვადასხვა ქვეყნებში (ინდონეზია, ირანი, ლიტვა და პოლონეთი) ოპიოიდური აგონისტებით ჩანაცვლებითი თერაპიის შესახებ [112] შეგროვდა მონაცემები რესურსების გამოყენებასა და დანახარჯებზე მეთადონით და ბუპრენორფონით მხარდამჭერი ჩანაცვლებითი თერაპიის დროს.
მეთადონით და ბუპრენორფინით ხანრგძლივი მხარდამჭერი მკურნალობის საერთო თვიური ღირებულება (საწყისი ინდუქციის ფაზის ჩათვლით) მერყეობს ისეთი მცირე თანხიდან, როგორიცაა 26-36 აშშ დოლარი ინდონეზიასა და ირანის ისლამურ რესპუბლიკაში (დაახლოებით, 1 აშშ დოლარი დღეში), 296 აშშ დოლარამდე პოლონეთში (დაახლოებით, 10 აშშ დოლარი დღეში). ეს გვაძლევს დაახლოებით იმ დიაპაზონს, რომელშიც უნდა განხორციელდეს მოსალოდნელი ინვესტიცია დაბალი ან საშუალო შემოსავლის ქვეყანაში მეთადონით მხარდამჭერი მკურნალობის უზრუნველსაყოფად. მაღალშემოსავლიან ქვეყნებში მეთადონით და ბუპრენორფინით ჩანაცვლებითი თერაპია წელიწადში დაახლოებით 5000 აშშ დოლარი ჯდება, ანუ 15 აშშ დოლარი დღეში [113].
მედიკამენტის მოწოდების ღირებულების შეფასება ბიუჯეტის დაგეგმვის ადეკვატური საფუძველი არ არის, რადგან ეს მთლიანი სერვისის ღირებულების მხოლოდ ნაწილს წარმოადგენს (მაგ <20%-ზე ირანის ისლამურ რესპუბლიკაში). ავსტრალიაში, კანადაში, აშშ-ში და გაერთიანებულ სამეფოში ჩატარებულმა კვლევებმა შეაფასა მკურნალობის გავლენა ჯანდაცვის და სოციალური დაცვის ღირებულებაზე, პროდუქტიულობის დაქვეითებასა და დანაშაულზე. ასე რომ, ეს კვლევები აფასებს ეკონომიკურ ინვესტირებას ოპიოიდური დამოკიდებულების მკურნალობაში [64, 114]. ისინი გვიჩვენებს, რომ ოპიოიდური დამოკიდებულების მკურნალობა თვითონ იფინანსებს საკუთარ თავს, რადგან მკურნალობაზე დანახარჯი უფრო ნაკლებია, ვიდრე მკურნალობით გამოწვეული სოციალური ხარჯების დანაზოგი. ამ კვლევების ექსტრაპოლირება რთულია დაბალშემოსავლიან ქვეყნებზე.
მაღალშემოსავლიან ქვეყნებში ხარჯების ეფექტიანობის მაჩვენებლების შეფასებისას აღმოჩნდა, რომ ამ თვალსაზრისით როგორც მეთადონით, ისე ბუპრენორფინით ჩანაცვლებითი თერაპია ეფექტიანია ხარჯი-სარგებელის ანალიზის მისაღებ ზღვარზე საკმაოდ დაბლა [115,116].
ოპიოიდების აღკვეთის ერთი ეპიზოდის მკურნალობის ღირებულება სხვადასხვა პროგრამაში განსხვავებულია; ეს დამოკიდებულია მკურნალობის მეთოდზე, მკურნალობის ხანგრძლივობაზე, გამოყენებულ მედიკამენტზე და პერსონალის რესურსებზე.
მხარდამჭერ თერაპიასა და მოხსნას შორის არსებული განსხვავებების გამო, გრძელვადიან პერსპექტივაში რთულია ხარჯის განსაზღვრა, როდესაც კეთდება შემდეგი არჩევანი:
ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა, რომელიც დაბალინტენსიური და ხანგრძლივია და რეციდივის დაბალი მაჩვენებელი აქვს ან
ოპიოიდების მოხსნა, რომელიც მაღალინტენსიური და ხანმოკლეა და რეციდივის შედარებით მაღალი მაჩვენებელი აქვს.
შეზღუდული მონაცემები
ვერ მოინახა კვლევები, სადაც პირდაპირ იქნებოდა შედარებული მკურნალობის სამი სხვადასხვა მეთოდი რანდომიზებული დიზაინის გამოყენებით. შეიძლება, ამ პრინციპის კვლევებით ამ საკითხის შესწავლა რთული იყოს, რადგან პაციენტებს არ ენდომებათ მკურნალობის მეთოდის არჩევის უფლების შეზღუდვა. მოძებნილ კლინიკურ კვლევებში ერთმანეთთან შედარებულ იქნა ოპიოიდების ერთბაშად მოხსნის გადაწყვეტილება და მეთადონით მხარდაჭერა. პრაქტიკაში, ოპიოიდების მოხსნის წარუმატებელ მცდელობას მოჰყვება განმეორებითი მცდელობები, ვიდრე პაციენტი არ მიაღწევს წარმატებას ან შეწყვეტს ოპიოიდების მოხსნის მცდელობას. ამ მიმოხილვით ვერ მოიძებნა რანდომიზებული კონტროლირებული კვლევები, რომლებშიც შედარებულ იქნებოდა მოხსნის განმეორებითი მცდელობები ოპიოიდებით მხარდამჭერ ჩანაცვლებით მკურნალობასთან. ასევე, არ იყო კვლევები, სადაც მეთადონით და ბუპრენორფინით მხარდამჭერი მკურნალობა შედარებულ იქნებოდა ოპიოიდების მოხსნასთან და ნალტრექსონით რეციდივის პრევენციასთან.
მკურნალობის განხილვა
პრაქტიკაში, ხშირად მკვეთრი ზღვარი წაშლილია ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობასა და მეთადონის და ბუპრენორფინის კლებადი დოზების გამოყენებით ოპიოიდების მოხსნას შორის. პაციენტები ხშირად იწყებენ აგონისტის დოზების კლებას და, იმავდროულად, ცდილობენ ჰეროინის მოხმარების შეწყვეტას; პერიოდულად, რეციდივის დროს, ისინი ზრდიან აგონისტის დოზას.
ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის სარგებელი
ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის ყველაზე მნიშვნელოვანი სარგებელი მასთან დაკავშირებული სიკვდილიანობის გაცილებით დაბალი მაჩვენებელია ოპიოიდების მოხსნასთან შედარებით (ამ ეფექტის მონაცემი უფრო ძლიერია მეთადონისთვის, ვიდრე ბუპრენორფინისთვის). ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა იწვევს ჰეროინის მოხმარების შემცირებას პაციენტების უმრავლესობაში; ზოგადად, უკეთესია მკურნალობის პროგრამაში დაყოვნების მაჩვენებელი.
არასასურველი ეფექტები და შედეგები
ბევრი პაციენტისთვის სერიოზულ დისკომფორტს ქმნის ყველა დოზის ზედამხედველობა. ზოგიერთ მათგანს მეთადონის მიმართ გვერდითი მოვლენები აღენიშნება (მათ შორის, დოზებს შორის ოპიოიდური აღკვეთის მდგომარეობის სიმპტომები). მეთადონზე და ბუპრენორფინზე მყოფ პაციენტებს კვლავაც შეუძლიათ ოპიოიდების ეფექტების განცდა, თუ აკრძალულ ოპიოიდებს მიიღებენ. მიუხედავად იმისა, რომ ეს ეფექტები შემცირებულია, ისინი მთლიანად არ არის ბლოკირებული, როგორც ეს ნალტრექსონის შემთხვევაში იქნებოდა. ეს იწვევს ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობის პროგრამაში დარჩენის მაღალ მაჩვენებელს იმ პაციენტებშიც კი, რომლებიც ჰეროინსაც მოიხმარენ, მაგრამ, ამავდროულად შეიძლება დიდი ხნით დაყოვნდეს ხანგრძლივი სიფხიზლის მიღწევა. თუ მეთადონზე და ბუპრენორფინზე მყოფი პაციენტები დოზებს მხოლოდ ზედამხედველობით იღებენ, მათთვის მგზავრობა გარკვეულ სირთულეებთან იქნება დაკავშირებული. ზედამხედველობის გარეშე მიღება იწვევს ოპიოიდური აგონისტების არადანიშნულებით მოხმარების დონის ზრდას, მათ შავ ბაზარზე მოხვედრას; ასევე, სახლში მისაღებ დოზებს ზოგჯერ იღებენ ბავშვები და ოპიოიდებს მიუჩვეველი მოზრდილები, რასაც ფატალური შედეგები მოჰყვება. მეთადონის და ბუპრენორფინის შეწყვეტამ შეიძლება გამოიწვიოს აღკვეთის სინდრომი, რომელიც უფრო გახანგრძლივებულია და ზოგჯერ უფრო მძიმეც, ვიდრე ჰეროინის აღკვეთის მდგომარეობა. აგრეთვე, მეთადონის შეწყვეტის შემდეგ ბევრი პაციენტი განაახლებს ჰეროინის მოხმარებას, ხანგრძლივი მკურნალობის შემდეგაც კი.
დასკვნა
პაციენტების უმრავლესობისთვის, ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა უკეთეს შედეგებს იძლევა, ვიდრე მოხსნის მცდელობა (მოხსნის შემდეგ ნალტრექსონის დანიშვნით ან მის გარეშე). კერძოდ, ოპიოიდური აგონისტებით ჩანაცვლებით მკურნალობის კურსში ჩართულ პაციენტებს ცოცხლად დარჩენის უფრო მეტი შანსი აქვთ, ვიდრე მათ, ვინც ამგვარ მკურნალობას არ იტარებს. ისინი უფრო ხშირად ანებებენ თავს ჰეროინის მოხმარებას და კონტაქტში რჩებიან მკურნალობის პროგრამასთან.
რეკომენდაცია ოპიოიდური დამოკიდებულების ფარმაკოლოგიური მკურნალობისთვის კლინიცისტებმა პაციენტს უნდა შესთავაზონ ოპიოიდების მოხსნა, ოპიოიდური აგონისტებით მხარდამჭერი თერაპია და ოპიოიდური ანტაგონისტებით (ნალტრექსონი) მკურნალობა, მაგრამ პაციენტების უმრავლესობას უნდა ვურჩიოთ, სცადოს ოპიოიდური აგონისტებით მხარდამჭერი თერაპია.
რეკომენდაცია ოპიოიდებზე დამოკიდებული პაციენტებისთვის, რომლებიც არ იწყებენ ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას, განიხილეთ ანტაგონისტით (ნალტრექსონით) ფარმაკოთერაპიის საკითხი ოპიოიდის მოხსნის შემდეგ.
|
 |
10.3 6.3 ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა |
▲back to top |
 |
10.3.1 6.3.1 ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის ჩვენებები |
▲back to top |
რა არის ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის ჩვენებები? აგონისტებით მხარდამჭერი მკურნალობა ნაჩვენებია ოპიოიდებზე დამოკიდებული ყველა პაციენტისათვის, რომლებსაც შეუძლიათ ინფორმირებული თანხმობის მოცემა და რომელთათვისაც სპეციფიკური უკუჩვენებები არ არსებობს. იმის გათვალისწინებით, რომ მკურნალობა ხანგრძლივია და პირველ ორ კვირაში ინტოქსიკაციის პოტენციური საფრთხე არსებობს, ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობის დაწყებამდე აუცილებელია მაღალი სანდოობის დიაგნოზის დასმა. თუ დიაგნოზი ვერ დასტურდება ოპიოიდური აღკვეთის სინდრომზე დაკვირვებით, ნანემსარების ან წარსულში მკურნალობის მცდელობის არსებობით, მაშინ მკურნალობა სიფრთხილით და დაკვირვებით უნდა დავიწყოთ; ამგვარ სიტუაციაში ოპიოიდური აგონისტებით ინტოქსიკაციის არარსებობა ოპიოიდური ტოლერანტობის პირდაპირი მაჩვენებელი იქნება. პერსონალი ფრთხილად უნდა იყოს, როდესაც პაციენტს უარს ეუბნება ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაზე, რადგან ამგვარ პაციენტებს მკურნალობის გარეშე დატოვებისას ცუდი კლინიკური შედეგი აქვთ [117].
 |
10.3.2 6.3.2 აგონისტებით მხარდამჭერი მკურნალობის არჩევა |
▲back to top |
იმ პაციენტებისათვის, რომელთათვისაც გადაწყვეტილია აგონისტებით მხარდამჭერი თერაპიის დაწყება, რომელს უნდა მიენიჭოს უპირატესობა - მეთადონს თუ ბუპრენორფინს?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.4 |
ეფექტიანობა
კოქრეინის კოლაბორაციამ სისტემატური განხილვა და მეტაანალიზი ამ საკითხზე 2004 წელს [118] ჩაატარა და 2008 წელს განაახლა (გამოქვეყნების პროცესშია). ათ კვლევაში ადარებდნენ მეთადონს და ბუპრენორფინს მოქნილი დოზებით, 6 მგ-ზე მეტი ბუპრენორფინით ან 50 მგ-ზე მეტი მეთადონით.
ბუპრენორფინის თავისუფალი დოზები მეთადონის თავისუფალ დოზებთან შედარებით
თავისუფალი დოზების გამოყენებისას ბუპრენორფინი მეთადონთან შედარებით ნაკლებად ეფექტიანია პაციენტის მკურნალობის პროგრამაში დარჩენის თვალსაზრისით (6 კვლევა, 837 მონაწილე; RR = 0.82, 95%-ი CI: 0.69-0.96). ჰეროინის გამოყენების სიხშირით (დგინდება შარდში მორფინის ტესტით) სტატისტიკურად მნიშვნელოვნად არ განსხვავდება (6 კვლევა, 836 მონაწილე; SMD = -0.12, 95%-ი CI: -0.26-0.02); ასევე არ არის განსხვავება თვით პაციენტის მიერ ჰეროინის მოხმარების აღიარების თვალსაზრისით (2 კვლევა, 326 მონაწილე; SMD = -0.10, 95%-ი CI: -0.32-0.12).
ბუპრენორფინის საშუალო დოზა (6-8 მგ/დღეში) მეთადონის საშუალო დოზასთან (50-80 მგ/დღეში) შედარებით
მეთადონით მკურნალობის დროს, საშუალო დოზების გამოყენებისას, პროგრამაში დარჩენის უკეთესი მაჩვენებელია, ვიდრე ბუპრენორფინით მკურნალობისას (RR = 0.79, 95%-ი CI 0.64-0.99, საშუალო ხარისის მტკიცებულება). ასევე, ბუპრენორფინის გამოყენებისას ჰეროინის მოხმარება უფრო ხშირია, რაც მორფინზე შარდის
დადებითი ანალიზით დადგინდა (3 კვლევა, 314 მონაწილე: SMD = 0.27, 95%-ი CI 0.05-0.50). ჰეროინის მოხმარების თვითაღიარების მხრივ განსხვავება არ იყო (2 კვლევა, 74 მონაწილე, SMD = -0.02, 95%-ი CI - 0.48-0.45).
მონაცემები უსაფრთხოების შესახებ
როგორც ნაწილობრივ აგონისტს, ბუპრენორფინს უკეთესი ფარმაკოლოგიური უსაფრთხოების პროფილი აქვს, ვიდრე მეთადონს. მონაცემები უსაფრთხოების შესახებ რანდომიზებული კონტროლირებული კვლევებიდან არ გვიჩვენებს მნიშვნელოვან განსხვავებას მეთადონსა და ბუპრენორფინს შორის საკვლევ პირთა მცირე რაოდენობის გამო. ყველაზე მყარი მონაცემები ბუპრენორფინის უსაფრთხოების გაუმჯობესების შესახებ მიღებულია 1995 წელს ბუპრენორფინის ფართო გამოყენებით საფრანგეთში, რასაც მოჰყვა ოპიოიდური ზედოზირებით სიკვდილიანობის 79%-ით შემცირება [119]. 1994-1998 წლებში ბუპრენორფინის გამოყენებისას სიკვდილიანობის მაჩვენებელი 1.4-ჯერ მეტი იყო მეთადონთან შედარებით, თუმცა უნდა ითქვას, რომ ბუპრენორფინს 14-ჯერ მეტი პაციენტი იღებდა[120].
დაფიქსირებულია სიკვდილიანობის შემთხვევები ბუპრენორფინის სედატიურ ნივთიერებებთან კომბინაციაში მოხმარებისას [121, 122]. სიკვდილიანობის ბუპრენორფინთან დაკავშირებული მაჩვენებელი არის 0.2 1000 პაციენტზე წელიწადში [123], რაც გაცილებით ნაკლებია, ვიდრე არანამკურნალები ჰეროინული დამოკიდებულების დროს [124].
რანდომიზებულ კონტროლირებულ კვლევებში, უსაფრთხოების მონაცემები იშვიათად გროვდება; თუმცა, დადგენილია, რომ ბუპრენორფინის მიღებისას პაციენტები უფრო ხშირად უჩივიან თავის ტკივილს, ხოლო მეთადონის მიღებისას აღენიშნებათ უფრო გამოხატული სედაცია [125]. არსებობს მოსაზრება, რომ ბუპრენორფინის მოხმარებისას ფსიქო-მოტორული ფუნქციები უკეთესია [126, 127]. ვენაში შეყვანისას ბუპრენორფინი აზიანებს ვენებს; ბუპრენორფინის ინექციის გართულებები ხშირად აღინიშნება ინტრავენურ ნარკომანებში [119, 128]. მეთადონი ახანგრძლივებს QT ინტერვალს, დაფიქსირებულია არითმიების განვითარებაც. კლინიკურ კვლევებში ნაჩვენებია, რომ მეთადონის მიერ QT ინტერვალის გახანგრძლივება უმნიშვნელოა; თუმცა, მაინც არსებობს სიცოცხლისათვის საშიში არითმიების განვითარების გაზრდილი რისკი, რაც არ აღინიშნება ბუპრენორფინის მოხმარებისას [129, 130, 131, 132].
ბუპრენორფინის ტაბლეტებს მავნედმოხმარების დიდი პოტენციალი აქვს. იქ, სადაც ბუპრენორფინი ინტრავენურ ნარკომანებში ინიშნებოდა, ყველგან ჩნდებოდა მისი ინტრავენურად გამოყენების ეპიდემია. შედეგად, მკურნალობის სურვილი გამოთქვეს იმ პაციენტებმა, რომლებისთვისაც პირველად მიღებული და ძირითადი ნარკოტიკი იყო ბუპრენორფინი. მართალია, მეთადონის ინექციის შემთხვევებიც აღინიშნება, მაგრამ იშვიათია, განსაკუთრებით, როცა სახლში მისაღებად 200 მლმდე განზავებული დოზა ეძლევა. ამ პრობლემის მოგვარება შეიძლება მეთადონის დოზის ზედამხედველობით მიღების საშუალებით.
ბუპრენორფინის დოზაზე ზედამხედველობა მთლიანად არ ხსნის მავნედმოხმარების რისკს, რადგან რთულია ზედამხედველობა ენისქვეშ მისაღები პრეპარატზე, რომლის გახსნას 15 წუთი სჭირდება. მკურნალობის დროს ბუპრენორფინის არასათანადო გამოყენებამ, ანუ ინტრავენურად შეყვანამ შეიძლება გააღრმავოს დამოკიდებულება, ხელი შეუწყოს სისხლით გადამდები ვირუსების გავრცელებას და სხვა სედატიურ ნივთიერებებთან კომბინირებისას გამოიწვიოს ზედოზირება. ასევე აღწერილია ჰეპატიტის, ლოკალური და სისტემური ინფექციების, ვენების და არტერიების დაზიანების და ინექციებთან დაკავშირებული სხვა პრობლემების შემთხვევები.
ბუპრენორფინთან დაკავშირებული ხშირი გვერდითი მოვლენებია თავის ტკივილი, შეკრულობა, ძილის დარღვევა და აგზნებადობა. არსებული მონაცემებით ბუპრენორფინი არ იძლევა QT ინტერვალის მნიშვნელოვან გახანგრძლივებას.
საერთო ჯამში, მართალია, ბუპრენორფინი უფრო უსაფრთხო მედიკამენტადაა მიჩნეული, მაგრამ ამ სარგებლის გამოთვლის სირთულეს და მისი მავნედმოხმარების და ინტრავენური შეყვანის რისკის არსებობას იმ დასკვნამდე მივყავართ, რომ განსხვავება უსაფრთხოების თვალსაზრისით მკვეთრი არ არის.
ხარჯების ეფექტიანობა
მეთადონის ღირებულება დაახლოებით არის 0.5-1.0 აშშ ცენტი/მგ, ანუ ყოველი ეფექტური დოზა 60 აშშ ცენტიდან 1.20 აშშ დოლარამდე მერყეობს (იხ. შემდეგი ნაწილი). პრეპარატის გაცემასა და ასოცირებულ მკურნალობასთან დაკავშირებული ხარჯები დიდი რესურსების მქონე ქვეყნებში ყოველწლიურად 5000 აშშ დოლარიდან მერყეობს, 500 აშშ დოლარამდე კი - მცირე რესურსების მქონე ქვეყნებში.
ბუპრენორფინის ღირებულება დაახლოებით არის 10 აშშ ცენტიდან 1 აშშ დოლარამდე/მგ. რეკომენდებული დოზის ღირებულება 80 აშშ ცენტიდან 8 აშშ დოლარამდეა (იხ. შემდეგი ნაწილი). მკურნალობის სხვა ხარჯები იგივეა, რაც მეთადონისთვის, როდესაც ბუპრენორფინის მიღება ზედამხედველობით ხდება.
შესწავლილი დოზების მოხმარებისას მეთადონი უფრო იაფი და ეფექტიანი პრეპარატია, ვიდრე ბუპრენორფინი; ამდენად, ხარჯების ეფექტიანობის შედარებისას ამ განხილვაში იგი დომინანტურ ადგილს იკავებს.
შეზღუდული მონაცემები
რადგან როგორც მეთადონით, ისე ბუპრენორფინით დოზაზე დამოკიდებული მკურნალობა ტარდება, ადეკვატური შედარების დროს ყურადღება სწორედ დოზებს უნდა მივაქციოთ. ასევე, ვინაიდან ბუპრენორფინი ნაწილობრივი აგონისტია, რთულია დოზების პირდაპირ მეთადონთან შედარება. ფარმაკოლოგიური მონაცემები მიუთითებს, რომ 6-8 მგ შეიძლება არ იყოს ბუპრენორფინის ოპტიმალური დოზა. ბუპრენორფინის უფრო მაღალი დოზები გაცილებით ეფექტიანი იქნება, რადგან ისინი უფრო დიდხანს მოქმედებს და უფრო შედეგიანია ჰეროინის გამოყენების ეფექტების ბლოკირებაში. ბევრ კვლევას არ ჩაუტარებია განზრახვამკურნალობის ანალიზი და პაციენტებს, რომლებმაც დატოვეს მკურნალობის პროცესი, ჩვეულებრივ, აღარ აკვირდებიან ხოლმე.
მკურნალობის საკითხები
მეთადონის რამდენიმე ფორმა არსებობს - საინექციო, პერორალური ხსნარი და აბი. ოპიოიდური დამოკიდებულების მკურნალობისთვის რეკომენდებულია პერორალური ხსნარის ფორმა, რადგან მის შეყვანაზე ზედამხედველობა უფრო ადვილად შეიძლება; ასევე სახლში მისაღები დოზების შემთხვევაში თუ საკმარისად განზავებულ ხსნარს მივცემთ (მაგ. 200 მლმდე), პრეპარატის ინტრავენური შეყვანის ნაკლები რისკი იქნება.
ბუპრენორფინი სუბლინგვური ტაბლეტია, ყველაზე ხშირად 2 და 8 მგ-იანი აბები გვხვდება. რადგან მისი სრული გახსნისათვის 5-15 წუთია საჭირო, მის მიღებაზე ზედამხედველობა რთულია. დადებითი მხარე ის არის, რომ ხანგრძლივი მოქმედების გამო, პაციენტების ორ მესამედში ბუპრენორფინი შეიძლება დაინიშნოს ყოველ მეორე ან მესამე დღეს, რაც ყოველდღიური ზედამხედველობის აუცილებლობას აგვარიდებს. ამჟამად, ავსტრალიაში, ევროპასა და შეერთებულ შტატებში ხელმისაწვდომია ბუპრენორფინის ნალოქსონთან კომბინირებული ფორმულა თანაფარდობით 4:1 (დამატებითი დისკუსიისათვის იხ. მე-4 დანართი).
როცა პაციენტებს ანამნეზში აღენიშნებათ ბუპრენორფინის ინექცია (უკანონოდ მოპოვებულის, ან გამოწერილის), უპირატესობა უნდა მიენიჭოს მეთადონით შემანარჩუნებელ თერაპიას (ბუპრენორფინთან შედარებით).
სხვა კვლევების და ფუნდამენტური კვლევების შედეგები
მეთადონის ნახევარდაშლის პერიოდი ცვალებადია. პაციენტების მხოლოდ მცირე რაოდენობას აღენიშნება მოხსნის სიმპტომები მეთადონის 24-საათიან დოზებს შორის. [133]. მრავალი მათგანისათვის ბუპრენორფინი შეიძლება უკეთესი არჩევანი იყოს.
დასკვნა
აქამდე ჩატარებულ კვლევებში მეთადონის სტანდარტული დოზები (ბუპრენორფინის სტანდარტულ დოზებთან შედარებით) უფრო ეფექტიანი აღმოჩნდა პაციენტების მკურნალობის პროგრამაში დაყოვნების და ჰეროინის მოხმარების შემცირების მხრივ, თანაც, მეთადონი უფრო იაფიცაა. ეს მონაცემი მიღებულია ჩატარებული კლინიკური კვლევების მეტაანალიზიდან (საშუალო ხარისხის მტკიცებულება); უნდა აღინიშნოს, რომ ბუპრენორფინის უფრო მაღალ დოზებს სხვა შედეგების მოცემა შეუძლია. შესაძლოა, ბუპრენორფინით მკურნალობა უფრო უსაფრთხოდაც მივიჩნიოთ, ვიდრე მეთადონით მკურნალობა, მაგრამ ეს ვარაუდი მეცნიერული კვლევებით არ დადასტურდა. დღესდღეობით, მაღალი ხარისხის მეთადონის გამოყენება ოპტიმალურ მკურნალობადაა მიჩნეული. ბუპრენორფინი რეზერვში უნდა იყოს, როგორც მეორე რიგის პრეპარატი იმ პაციენტებისთვის, რომლებსაც მეთადონის მიღება არ სურთ ან როდესაც მეთადონის გამოყენება მიზანშეწონილი ან ეფექტიანი არ არის. ბუპრენორფინის ინტრავენურად მომხმარებელი პაციენტების მკურნალობისას უპირატესობა მეთადონს უნდა მიენიჭოს (ბუპრენორფინთან შედარებით). ამ დასკვნის მიხედვით, უფრო დიდი მნიშვნელობა აქვს მკურნალობის შედეგს, ვიდრე შესაძლო განსხვავებებს უსაფრთხოების თვალსაზრისით, რადგან არანამკურნალებ ოპიოიდურ დამოკიდებულებას უფრო მაღალი სიკვდილიანობა უკავშირდება.
რეკომენდაცია ოპიოიდური აგონისტებით მხარდამჭერი მკურნალო ბისთვის პაციენტების უმრავლესობას მეთადონის ადეკვატური დოზები უნდა ვურჩიოთ (ბუპრენორფინთან შედარებით). რეკომენდაციის ძალა - ძლიერი მტკიცებულების ხარისხი - მაღალი შენიშვნები - მართალია, ზოგადად, ბუპრენორფინთან შედარებით უპირატესობა მეთადონს ენიჭება, მაგრამ ზოგიერთმა პაციენტმა შესაძლოა ბუპრენორფინი უკეთ აიტანოს. ბუპრენორფინის მოხმარების მიზეზი შეიძლება იყოს წარსულში ბუპრენორფინზე კარგი რეაქცია, მეთადონის მიმართ ეფექტის არარსებობა, მეთადონის მოქმედების მოკლე ვადა (ანუ დოზებს შორის მოხსნის სიმპტომები), მეთადონის და სხვა მედიკამენტის ურთიერთქმედება, მეთადონის სპეციფიკური გვერდითი მოვლენები, მკურნალობის მისაწვდომობა და პაციენტის მიერ უპირატესობის მინიჭება ბუპრენორფინის სუბიექტური ეფექტებისთვის მეთადონთან შედარებით. ბუპრენორფინის არგამოყენების მიზეზებს მიეკუთვნება ანამნეზში ბუპრენორფინის ინტრავენური შეყვანის არსებობა, ბუპრენორფინის სპეციფიკური გვერდითი მოვლენები და ბუპრენორფინით მკურნალობის წარუმატებლობა წარსულში. |
 |
10.3.3 6.3.3 ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის საწყისი დოზები |
▲back to top |
როგორი საწყისი დოზები უნდა იქნეს მიღებული მეთადონის ან ბუპრენორფინის მოხმარებისას?
მეთადონის საწყისი დოზა
მეთადონის საწყისი დოზა უნდა ემყარებოდეს პაციენტის ნეიროადაპტაციის დონის დაკვირვებით შეფასებას. მეთადონით მკურნალობის პირველი ორი კვირა ზედოზირების მაღალი რისკით ხასიათდება, რადგან შეიძლება გართულდეს ნეიროადაპტაციის დონის ზუსტად შეფასება. პაციენტებისათვის, რომლებიც ოპიოიდებს სამედიცინო დანიშნულებით იღებენ, საერთო დღიური დოზა უნდა გადაანგარიშდეს მეთადონის ეკვივალენტურ ერთჯერად დღიურ დოზაზე. მათთვის კი, ვინც უკანონო ოპიოიდებს იღებს (მაგ. ჰეროინი), დღეში 20 მგ მეთადონის დოზა, ჩვეულებრივ, ადეკვატური იქნება აღკვეთის მდგომარეობის სიმპტომების მოსახსნელად და პაციენტების მკურნალობის პროგრამაში დასარჩენად. ამავდროულად, ნაკლები იქნება ოპიოიდების ზედოზირების რისკი.
ნეიროადაპტაციის გაურკვეველი დონის პაციენტებში მკურნალობა უნდა დავიწყოთ მეთადონის დაბალი დოზებით და დავაკვირდეთ. ნეიროადაპტაციის მაღალი დონის ზოგიერთ პაციენტს ჰეროინის მიღების შეწყვეტის და დღეში 20 მგ მეთადონის დანიშვნისას აღენიშნება გარკვეული დისკომფორტი. მკურნალობის პროგრამაში დასარჩენად ამ ჯგუფში რეკომენდებულია უფრო მაღალი დოზები (30 მგ-მდე). ყურადღება უნდა მივაქციოთ, რომ არ მოხდეს ნეიროადაპტაციის ზედმეტად შეფასება და ზედოზირება. უფრო უსაფრთხო, მაგრამ უფრო შრომატევადი სტრატეგიაა საწყისი უსაფრთხო დოზის მიცემა და პაციენტის შეფასება რამდენიმე საათის შემდეგ დოზაზე რეაგირების სანახავად, რის საფუძველზეც ხდება შემდეგი დღის დოზის დარეგულირება და, თუ საჭიროა, დოზის გაზრდა.
მას შემდეგ, რაც დადგინდება, რომ პაციენტი კარგად იტანს საწყის დოზას, მეთადონის დოზა თანდათან უნდა გაიზარდოს, ვიდრე პაციენტი თავს კომფორტულად იგრძნობს ჰეროინის და სხვა უკანონო ოპიოიდების გამოყენების გარეშე. ზრდის სიჩქარე ინდივიდუალურად უნდა დადგინდეს და არ უნდა აჭარბებდეს 10 მგ-ს რამდენიმე დღეში.
რეკომენდაცია მეთადონით მკურნალობის დროს საწყისი ყოვედღიური დოზა დამოკიდებული უნდა იყოს ნეიროადაპტაციის დონეზე; ზოგადად, დოზა არ უნდა იყოს 20 მგ-ზე მეტი და არც ერთ შემთხვევაში არ უნდა აღემატებოდეს 30 მგ-ს.
|
ბუპრენორფინის საწყისი დოზა
ბუპრენორფინით მკურნალობის დაწყებისას მცირეა ზედოზირების რისკი. თუმცა, ნეიროადაპტაციის მაღალი დონის მქონე პაციენტებს ბუპრენორფინმა შეიძლება დაუჩქაროს აღკვეთის მდგომარეობის სიმპტომების განვითარება. ამგვარ პაციენტებში შეიძლება მიზანშეწონილი იყოს დაბალი დოზებით დაწყება (2 მგ). ამასთანავე, პაციენტები უნდა დაელოდონ მსუბუქი აღკვეთის მდგომარეობის სიმპტომების განვითარებას და მაშინვე არ უნდა მიიღონ ბუპრენორფინის პირველი დოზა (სულ ცოტა, 12 საათი ჰეროინის ან სხვა ხანმოკლე მოქმედების ოპიოიდის მიღებიდან), რათა შენელდეს ბუპრენორფინით აღკვეთის მდგომარეობის სიმპტომების განვითარების პროცესი. ზოგადად, საშუალო დონის ნეიროადაპტაციის მქონე პაციენტები კარგად იტანენ 4-8 მგ საწყის დოზებს დღეში ერთხელ.
მას შემდეგ, რაც დადგინდება, რომ საწყისი დოზა მარტივად გადასატანია, ბუპრენორფინის დოზა შეიძლება საკმაოდ სწრაფად გაიზარდოს იმ დოზამდე, რომელიც სტაბილურ ეფექტებს უზრუნველყოფს 24 საათის განმავლობაში და კლინიკურად ეფექტიანია.
 |
10.3.4 6.3.4 ფიქსირებული ან თავისუფალი დოზირება აგონისტებით მხარდამჭერი მკურნალობის დროს |
▲back to top |
როგორი უნდა იყოს მეთადონის და ბუპრენორფინის დოზები - ფიქსირებული თუ ინდივიდუალურად მორგებული?
ვერ მოიძებნა კვლევა, სადაც შედარებული იქნებოდა ფიქსირებული და თავისუფალი დოზები მეთადონით და ბუპრენორფინით მკურნალობისას. თავისუფალი დოზების გამოყენებას ის უპირატესობა აქვს, რომ გათვალისწინებულია შეწოვის და მეტაბოლიზმის ინდივიდუალური თავისებურებები და დოზასთან დაკავშირებული განსხვავებები, რაც გავლენას ახდენს კლინიკურ შედეგზე. საზოგადოდ, მეთადონის და ბუპრენორფინის დოზა მანამდე უნდა გაიზარდოს, ვიდრე არ შეწყდება უკანონო ოპიოიდების მოსმარება. ამის შემდეგ, დოზა ხშირად უნდა შემოწმდეს, პაციენტს არ უნდა მივცეთ საშუალება, ყურადღება ზედმეტად დააფიქსიროს დოზის მინიმალურ ცვლილებაზე. მეთადონის დოზა უფრო ხშირად უნდა გადაიხედოს მკურნალობის დაწყებისას და დოზის ზრდისას, ასევე დოზის გამოტოვების და შემცირებისას. ჩვეულებრივ, მკურნალობის მხარდამჭერ ფაზაში პაციენტები, სულ ცოტა, თვეში ერთხელ უნდა გამოვიკვლიოთ.
 |
10.3.5 6.3.5 მეთადონის მხარდამჭერი დოზები |
▲back to top |
როგორი უნდა იყოს მეთადონის და ბუპრენორფინის მხარდამჭერი დოზები?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.5 |
არსებობს საშუალო ხარისხის მონაცემი, რომ მეთადონის დიდი დოზები (>60 მგ) (უფრო დაბალ დოზებთან შედარებით (<40 მგ)) დაკავშირებულია პაციენტის მკურნალობის პროგრამაში დაყოვნების გაუმჯობესებასთან და ჰეროინის ნაკლებ მოხმარებასთან. სამედიცინო პერსონალმა უნდა დანიშნოს მეთადონის ეფექტიანი დოზა და მზად იყოს დოზის გასაზრდელად, თუ პაციენტი ისევ იყენებს აკრძალულ ოპიოიდებს. მეტადონის ფიქსირებულ დოზაზე ჩატარებული კვლევები დაიყო ჯგუფებად, სადაც შედარებულ იქნა დოზები 1-39, 40-59, 60-109 და 109 მგ.-ზე მაღალი (ამ ბოლო კატეგორიაში პაციენტები იღებდნენ 160 მგ-ს).
ეფექტიანობა
60-109 მგ 1-39 მგ-თან შედარებით
1-39 მგ დოზის დიაპაზონთან შედარებით 60-109 მგ დოზა უკეთესი იყო პაციენტის მკურნალობის პროგრამაში დაყოვნების თვალსაზრისით (RR 1.36, 95%-ი CI 1.13-1.63, მაღალი ხარისხის მტკიცებულება) და ჰქონდა ოპიოიდების მოხმარების შეწყვეტის უფრო მაღალი მაჩვენებელი (RR 1.59, 95%-ი CI 1.16-2.18, დაბალი ხარისხის მტკიცებულება); ასევე, მცირდება კოკაინის მოხმარებაც (RR 1.81, 95%-ი CI 1.15-2.85, საშუალო ხარისხის მტკიცებულება).
60-109 მგ 40-59 მგ-სთან შედარებით
40-59 მგ-სთან შედარებით 60-109 მგ დოზა დაკავშირებულია ხანგრძლივი პერიოდის განმავლობაში მკურნალობის პროგრამაში დაყოვნების გაუმჯობესებასთან (RR 1.23, 95%-ი CI 1.05-1.45, მაღალი ხარისხის მტკიცებულება) და ჰეროინის მოხმარების შემცირებასთან. სტატისტიკურად მნიშვნელოვანი მონაცემი არ მოიპოვება (RR 1.51, 95%-ი CI 0.63-3.61, დაბალი ხარისხის მტკიცებულება).
40-59 მგ 1-39 მგ-სთან შედარებით
მკურნალობის პროგრამაში დაყოვნების თვალსაზრისით საშუალო (40-59 მგ) და დაბალ დოზებს (1-39 მგ) შორის მნიშვნელოვანი განსხვავება არ არის (RR 1.26, 95%-ი CI 0.91-1.75, საშუალო დოზის სასარგებლოდ, საშუალო ხარისხის მტკიცებულება).
109 მგ-ზე მაღალი დოზები
60-109 მგ დოზებთან შედარებით 160 მგ დღეში არ იყო დაკავშირებული მკურნალობის პროგრამაში დაყოვნების გაუმჯობესებასთან (RR 0.96, 95%-ი CI 0.69-1.34, დაბალი ხარისხის მტკიცებულება), თუმცა ეს მაღალი დოზა მკურნალობის პროგრამაში დაყოვნების გაუმჯობესებას იწვევს 60 მგ-ზე ნაკლებ დოზასთან შედარებით (RR 1.67, 95%-ი CI 1.05-2.66).
არარანდომიზებული კვლევები
ბევრ არარანდომიზებულ კვლევაში პაციენტებს უკეთესი შედეგები აქვთ მეთადონის მაღალი დოზების მიღებისას [134, 135, 136, 137, 138,139].
უსაფრთხოება
მეთადონის მაღალი დოზები შეიძლება დაკავშირებული იყოს QT ინტერვალის გახანგრძლივების გაზრდილ რისკთან. QT-ინტერვალთან დაკავშირებული გვერდითი მოვლენების ზუსტი რისკის განსაზღვრა რთულია, მაგრამ სავარაუდოდ, უფრო ნაკლებია მეთადონის მაღალი დოზებით მიღებულ სარგებელთან შედარებით. ამ მოსაზრებას ამყარებს ის, რომ მეთადონის მაღალ დოზებზე მყოფი პაციენტების სიკვდილიანობის რისკი მცირდება [140].
ხარჯების ეფექტიანობა
ვერ მოიძებნა კვლევები, სადაც შედარებული იქნებოდა მეთადონის დაბალი და მაღალი დოზების ხარჯების ეფექტიანობა. რესურსებით მდიდარ ქვეყნებში მეთადონის ღირებულება მკურნალობის საერთო ღირებულების მცირე ნაწილს წარმოადგენს და მეთადონის მაღალი დოზა, სავარაუდოდ, გაზრდის მისი ხარჯების ეფექტიანობას. რესურსებით ნაკლებად მდიდარ ქვეყნებში სიტუაცია ნაკლებად გარკვეულია. თუმცა, თუ მეთადონის ნებისმიერი დოზის პირობებში ჰეროინის გამოყენება გრძელდება, მეთადონის დოზის გაზრდა ხარჯების თვალსაზრისით ყველა შემთხვევაში ეფექტიანი იქნება.
შეზღუდული მონაცემები
ამ საკითხთან დაკავშირებით სარწმუნო მტკიცებულებები არ არსებობს. უფრო ზუსტად, ნაკლებია კონტროლირებული რანდომიზებული კვლევები მეთადონის დოზების შესახებ. მიუსედავად იმისა, რომ არარანდომიზებული კვლევების შედეგების მიხედვით მჭიდრო ასოციაცია არსებობს მეთადონის მაღალ დოზებსა და კარგ კლინიკურ გამოსავალს შორის, ეს მონაცემი შეიძლება მიკერძოებული იყოს - პაციენტები, რომლებიც მეთადონით მკურნალობას ემორჩილებიან, უფრო დიდხანს რჩებიან პროგრამაში და უფრო მაღალ დოზებს იღებენ, ვიდრე ის პაციენტები, რომლებიც არ ემორჩილებიან მეთადონით მკურნალობას.
მკურნალობის საკითხები
კლინიკურ პრაქტიკაში დოზების შერჩევა ინდივიდუალურად ხდება, რაც დამყარებულია ჰეროინის მოცემულ დოზაზე, აღკვეთის მდგომარეობის სიმპტომებზე დოზებს შორის და გვერდით მოვლენებზე. ფარმაკოკინეტიკური კვლევები მიუთითებს მნიშვნელოვან განსხვავებებზე მეთადონის აბსორბციისა და მეტაბოლიზმის პროცესებში. ამის გათვალისწინებით, მეთადონის დოზის განსაზღვრა მისი მიღებიდან 24 საათის შემდეგ უფრო აზუსტებს აქტიურ დოზას. ზოგიერთი პაციენტის ადეკვატური მკურნალობა შესაძლებელია მცირე დოზებით; სხვებს შეიძლება დაგეგმილი დოზის დიაპაზონზე მაღალი დოზა დასჭირდეთ.
დასკვნა
დოზები, რომლებიც მოქცეულია 60-109 მგ ფარგლებში, უფრო ეფექტიანია, ვიდრე უფრო დაბალი დოზები. კლინიცისტებმა, ზოგადად, დოზის ამ დიაპაზონში უნდა იმუშაონ. მათ უნდა დაარწმუნონ პაციენტები, რომ გამოიყენონ ეს მაღალი დოზები და არ შეამცირონ ის, განსაკუთრებით, თუ ისინი ჯერ კიდევ იყენებენ აკრძალულ ოპიოიდებს.
რეკომენდაცია საშუალოდ, მეთადონის მხარდამჭერი დოზა დღეში უნდა იყოს 60-120 მგ-ის ფარგლებში. რეკომენდაციის ძალა - |
 |
10.3.6 6.3.6 ბუპრენორფინის მხარდამჭერი დოზები |
▲back to top |
ეფექტიანობა
სისტემატური კვლევები ბუპრენორფინის სხვადასხვა დოზების ეფექტიანობის შესახებ ვერ მოიძებნა. რანდომიზებულ კვლევებში, რომლებშიც დოზების შედარება მოხდა, აღმოჩნდა, რომ 6 მგ ბუპრენორფინი ჰეროინის უფრო ნაკლებ მოხმრებას უკავშირდებოდა, ვიდრე 2 მგ. [141]. 8 მგ ბუპრენორფინი დღეში უფრო მეტად უწყობს ხელს პაციენტის მკურნალობის პროგრამაში დარჩენას, ვიდრე 3 მგ/დღეში [142], 12 მგ/დღეში კი, 4 მგ-სთან შედარებით, დაკავშირებულია ჰეროინის ნაკლებ მოხმარებასთან [143]. ორმა კვლევამ, რომლებშიც მაღალი დოზები გამოიყენებოდა, აჩვენა ტენდენცია (არც ერთ კვლევაში არ იყო სტატისტიკურად მნიშვნელოვანი მონაცემები), რომ 16 მგ დღეში უფრო ეფექტიანია, ვიდრე 8 მგ. [110, 144].
უსაფრთხოება
ბუპრენორფინის დოზებს საფრთხის რისკი არ უკავშირდება. თუმცა, რანდომიზებული კონტროლირებული კვლევის მიხედვით, ბუპრენორფინის მაღალ დოზებზე მყოფ პაციენტებში შეიძლება მოიმატოს ალანინამინოტრანსფერაზას (ალტ) და ასპარტატამინოტრანსფერაზას (ასტ) დონემ.
ხარჯების ეფექტიანობა
ამ მიმოხილვის დროს, ვერ მოიძებნა კვლევა, სადაც შეფასებული იქნებოდა ბუპრენორფინის სხვადასხვა დოზების ხარჯების ეფექტიანობა. ბუპრენორფინით მკურნალობის დროს მისი ღირებულება მნიშვნელოვანი კომპონენტია და, მიუხედავად იმისა, რომ, სავარაუდოდ, მაღალი დოზები უფრო შედეგიანია, ხარჯების ეფექტიანობა განსაზღვრული არ არის.
შეზღუდული მონაცემები
მწირია მონაცემები, სადაც დაბალი დოზები 6 მგ-ზე მაღალ დოზებთანაა შედარებული.
სხვა მონაცემები
ბუპრენორფინის მაღალი დოზები (16-32 მგ) უკეთესად ბლოკავს ჰეროინის დამატებით ეფექტებს, ვიდრე უფრო დაბალი დოზები [145, 146, 147, 148, 149, 150] და მოქმედებს უფრო ხანგრძლივად მნიშვნელოვანი სედაციის გამოწვევის გარეშე.
დასკვნა
მართალია, მტკიცებულებების ხარისხი დაბალია, მაგრამ, სავარაუდოდ, მაღალი დოზები (დაბალ დოზებთან შედარებით) დაკავშირებულია მკურნალობის პროგრამაში დაყოვნების უკეთეს მაჩვენებელთან და ჰეროინის ნაკლებ მოხმარებასთან. დოზის გაზრდას, ღირებულების გარდა, სხვა უარყოფითი შედეგი პრაქტიკულად არ აქვს. საშუალოდ, დოზა უნდა იყოს დღეში, სულ ცოტა, 8 მგ. თუ პაციენტი კვლავ მოიხმარს აკრძალულ ოპიოიდებს, უნდა განვიხილოთ დოზის 4-8 მგ-ით მომატების საკითხი მაქსიმალურ დოზამდე - 32 მგ დღეში.
რეკომენდაცია საშუალოდ, ბუპრენორფინის მხარდამჭერი დოზა დღეში უნდა იყოს, სულ მცირე, 8 მგ. რეკომენდაციის ძალა - სტანდარტული მტკიცებულების ხარისხი - მაღალი |
 |
10.3.7 6.3.7 ზედამხედველობა დოზირებაზე ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის დროს |
▲back to top |
საჭიროა თუ არა ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის დოზებზე ზედამხედველობა?
ძალიან ცოტაა სისტემატიზებული კვლევები ოპიოიდური აგონისტებით მხარდამჭერი თერაპიის დოზების ზედამხედველობაზე. ყველა კლინიკურ კვლევაში, რომლებშიც ნაჩვენებია მეთადონის და ბუპრენორფინის ეფექტიანობა და უსაფრთხოება (პლაცებოსთან ან ოპიოიდების მოხსნასთან შედარებით), მხარდამჭერი თერაპია ტარდებოდა დოზაზე ზედამხედველობით. ასევე, დოზაზე ზედამხედველობა გამოიყენებოდა კვლევებში, სადაც ერთმანეთს ადარებდნენ მეთადონს და ბუპრენორფინს. ზოგიერთ ქვეყანაში, რომელთა შორის აღსანიშნავია საფრანგეთი, მიღებულია ბუპრენორფინით მკურნალობა დოზაზე ზედამხედველობის გარეშე. ზოგიერთში კი მეთადონზე მყოფ სტაბილურ პაციენტებში მიღებულია შედარებით იშვიათი ზედამხედველობა დოზაზე (დოზის გაცემა ხდება კვირაში ერთხელ ან უფრო იშვიათად). ზედამხედველობის არარსებობის გარეშე აღინიშნება როგორც მეთადონის, ისე ბუპრენორფინის არადანიშნულებისამებრ გამოყენება. თუმცა, ბუპრენორფინის ინტრავენური შეყვანა მეთადონთან შედარებით გაცილებით უფრო ხშირია ნალოქსონთან კომბინირების დროსაც კი [151].
ეს შესაძლებელია გამოწვეული იყოს მრავალი ფაქტორით:
ინტრავენური შეყვანისათვის უპირატესობას ანიჭებენ ბუპრენორფინს, რადგან იგი დაბალი დოზებითაც კი უფრო ძლიერ ეფექტებს იწვევს. ამის გამო, არსებობენ ადამიანები, რომლებისთვისაც ბუპრენორფინი პირველი და ძირითადი ნარკოტიკია.
ბუპრენორფინის დოზის შემცირებისას აღკვეთის მდგომარეობის სიმპტომები უფრო მსუბუქია, რაც ნიშნავს, რომ პაციენტს შეუძლია, ბუპრენორფინის დოზის ნაწილი გამოიყენოს არადანიშნულებისამებრ ისე, რომ არ განუვითარდეს ძლიერი აღკვეთის მდგომარეობა.
ბუპრენორფინზე ეფექტიანი ზედამხედველობა რთულია, რადგან მისი მიღება ხდება ენისქვეშ და გახსნას 5-15 წუთი სჭირდება. მეთადონი კი პაციენტმა უნდა გადაყლაპოს.
მეთადონის არადანიშნულებისამებრ გამოყენება რთულდება დოზის ზედამხედველობით მიღებისას ან თუ სახლში მისაღებ დოზას განზავებული სახით გავატანთ (200 მლ). ამ დროს ინტრავენური შეყვანა იშვიათია. მეთადონი ხანგრძლივად მოქმედი პრეპარატია, რაც მის რეგულარულ ინტრავენურ მოხმარებას ნაკლებად სასურველს ხდის. ადამიანები, რომლებიც მეთადონს უკანონოდ ყიდულობენ, ჩვეულებრივ მას თვითმკურნალობისთვის [152] იყენებენ.
მონაცემები არადანიშნულებით გამოყენების და დოზის გადაჭარბებით სიკვდილიანობის შესახებ მიუთითებს, რომ მეთადონის მიცემა ზედამხედველობის გარეშე სარისკოა, რადგან მას შეუძლია გამოიწვიოს იმ ადამიანების სიკვდილი, რომლებსაც ის დანიშნული არ აქვთ [153]. მეორე მხრივ, არადანიშნულებით გამოყენებულ ბუპრენორფინს სიკვდილის გამოწვევა ნაკლებად შეუძლია (თუმცა, სიკვდილის შემთხვევები დაფიქსირებულია სხვა სედატიურ საშუალებებთან კომბინაციისას), მაგრამ, მისი ინტრავენურად შეყვანის გაცილებით დიდი რისკი არსებობს. ბუპრენორფინის არადანიშნულებით გამოყენების მთავარი პრობლემა იმ ადამიანების ჯგუფის შექმნაა, რომლებიც უპირატესად დამოკიდებულნი არიან ბუპრენორფინის უკანონო მოხმარებაზე. ასეთ ინდივიდებს ექმნებათ ნარკოტიკების ინტრავენურ გამოყენებასთან დაკავშირებული პრობლემები - C ჰეპატიტი, აივ ინფექცია, ენდოკარდიტი და ადგილობრივი ინფექციები. ადვილი არ არის იმის შეფასება, გარკვეული სარგებელის მატარებელი თუ საზიანოა არადანიშნულებისამებრ გამოყენებული ბუპრენორფინის ეპიდემია, რადგან მას ჰეროინის გამოყენების შემცირება შეუძლია; თუმცა, ეს ბევრ ქვეყანაში მიუღებელია, რადგან ემუქრება ნარკომანიის მკურნალობის არსებული სისტემის სიცოცხლისუნარიანობას.
ყოველივე ჩამოთვლილი ქმნის არგუმენტებს საზოგადოებრივი ჯანდაცვისთვის მკურნალობაზე ზედამხედველობის დასაწესებლად. მეორე მხრივ, ზედამხედველობის გარეშე მკურნალობის სისტემა ადვილი ასაწყობია და მისი გაფართოებაც მარტივია, რაც მნიშვნელოვანი პრიორიტეტია ბევრ რეგიონში, სადაც ინტრავენულ ნარკომანებში აივ ინფექცია დიდი პრობლემაა და მკურნალობის არსებული მასშტაბები ძალიან მცირეა. ბუპრენორფინით ზედამხედველობის გარეშე მკურნალობის სწრაფი გაფართოება ყველაზე ადვილი გზაა მკურნალობაზე მოთხოვნილების მოკლე ხანში დასაკმაყოფილებლად [154]. თუმცა, გაურკვეველია, ბუპრენორფინით მკურნალობა ზედამხედველობის გარეშე (ამასთან დაკავშირებული იმგვარი პრობლემით, როგორიცაა ბუპრენორფინის ინტრავენური შეყვანა) ნამდვილად შეძლებს თუ არა აივ ინფექციის გავრცელების შემცირებას ისე, როგორც ეს მეთადონით ზედამხედველობით მკურნალობისას ხდება.
უნდა გავითვალისწინოთ მკურნალობაზე ზედამხედველობის გავლენა თავად პაციენტებზე. ოპიოიდური დამოკიდებულება მოიცავს ოპიოიდების მოხმარებაზე კონტროლის არქონას; ამდენად, არსებობს სარწმუნო თეორიული მიზეზები, თუ პაციენტისთვის რატომაა უპირატესობა მეთადონზე და ბუპრენორფინზე ზედამხედველობა, განსაკუთრებით, მკურნალობის ადრეულ ეტაპზე. სამწუხაროდ, ამ საკითხთან დაკავშირებით კლინიკური კვლევის მონაცემები საკმარისი არ არის. კვლევები ძირითადად კონცენტრირებულია პაციენტებზე, რომლებიც გარკვეული პერიოდის განმავლობაში იტარებენ მკურნალობას. ეს კვლევები აფასებს ზედამხედველობის გარეშე მკურნალობის გავლენას პაციენტებზე, რომლებიც სტაბილურობის გარკვულ კრიტერიუმებს აკმაყოფილებენ. ამგვარ სიტუაციაში, რანდომიზებული კონტროლირე ბული კვლევები გვიჩვენებს, რომ აკრძალული პრეპარატის მიღების შეწყვეტის შემდეგ, პაციენტების გარკვეული ნაწილის გადაყვანა ზედამხედველობის გარეშე მკურნალობაზე დაკავშირებულია აკრძალული ოპიოიდების მოხმარების შემცირებასთან.
ბალანსის დასაცავად მიზანშეწონილია მკურნალობის დაწყება ზედამხედველობით, შემდეგ მკურნალობაზე პასუხის შეფასება და სტაბილური პაციენტებისთვის დოზების თანდათან, ზედამხედველობის გარეშე მიცემა. ამგვარი მიდგომით მნიშვნელოვნად მცირდება პრეპარატის არასათანადო გამოყენება, არ იკლებს ეფექტიანობა და მკურნალობა დადებითად ფასდება პაციენტის მიერ.
„სტაბილურობის“ მთავარი ელემენტები მოიცავს საცხოვრებლის, სამსახურის ქონას, რამდენიმე პრეპარატზე დამოკიდებულების არქონას და მკურნალობის დაწყების შემდეგ ნარკოტიკების ინტრავენური მოხმარების შეწყვეტას.
არსებობს აზრი, რომ რადგან ბუპრენორფინს, მეთადონთან შედარებით, ნაკლებად ახლავს ზედოზირების რისკი და რადგან დოზების მიცემა ზედამხედველობის გარეშე უფრო იაფი და მარტივია, იმ რეგიონებში, სადაც ოპიოიდური აგონისტებით მკურნალობა ამჟამად ხელმისაწვდომი არ არის, ყველაზე დიდი სარგებელი საზოგადოებრივი ჯანდაცვისთვის ბუპრენორფინის დოზებზე ზედამხედველობის გარეშე შეტანა იქნება. დღესდღეობით არსებული მონაცემების საფუძველზე შეუძლებელია მტკიცე დასკვნების მიღება და შეთავაზებების გაკეთება. მკურნალობის ხელმისაწვდომობის (მათ შორის ფინანსური) და პაციენტისგან მისი მიმღებლობის გაზრდის პოტენციური სარგებელი გაწონასწორებული უნდა იყოს ნაკლებად ეფექტიანი მკურნალობის, ბუპრენორფინის უკანონო ბაზრის შექმნის და საზოგადოებაში პოტენციური ანტაგონიზმის რისკებთან.
პრაქტიკული საკითხები
მეთადონის დოზაზე ზედამხედველობა მოიცავს მეთადონის თხევადი დოზის გაცემას სუფთა ჭიქით. სითხის მიღებას უშუალოდ აკვირდება ექთანი, ფარმაცევტი, ან ექიმი. მეთადონის მიღების შემდეგ მიზანშეწონილია პაციენტთან გასაუბრება იმაში დასარწმუნებლად, რომ მან ეს დოზა ნამდვილად მიიღო.
ბუპრენორფინზე ზედამხედველობა უფრო რთულია, რადგან ადვილად შეიძლება აბის ნატეხის პირში შენახვა - აბის გახსნას პირის ღრუში 15 წუთი სჭირდება. ტაბლეტი უნდა გაიცეს სუფთა კონტეინერით, მოთავსდეს პაციენტის პირის ღრუში ენის ქვეშ. პერიოდულად უნდა მოხდეს ტაბლეტის შემოწმება გახსნის სხვადასხვა ეტაპზე.
თუ რაიმე მიზეზის გამო საჭირო აღარ არის, ზედამხედველობის გარეშე გაცემული და გამოუყენებელი დოზები უნდა დაბრუნდეს იმ ადგილას, საიდანაც გაიცა.
დასკვნა
ბალანსის დასაცავად მიზანშეწონილია მკურნალობის ზედამხედველობით დაწყება, შემდეგ მკურნალობაზე პასუხის შეფასება და სტაბილური პაციენტებისთვის დოზების თანდათან, ზედამხედველობის გარეშე მიცემა. ამგვარი მიდგომით მნიშვნელოვნად მცირდება პრეპარატის არასათანადო გამოყენება, არ იკლებს ეფექტიანობა და მკურნალობა დადებითად ფასდება პაციენტის მიერ.
მეთადონის და ბუპრენორფინის დოზაზე რუტინული ზედამხედველობა რეკომენდებულია ყველა პაციენტისთვის, გარდა იმ პაციენტებისა, რომლებიც სახლში მისაღები დოზისთვის საჭირო კრიტერიუმებს აკმაყოფილებენ. ეს კრიტერიუმები შემუშავებულია რეგიონის ან ქვეყნის დონეზე.
რეკომენდაცია მკურნალობის ადრეულ ეტაპზე საჭიროა მეთადონის და ბუპრენორფინის დოზებზე უშუალო ზედამხედველობა. რეკომენდაციის ძალა - მყარი მტკიცებულების ხარისხი - ძალიან დაბალი რეკომენდაცია სახლში მისაღები დოზები უნდა მიეცეს პაციენტს, თუ მისი კლინიკაში მოსვლის სიხშირის შემცირებით მიღებული სარგებელი გადაწონის ამ პრეპარატის არადანიშნულებისამებრ გამოყენების რისკს. პერიოდულად უნდა მოხდეს ამ რისკის შემოწმება. რეკომენდაციის ძალა - სტანდარტული მტკიცებულების ხარისხი - ძალიან დაბალი |
 |
10.3.8 6.3.8 ოპიოიდური აგონისტებით მკურნალობის ოპტიმალური ხანგრძლივობა |
▲back to top |
როგორია ოპიოიდური აგონისტებით მკურნალობის ოპტიმალური ხანგრძლივობა?
ოპიოიდური აგონისტებით მკურნალობის ოპტიმალური ხანგრძლივობის შესახებ კვლევები ნაკლებად არის ჩატარებული. კვლევები, რომლებშიც ოპიოიდური აგონისტებით ხანმოკლე მკურნალობა (ანუ რამდენიმე კვირიდან რამდენიმე თვემდე) შედარებულია უფრო ხანგრძლივ მკურნალობასთან, გვიჩვენებს, რომ ხანგრძლივ მკურნალობას უკეთესი შედეგები აქვს. ეს გასაგებიცაა, რადგან ოპიოიდური დამოკიდებულება ხანგრძლივად მიმდინარე დაავადებაა.
კონტროლირებული რანდომიზებული კვლევები, რომლებშიც შედარებული იქნება ხანგრძლივი მკურნალობის პროგრამები, ვერ მოიძებნა. დაკვირვების საფუძველზე ჩატარებულმა კვლევებმა აჩვენა, რომ პაციენტებს, რომლებიც ოპიოიდური აგონისტებით ხანგრძლივ მკურნალობას გადიან, გადარჩენის მეტი ალბათობა აქვთ, ვიდრე მათ, რომლებიც არ არიან ხანგრძლივ მკურნალობაზე. ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის შეწყვეტა დაკავშირებულია ოპიოიდების მოხმარების განახლების რისკთან. ამ მონაცემების გათვალისწინებით მოცემული სახელმძღვანელო რეკომენდაციას უწევს ოპიოიდური აგონისტებით განუსაზღვრელი დროით მკურნალობას, იმდენ ხანს, რამდენ ხანსაც კლინიკურად არის ნაჩვენები. პაციენტმა და კლინიკის პერსონალმა ადვილად არ უნდა გადაწყვიტოს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის შეწყვეტა (მაგ. ადმინისტრაციული მიზეზებით). ფაქტორები, რომლებიც მიუთითებს ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის ეფექტიან დასრულებაზე, კარგად არ არის აღწერილი, მაგრამ სავარაუდოდ, მოიცავს ოპიოიდური აგონისტებით მკურნალობის დაწყების შემდეგ დასაქმებას ან სხვა მიზნობრივ აქტივობას, ოპიოიდებისგან და სხვა ნარკოტიკებისგან თავშეკავებას და ცვლილებებს ფსიქოსოციალურ გარემოში.
პრაქტიკული საკითხები
ოპიოიდებით ჩანაცვლებითი თერაპიის შეწყვეტის გადაწყვეტილების მიღება რთულია პაციენტისთვის და ის ყოველთვის ეძებს დახმარებას მკურნალი პერსონალისგან. მეორე მხრივ, ზოგიერთი პაციენტი, უბრალოდ, იღებს გადაწყვეტილებას, რომ უნდა შეწყვიტოს ოპიოიდური აგონისტებით მკურნალობა. ორივე სიტუაციაში პაციენტს უნდა გავაცნოთ მკურნალობის შეწყვეტასთან დაკავშირებული რისკები და დავეხმაროთ გონივრული გადაწყვეტილების მიღებაში. პაციენტებში, რომლებიც თავს კარგად გრძნობენ ოპიოიდებით ჩანაცვლებითი მკურნალობის ფონზე, შეიძლება განვიხილოთ სახლში მისაღები დოზების გაზრდის საკითხი, როგორც მკურნალობის შეწყვეტის ალტერნატივა.
6.3.9 ფსიქოსოციალური ჩარევის გამოყენება მხარდამჭერი მკურნალობის დროს
საჭიროა თუ არა ფსიქოსოციალური მკურნალობის გამოყენება ფარმაკოლოგიურ მხარდამჭერ მკურნალობასთან ერთად?
მონაცემები იხ. 1-ლ დანართში, ნაწილი A1.12 |
ეფექტიანობა
კოქრეინის ლაბორატორიის ბოლო მიმოხილვამ გამოავლინა რვა რანდომიზებული კონტროლირებული კვლევა, რომლებმაც შეისწავლეს, უნდა იყოს თუ არა გამოყენებული ფსიქოსოციალური დახმარება ფარმაკოლოგიურ ჩანაცვლებით თერაპიასთან ერთად. როდესაც ერთმანეთს შეადარეს მეთადონის ფსიქოსოციალურ დახმარებასთან კომბინირებული მკურნალობა მხოლოდ მეთადონით მკურნალობას, ანალიზმა აჩვენა, რომ მკურნალობის პროგრამაში დაყოვნების მხრივ განსხვავება არ იყო (RR 0.69, 95%-ი CI 0.53-0.91, მაღალი ხარისხის მტკიცებულება).
ხარჯების ეფექტიანობა
ხარჯების ეფექტიანობის კვლევებმა შეერთებულ შტატებში აჩვენა, რომ მეთადონი საშუალო ინტენსივობის ფსიქოსოციალურ დახმარებასთან ერთად (1-2 საათი კვირაში) ხარჯების მხრივ უფრო ეფექტიანი იყო, ვიდრე მეთადონი ფსიქოსოციალური დახმარების გარეშე ან მაღალი ინტენსივობის დახმარებასთან ერთად (მაგ. რამდენიმე საათი დღეში) [155, 156, 157].
შეზღუდული მონაცემები
კვლევებში გამოყენებული იყო სხვადასხვა ტექნიკა, მათ შორის, ჰიპნოთერაპია, ფსიქოთერაპია, მიმღებლობის და პასუხისმგებლობის განვითარება, ინტერპერსონალური ფსიქოთერაპია, დამხმარე ექსპრესიული ფსიქოთერაპია, კონსულტაცია, კოგნიტური ქცევითი თერაპია, გაუთვალისწინებელი სიტუაციების მართვა, დიალექტური ქცევითი თერაპია და განმარტებითი თერაპია. მეტაანალიზში ამ ჩარევების შედარება რთულია. გაუთვალისწინებელი სიტუაციების მართვის კვლევებს ყველაზე ხშირად აქვს დადებითი შედეგები, მიუხედავად იმისა, თუ რა იქნა გამოყენებული: ვაუჩერები, სახლში მისაღები მეთადონის პრივილეგია თუ საჩუქარი. ნათელი არ არის, შესაძლებელია თუ არა ამ ჩარევების განზოგადება იმ კონკრეტული სიტუაციების გარეთ, სადაც ისინი ჩატარდა (ძირითადად შეერთებულ შტატებში).
დასკვნა
ფსიქოსოციალურმა დახმარებამ მეთადონით ჩანაცვლების დროს მკურნალობის პროცესში შეიძლება შეამციროს ჰეროინის მოხმარება. შეერთებულ შტატებში, ხარჯების მხრივ, ასეთი სერვისი უფრო ეფექტიანია, თუ იგი საშუალო ინტენსივობით გამოიყენება (1-2 საათი კვირაში).
რეკომენდაცია ფსიქოსოციალური დახმარება რუტინულად უნდა შევთავაზოთ ოპიოიდური დამოკიდებულების ფარმაკოლოგიურ მკურნალობასთან ერთად.
|
 |
10.4 6.4 ოპიოიდური აღკვეთის სინდრომის მკურნალობა |
▲back to top |
მიუხედავად სერიოზული დისკომფორტისა, ოპიოიდური აღკვეთის სინდრომი იშვიათად არის სიცოცხლისათვის საშიში; ოპიოიდების მოხსნა, ფარმაკოლოგიურ დახმარებასთან ერთად, უფრო კომფორტულს ხდის ოპიოიდების მოხსნის შემდგომ მდგომარეობას და წარმატების შანსიც იზრდება. რეციდივის მაღალი სიხშირის გათვალისწინებით, ოპიოიდების მოხსნა დახმარების თანხლებით არ განიხილება როგორც ოპიოიდური დამოკიდებულების ეფექტიანი მკურნალობა (იხ. ნაწილი 6.3).
 |
10.4.1 6.4.1 ნიშნები, სიმძიმე და მკურნალობის პრინციპები |
▲back to top |
ოპიოიდების აღკვეთის სიმპტომების სიმძიმე დამოკიდებულია მოხმარებული ოპიოიდების დოზაზე და ფარმაკოლოგიურ თავისებურებებზე, ასევე, პაციენტში მომხდარი ნეიროადაპტაციური ცვლილებების ხარისხზე. ნარკოტიკები, რომლებსაც ხანმოკლე ნახევარდაშლის პერიოდი აქვს, აღკვეთის მდგომარეობის სიმპტომებს გაცილებით ადრეულ ფაზაში იძლევა, ვიდრე ხანგრძლივი ნახევარდაშლის პერიოდის მქონე ნარკოტიკები; უკანასკნელ შემთხვევაში სიმპტომები მოგვიანებით აღწევს პიკს და შემდეგ მცირდება. მკურნალობის გარეშე:
ჰეროინის ან მორფინის აღკვეთის მდგომარეობის სიმპტომები, ჩვეულებრივ, პიკს აღწევს ბოლო დოზიდან 36-72 საათის შემდეგ. სიმპტომები მნიშვნელოვნად მცირდება 5 დღის შემდეგ;
მეთადონის ან სხვა ხანგრძლივი მოქმედების ოპიოიდის აღკვეთის მდგომარეობა პიკს აღწევს მე-4-6 დღეს და სიმპტომების მნიშვნელოვანი შემსუბუქება არ ხდება 10-12 დღის განმავლობაში;
ბუპრენორფინის აღკვეთის სიმპტომები, ბუპრენორფინით ხანგრძლივი მკურნალობის უეცარი შეწყვეტის შემდეგ, იწყება ბოლო დოზიდან 3-5 დღეში, მსუბუქი მოხსნის სიმპტომები შეიძლება რამდენიმე კვირა გაგრძელდეს.
ოპიოიდურ ანტაგონისტებს (მაგ. ნალტრექსონი), რომლებიც რეცეპტორების აქტივობის სწრაფი ცვლილების ინდუქციას ახდენს, შეუძლია უფრო მძიმე აღკვეთის სიმპტომების გამოწვევა, ვიდრე, ჩვეულებრივ, ჰეროინის აღკვეთის დროს აღინიშნება. ნალტრექსონით მკურნალობა შეიძლება დაიწყოს ხანმოკლე მოქმედების ოპიოიდების და ბუპრენორფინის მოხსნიდან ერთი კვირის განმავლობაში. ამისგან განსხვავებით, ნალტრექსონით მკურნალობა არ იწყება, ვიდრე მეთადონის მიღების შეწყვეტიდან 10-14 დღე არ გავა.
აღკვეთის სიმპტომების სიმძიმე დაკავშირებულია ოპიოიდების მოხმარებასთან მიბმული ნეიროადაპტაციური ცვლილებების ხარისხთან და შექცევადობასთან. ყველაზე მძიმე აღკვეთის სიმპტომები აღინიშნება ნეიროადაპტაციის მაღალი ხარისხის პირობებში უეცარი რევერსირების დროს; მაგ., როდესაც ნალტრექსონს მიიღებს პაციენტი, რომელიც მეთადონის მაღალ დოზებს იღებს.
 |
10.4.2 6.4.2 ოპიოიდური აღკვეთის სინდრომის შეფასება |
▲back to top |
ოპიოიდების აღკვეთის მდგომარეობის სიმძიმის შეფასებისას გასათვალისწინებელია როგორც სუბიექტური, ისე ობიექტური სიმპტომები. აღკვეთის სინდრომის სუბიექტური სიმპტომე ბი უფრო მგრძნობიარე გასაზომია, მკვეთრად გამოხატული ობიექტური ნიშნები კი - უფრო სანდო. დოზის განსაზღვრისათვის ობიექტურ ნიშნებს მეტი ყურადღება უნდა მიექცეს, ვიდრე სუბიექტურ სიმპტომებს. ქვემოთ მოცემულია ოპიოიდების აღკვეთის სიმპტომები და მდგომარეობის სიმძიმის შეფასება - ვარსკვლავი მიუთითებს აღკვეთის სიმპტომებზე, რომლების გამოთვლაც შესაძლებელია ოპიოიდების აღკვეთის სუბიექტური სკალის (SOWS) მიხედვით:
ოფლიანობა*
ცრემლდენა (ჭარბი ცრემლიანობა)
მთქნარება*
ციებ-ცხელება*
ანორექსია და აბდომინალური სპაზმები*
გულისრევა
ღებინება და დიარეა*
ტრემორი
უძილობა და მოუსვენრობა*
გენერალიზებული ტკივილის სინდრომი*
ტაქიკარდია
ჰიპერტენზია*
პილოერექცია (ბატის კანი)
გაფართოებული გუგები
ნაწლავების პერისტალტიკის გაძლიერების გამო მუცელში ყურყურის გაძლიერება.
აღკვეთის სიმპტომების სიმძიმე ასევე შეიძლება გამოვითვალოთ ოპიოიდების აღკვეთის ობიექტური სკალით (OOWS) ან ობიექტური და სუბიექტური კონბინირებული სკალით, როგორიცაა ოპიოიდების აღკვეთის კლინიკური სკალა (COWS) (დანართი 11).
როდესაც ხდება ოპიოიდის დაგეგმილი მოხსნა (ანუ პაციენტს ვათავსებთ დეტოქსიკაციის დაწესებულებაში ან ვუნიშნავთ მედიკამენტს აღკვეთის სიმპტომების შესაბსუბუქებლად), მნიშვნელოვანია, ჩატარდეს პაციენტის ამომწურავი შეფასება (იხ. ნაწილი 6.1). პაციენტს უნდა ვაცნობოთ, თუ რა რისკი ახლავს ოპიოიდების აღკვეთას (შემდგომი რეციდივის ჩათვლით) ოპიოიდური აგონისტებით მხარდამჭერ მკურალობასთან შედარებით. ის, რომ ოპიოიდების მოხსნა უფრო მაღალ სიკვდილიანობასთან არის დაკავშირებული, ვიდრე ოპიოიდების აგონისტებით მხარდამჭერი მკურნალობა, აუცილებლად მითითებულ უნდა იქნეს პაციენტის ინფორმირებულ თანხმობაში. ოპიოიდური დეტოქსიკაცია სიფრთხილით უნდა ჩატარდეს, თუ პაციენტი ორსულია (განსაკუთრებით, პირველი და მესამე ტრიმესტრები) ან თუ აქვს მწვავე თანმხლები დაავადებები.
 |
10.4.3 6.4.3 მკურნალობის არჩევანი ოპიოიდური აღკვეთის სინდრომის დროს |
▲back to top |
ოპიოიდების აღკვეთის მართვა შეიძლება ოპიოიდების მოხმარების შეწყვეტის სიჩქარის კონტროლირებით და სიმპტომების შემამსუბუქებელი პრეპარატების დანიშვნით, ან ორივე ამ ღონისძიების კომბინაციით.
ამ დოკუმენტში ჩატარებულ ანალიზში ხაზგასმულია ოპიოიდების აღკვეთის მართვის სამი მეთოდი, რომლებიც ყველაზე უკეთ არის შეფასებული: პერორალური მეთადონის კლებადი დოზები, ენისქვეშ ბუპრენორფინის კლებადი დოზები და პერორალური ადრენერგული ალფა-2 აგონისტების კლებადი დოზები.
არსებობს ბევრი სხვა ალტერნატიული მკურნალობა, მაგ.:
ხანმოკლე მოქმედების პერორალური ოპიოიდები, რომლებიც ამ სახელმძღვანელოში არ განიხილება, რადგან არ მოიძებნა კვლევები მათი გამოყენების თაობაზე მათზე ზედამხედველობის სირთულეების გამო.
ოპიოიდების და ადრენერგული ალფა-2 აგონისტების ტრანსდერმული ფორმები, რომლებიც უკანასკნელ ხანს შემუშავდა - ისინი შეიძლება ეფექტიანი იყოს, მაგრამ ამ შემთხვევაშიც კვლევები ჩატარებული არ არის.
პრეპარატები სპეციფიკური აღკვეთის სიმპტომების მართვისთვის, რომლებიც გამოიყენება ოპიოიდებთან ან ალფა-2 აგონისტებთან კომბინაციაში (მაგ., ბენზოდიაზეპინები აგზნების და უძილობისთვის, ღებინების საწინააღმდეგო პრეპარატები გულისრევა-ღებინებისთვის და ანთების საწინააღმდეგო არასტეროიდული პრეპარატები [NSAID] კუნთების ტკივილისთვის).
დეტალური მითითებები ამ პრეპარატების გამოყენების შესახებ სცილდება მოცემული სახელმძღვანელოს მიზნებს.
რა მკურნალობა უნდა იქნეს გამოყენებული ოპიოიდების აღკვეთის მდგომარეობის მართვისთვის?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.6 |
ეფექტიანობა
მეთადონი ალფა-2 აგონისტებთან შედარებით
ჯგუფური ანალიზის დროს (7 კვლევა, 577 მონაწილე) მნიშვნელოვანი განსხვავება არ აღმოჩნდა მეთადონს და ალფა-2 აგონისტებს შორის მკურნალობის დასრულების თვალსაზრისით (RR 1.09, 95%-ი CI 0.90-1.32, საშუალო ხარისხის მტკიცებულება). განსხვავება არ იყო რეციდივის სიხშირეში, რაც პაციენტებზე შემდგომი დაკვირვებით გამოვლინდა (მკურნალობის განზრახვის ანალიზი) (RR 1.06, 95%-ი CI 0.55-2.02, დაბალი ხარისხის მტკიცებულება).
მეთადონი ბუპრენორფინთან შედარებით
ჯგუფური ანალიზის დროს (2 კვლევა, 63 მონაწილე) მნიშვნელოვანი განსხვავება არ აღმოჩნდა მეთადონს და ბუპრენორფინს შორის მკურნალობის დასრულების თვალსაზრისით (RR 0.88: 95%-ი CI 0.67-1.15, დაბალი ხარისხის მტკიცებულება).
ბუპრენორფინი ალფა-2 აგონისტებთან შედარებით
ჯგუფური ანალიზის დროს (8 კვლევა, 884 მონაწილე), სადაც ერთმანეთს შეადარეს ბუპრენორფინი და ალფა-2 აგონისტები, მკურნალობის დასრულების მაჩვენებელი ბუპრენორფინის შემთხვევაში უფრო მაღალი იყო (RR 1.67, 95%-ი CI 1.24-2.25, საშუალო ხარისხის მტკიცებულება), ასევე, აღინიშნა აღკვეთის ობიექტური სკალის უფრო ნაკლები პიკური მაჩვენებელი (RR 0.61, 95%-ი CI 0.86-0.36, საშუალო ხარისხის მტკიცებულება) და პაციენტის მიერ შეტყობინებული ოპიოიდების აღკვეთის სიმპტომების უფრო დაბალი მაჩვენებელი (SMD - 0.59, 95%-ი CI - 0.79-0.39, მაღალი ხარისხის მტკიცებულება).
უსაფრთხოება
მეთადონს სედაციის ყველაზე დიდი რისკი აქვს, თუმცა, ეს რისკი უფრო დაბალი დოზების (<20 მგ) გამოყენებით მცირდება. მიუხედავად იმისა, რომ ბუპრენორფინი უფრო უსაფრთხოა, ვიდრე მეთადონის მაღალი დოზები, სხვა სედატიური ეფექტის მქონე ნივთიერებებთან კომბინაციაში (ბენზოდიაზეპინები, ალკოჰოლი, ტრიციკლური ანტიდეპრესანტები, სედატიური ანტიჰისტამინები და ტრანკვილიზატორები) გამოყენებისას შეუძლია სუნთქვის მნიშვნელოვანი დათრგუნვა. აღწერილია სიკვდილის მრავალი შემთხვევა, გამოწვეული ბუპრენორფინის და ბენზოდიაზეპინების, ან სხვა სედატიური ნივთიერებების კომბინაციით. როგორც ნაწილობრივ აგონისტს, ბუპრენორფინს შეუძლია დაჩქარებული აღკვეთის სინდრომის ინდუცირება, თუ იმ პერიოდში გამოიყენება, როდესაც ჰეროინი ჯერ კიდევ შეკავშირებულია რეცეპტორებთან. ეს შეიძლება მოხდეს ბუპრენორფინის ოპიოიდების აღკვეთის სამკურნალოდ გამოყენების შემთხვევათა 10%-ში. ბუპრენორფინის მთავარი გვერდითი მოვლენა არის თავის ტკივილი. ალფა-2 აგონისტებს შეუძლია პოსტურალური ჰიპოტენზიის გამოწვევა, რაც თავბრუსხვევის და გულის წასვლის მიზეზი ხდება. დოზის გარაჭარბებისას ალფა-2 აგონისტები იწვევს ძლიერ ბრადიკარდიას, რასაც შეიძლება ინტენსიური თერაპია დასჭირდეს, მაგრამ, ჩვეულებრივ, ფატალური არ არის. ლოფექსიდინი ნაკლებად იწვევს პოსტურალურ ჰიპოტენზიას, ვიდრე კლონიდინი; კოქრეინის კოლაბორაციის მიერ კლინიკური კვლევების მიმოხილვამ უსაფრთხოების მხრივ განსხვავება არ აჩვენა.
ხარჯების ეფექტიანობა
შეზღუდულია მონაცემები იმის შესახებ, თუ როგორია მოცემული პრეპარატების ხარჯების ეფექტიანობა ოპიოიდების აღკვეთის სინდრომის მკურნალობისას. ბუპრენორფინი და ლოფექსიდინი უფრო ძვირია, ვიდრე მეთადონი. ამის მიუხედავად, ავსტრალიაში ჩატარებულმა ანალიზმა აჩვენა, რომ ამბულატორიულად დანიშნული ბუპრენორფინი ხარჯების მხრივ უფრო ეფექტიანია, ვიდრე ამბულატორიულად დანიშნული კლონიდინი [158].
შეზღუდული მონაცემები
დეტოქსიკაციაზე ჩატარებული კვლევების მიხედვით აღკვეთის სინდრომის მკურნალობის ფარდობითი ეფექტიანობის შეფასება რთულია პრაქტიკაში გამოყენებული მეთოდების სხვადასხვაობის გამო. გარდა ამისა, მონაწილეები ხშირად კლინიკას ბოლო დოზის მიღების დღეს ტოვებენ, აღკვეთის სიმპტომების მთლიანად მოხსნამდე. სასარგებლო იქნებოდა აღკვეთის მდგომარეობის სიმძიმის შედარება მკურნალობის სხვადასხვა მეთოდის გამოყენებისას, მაგრამ ეს მონაცემები რეგულარულად არ გროვდება და რთულია მეტაანალიზის ჩატარება. გარდა ამისა, აღკვეთის სინდრომის მკურნალობის მეთოდები სხვადასხვაა, მცირეა კვლევების რაოდენობა, სადაც ერთნაირი მიდგომა გამოიყენება.
მკურნალობის საკითხები, მკურნალობის ხანგრძლივობა
ყველა ტიპის მკურნალობა შეიძლება ჩატარდეს როგორც ამბულატორიულ, ისე სტაციონარის პირობებში. არადანიშნულებით მოხმარების შესამცირებლად და უსაფრთხოების გასაზრელად მეთადონის და ბუპრენორფინის დანიშვნა შესაძლებელია ზედამხედველობით, დღეში ერთხელ (გუანფასინი ასევე შეიძლება დღეში ერთხელ დაინიშნოს, თუმცა ალფა-ადრენერგული აგონისტებისთვის დოზაზე ზედამხედველობა ნაკლებად არის საჭირო). მეთადონის და ბუპრენორფინის თანდათანობით შემცირებას შეუძლია შეამსუბუქოს აღკვეთის მდგომარეობის სიმპტომები და გაზარდოს აღკვეთის პერიოდი. ამგვარი თანდათანობითი კლება აუმჯობესებს მკურნალობის პროგრამაში დარჩენის პერსპექტივას, მაგრამ ამცირებს აღკვეთის სინდრომის მკურნალობის წარმატებით დასრულებას [159].
დასკვნა
ბუპრენორფინი შესაძლებელია დღეში ერთხელ დაინიშნოს; იგი იწვევს აღკვეთის ნაკლებად მძიმე სიმპტომებს და მისი საშუალებით უფრო ხშირად მიდის მკურნალობა ბოლომდე, ვიდრე ალფა-2 აგონისტების დროს.
მეთადონი უფრო იაფია, ვიდრე ბუპრენორფინი და დაჩქარებული აღკვეთის სინდრომის რისკი არ აქვს; იგი შეიძლება გამოვიყენოთ ორსულებშიც.
ალფა-2 აგონისტებს შეუძლია შეამციროს აღკვეთის სიმპტომების ხანგრძლივობა და შეამოკლოს ნალტრექსონის დასაწყებად საჭირო დრო.
ზემოთ ჩამოთვლილი ყველა მედიკამენტი შესაძ ლებელია გამოვიყენოთ ოპიოიდების აღკვეთისთვის. კლინიკური კვლევები ნათლად უჩვენებს, რომ ბუპრენორფინი უფრო ეფექტიანია, ვიდრე ალფა-2 აგონისტები, ხოლო კლინიკური გამოცდილების მიხედვით, მეთადონი ამ ორს შორის მდებარეობს. კოქრეინის კოლაბორაციის მიმოხილვის მიხედვით, მეთადონი დანარჩენი ორი პრეპარატის ეკვივალენტურია. არჩევანი დამოკიდებულია ინდივიდუალურ სიტუაციაზე, აღკვეთის სიმპტომების ატანის უნარზე, დროის რესურსზე და პაციენტის არჩევანზე.
რეკომენდაცია ოპიოიდების აღკვეთის მდგომარეობის სამართავად გამოყენებული უნდა იყოს ოპიოიდური აგონისტების კლებადი დოზები, თუმცა, ასევე შესაძლებელია ალფა-2 ადრენერგული აგონისტების გამოყენება.
|
 |
10.4.4 6.4.4 აღკვეთის სინდრომის დაჩქარებული მკურნალობის მეთოდები |
▲back to top |
აღკვეთის დაჩქარებული მეთოდების დროს ოპიოიდური ანტაგონისტები აღკვეთის ინდუქციისა და პროცესის უფრო სწრაფად დასრულებისთვის გამოიყენება. აქ ეს მეთოდები დაყოფილია იმის მიხედვით, თუ რა პირობებში ტარდება: მინიმალური თუ ღრმა სედაციის. მინიმალური სედაცია გულისხმობს იმგვარ სედაციას, რომელიც ხშირად გამოიყენება ოპიოიდების მოხსნისას ამბულატორიულ ან კლინიკის პირობებში, რადგან მას ნაკლებად ახლავს სუნთქვის დათრგუნვის რისკი. ღრმა სედაცია გულისხმობს პერორალური ან პარენტერალური სედატიური ნივთიერებების დანიშვნას ან ანესთეზიას, რაც სუნთქვის დათრგუნვის მნიშვნელოვან რისკს უკავშირდება. ღრმა სედაციის გამოყენება მოითხოვს ინტენსიურ მონიტორინგს და საჭიროების შემთხვევაში მართვითი სუნთქვის შესაძლებლობას, ისევე, როგორც ინტენსიური თერაპიის ბლოკში.
უნდა გამოვიყენოთ თუ არა ოპიოიდების აღკვეთისას ანტაგონისტები მინიმალური სედაციით?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.8 |
ეფექტიანობა
მოიძებნა ოთხი კვლევა (394 მონაწილე), რომლებშიც შესწავლილ იქნა მინიმალური სედაციის ანტაგონისტების ოპიოიდების აღკვეთის დროს გამოყენების შესაძლებლობა. ჯგუფური ანალიზის დროს ოპიოიდური ანტაგონისტების გამოყენების სხვადასხვა მეთოდებს შორის მკურნალობის დასრულების სიხშირის მხრივ მნიშვნელოვანი განსხვავება არ გამოვლინდა (RR 1.26: 95%-ი CI 0.80-2.00, საშუალო ხარისხის მტკიცებულება). არ გამოვლინდა ასევე განსხვავება რეციდივის სიხშირეებს შორის (RR 0.83: 95%-ი CI 0.52-1.35, დაბალი ხარისხის მტკიცებულება) [160].
უსაფრთხოება
მონაცემები დაკვირვების პრინციპით ჩატარებული კვლევებიდან გვიჩვენებს გვერდითი მოვლენების მაღალ სიხშირეს ოპიოიდური ანტაგონისტების გამოყენების დროს (RR 3.7: 95%-ი CI 0.65-21.32, ძალზე დაბალი ხარისხის მტკიცებულება).
ხარჯების ეფექტიანობა
მართალია ოპიოიდური ანტაგონისტების მოხმარება ზრდის მედიკამენტებზე გაწეულ ხარჯებს ოპიოიდების აღკვეთის მდგომარეობის მკურნალობისას, მაგრამ ხარჯების საერთო ეფექტიანობა შეიძლება უკეთესი იყოს ჩვეულებრივი აღკვეთის მდგომარეობის მართვასთან შედარებით, თუ პირველ შემთხვევაში ანტაგონისტების გამოყენების გამო მკურნალობის ხანგრძლივობა შემცირდება [158].
მკურნალობის საკითხები
ნალტრექსონის ჰიდროქლორიდი ძირითადად გამოდის მყარი პერორალური ფორმის სახით - 25 და 50 მგ-იანი ტაბლეტები. ნალოქსონი არსებობს საინექციო ამპულების სახით, კონცენტრაციით 0.4 მგ 1 მლ-ში, ან წინასწარ მომზადებული შპრიცის სახით.
მკურნალობის რეჟიმები
კლინიკურ კვლევებში გამოყენებული დოზის დანიშვნის რეჟიმი შეიძლება გულისხმობდეს დღეში 50 მგ ნალტრექსონის ერთჯერად მიღებას ან დღეში 12.5 მგ ნალტრექსონის დოზის თანდათანობით ზრდას. შესაძლებელია ნალოქსონის ერთჯერადი დღიური დოზის ან ნალოქსონის ინფუზიების გამოყენება. გარკვეული არ არის, თუ ამ მეთოდებიდან რომელია უფრო ეფექტიანი. ერთი, რაც დადგენილია, არის ის, რომ ნალტრექსონის უფრო მაღალი საწყისი დოზების გამოყენება დაკავშირებულია დელირიუმის განვითარების მაღალ რისკთან. ოპიოიდური ანტაგონისტების შეყვანიდან რამდენიმე საათის განმავლობაში აუცილებელია პაციენტზე ყურადღებით დაკვირვება, რადგან არსებობს დელირიუმის, ღებინების და დიარეის განვითარების რისკი. ხშირი დიარეის და გულისრევის თავიდან ასაცილებლად, ძირითადად, საჭიროა ძვირი მედიკამენტები, როგორებიცაა ონდანსეტრონი და ოქტრეატიდი სითხეების ინტრავენურ შეყვანასთან ერთად. ოპიოიდური ანტაგონისტებით აღკვეთის სინდრომის მკურნალობის მეთოდებით არ უნდა ვისარგებლოთ გულით, ფსიქოზით, თირკმლის ქრონიკული უკმარისობით, ღვიძლის დეკომპენსაციით დაავადებულ ან ალკოჰოლზე, ბენზოდიაზეპინებზე ან სტიმულატორებზე დამოკიდებულ პაციენტებთან.
სარგებელი
ანტაგონისტების გამოყენებას შეუძლია აღკვეთის სინდრომის ხანგრძლივობის შემცირება, რაც, საერთო ჯამში, ამცირება აღკვეთის სინდრომის სიმძიმეს და ზრდის მკურნალობის წარმატებით დამთავრების შანსს. ჰოსპიტალიზებული პაციენტებისათვის (რომლებსაც კლინიკაში ყოფნა მედიკამენტის ღირებულებაზე გაცილებით ძვირი უჯდებათ) ამ მეთოდის გამოყენებას თანხების მნიშვნელოვანი დაზოგვაც შეუძლია. ეს მეთოდი აადვილებს ნალტრექსონით მკურნალობის დაწყებას. არასასურველი ეფექტები და შედეგები ოპიოიდების აღკვეთის სინდრომის მკურნალობის გვერდითი მოვლენები შეიძლება მოიცავდეს აღკვეთის სიმპტომების მაღალ პიკს, რამაც შეიძლება გამოიწვიოს დეჰიდრატაცია (და ამასთან დაკავშირებული გართულებები, როგორიცაა თირკმლის უკმარისობა) და დელირიუმი. მძიმე აღკვეთის სიმპტომების პიკზე ჭარბი სედაციის გართულებები შეიძლება იყოს ასპირაციული პნევმონია და სუნთქვის დათრგუნვა.
დასკვნა
ოპიოიდების აღკვეთის სინდრომის მკურნალობაზე ჩატარებულ მცირე რაოდენობით კლინიკურ კვლევებში სხვადასხვა მეთოდია გამოყენებული, რაც ართულებს შედეგების განზოგადებას. ამ კვლევებიდან მიღებული შედეგები მიუთითებს, რომ ანტაგონისტებით ინდუცირებული აღკვეთის მეთოდები დასაწყისში ზრდის ოპიოიდების აღკვეთის სინდრომის სიმძიმეს და შეიძლება აღკვეთასთან დაკავშირებული გვერდითი მოვლენების სიხშირეც გაიზარდოს. პოტენციური ზიანის გათვალისწინებით, არ არის საკმარისი მონაცემები სარგებლის შესახებ ამ მეთოდების რუტინული გამოყენების რეკომენდაციის გასაცემად.
რეკომენდაცია ოპიოიდების აღკვეთის სინდრომის მართვის დროს კლინიცისტებმა რუტინულად არ უნდა გამოიყენონ ოპიოიდური ანტაგონისტების და მინიმალური სედაციის კომბინაცია. რეკომენდაციის ძალა - სტანდარტული მტკიცებულების ხარისხი - ძალიან დაბალი შენიშვნები - ეს რეკომენდაცია უფრო დიდ მნიშვნელობას ანიჭებს დელირიუმთან და დეჰიდრატაციასთან დაკავშირებული გვერდითი მოვლენების პრევენციას, ვიდრე აღკვეთის სიმპტომების საერთო სიმძიმის ან ხანგრძლივობის შემცირების რაიმე შეასაძლებლობას. თუ ოპიოიდური ანტაგონისტების გამოყენება აუცილებელია, სულ ცოტა, 8 საათის განმავლობაში ყურადღებით უნდა დავაკვირდეთ პაციენტს, რადგან არსებობს დელირიუმის, ღებინების და დიარეის განვითარების შანსი; ხელმისაწვდომი უნდა იყოს სისტემები იმ პაციენტების იდენტიფიცირებისა და მკურნალობისთვის, რომლებსაც დეჰიდრატაცია ან დელირიუმი უვითარდებათ. ოპიოიდური ანტაგონისტებით ოპიოიდების მოხსნა არ უნდა მოხდეს ორსულ ქალებში, რადგან ამან შეიძლება გამოიწვიოს აბორტი ან ნაადრევი მშობიარობა. |
შეიძლება თუ არა ოპიოიდების აღკვეთის დროს ანტაგონისტების გამოყენება ღრმა სედაციასთან ან ანესთეზიასთან ერთად?
ოპიოიდების მოხსნა ოპიოიდური ანტაგონისტების და ღრმა სედაციის ან ანესთეზიის საშუალებით განისაზღვრება როგორც აღკვეთის სინდრომის მკურნალობის მეთოდი, რომლის დროსაც საჭიროა სასიცოცხლო ფუნქციების (სუნთქვის სიხშირე და ჟანგბადის სატურაცია) მონიტორინგი. ამგვარი მკურნალობა, ჩვეულებრივ, ინტენსიური თერაპიის განყოფილებებში ტარდება.
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.9 |
ეფექტიანობა
კოქრეინის კოლაბორაციის ბოლო მიმოხილვაში [161] გამოვლინდა რანდომიზებული კონტროლირებული კვლევები, რომლებშიც ულტრასწრაფი ოპიოიდური დეტოქსიკაცია (UROD) შედარებულ იქნა შემდეგ მეთოდებთან:
ოპიოიდების აღკვეთის სინდრომის მკურნალობა სტაციონარის პირობებში კლონიდინთან ერთად (ორი კვლევა [162, 163];
ოპიოიდების აღკვეთის სინდრომის მკურნალობა სტაციონარის პირობებში ბუპრენორ ფინის გამოყენებით (ერთი კვლევა [163]);
ოპიოიდური ანტაგონისტების და მინიმალური სედაციის გამოყენების მეთოდი (ორი კვლვა [164, 165]).
მკურნალობის დასრულება და ნალტრექსონის დაწყება
ჯგუფური ანალიზის დროს ნალტრექსონის კლონიდინთან (RR 1.15, 95%-ი CI 0.79-1.68, საშუალო ხარისხის მტკიცებულება) ან ბუპრენორფინთან (RR 0.82, 95%-ი CI 0.34-1.97, დაბალი ხარისხის მტკიცებულება) შედარებისას მკურნალობის დასრულების სიხშირის მხრივ განსხვავება არ აღმოჩნდა. ანტაგონისტების და ღრმა სედაციის გამოყენებას ნალტრექსონის მიღების დაწყების უფრო მაღალი მაჩვენებელი ჰქონდა, ვიდრე სტაციონარში კლონიდინით აღკვეთის მკურნალობას (RR 3.40, 95%-ი CI 2.32-4.98, საშუალო ხარისხის მტკიცებულება), მაგრამ არა სტაციონარში ბუპრენორფინით აღკვეთის მკურნალობას (RR 0.97, 95%-ი CI 0.88-1.07, დაბალი ხარისხის მტკიცებულება).
რეციდივი დაკვირვების პერიოდში
ღრმა სედაციის ან ანესთეზიის გამოყენებას განსხვავებული შედეგი არ მოჰყოლია 6 თვიანი დაკვირვების დროს ჰეროინის გამოყენების განახლების მხრივ (RR 0.97, 95%-ი CI 0.88-1.08, საშუალო ხარისხის მტკიცებულება).
მკურნალობის პროგრამაში დარჩენა 12 თვის
განმავლობაში ღრმა სედაციის ან ანესთეზიის გამოყენებას განსხვავებული შედეგი არ მოჰყოლია 12 თვის განმავლობაში მკურნალობის პროგრამაში დარჩენის მხრივ (RR 0.95, 95%-ი CI 0.69-1.30, საშუალო ხარისხის მტკიცებულება).
უსაფრთხოება
ღრმა სედაციის ან ანესთეზიის გამოყენებისას აღინიშნა გვერდითი მოვლენების უფრო მაღალი მაჩვენებლები (RR 3.21, 95%-ი CI 1.13-9.12, საშუალო ხარისხის მტკიცებულება). პოტენციური გვერდითი მოვლენები მოიცავს ოპიოიდების აღკვეთის მძიმე სიმპტომებს, რაც იწვევს დეჰიდრატაციას (და შემდგომ გართულებებს, როგორიცაა თირკმლის უკმარისობა) და დელირიუმს. ჭარბი სედაციის პოტენციურ გართულებებს მიეკუთვნება ასპირაციული პნევმონია და სუნთქვის დათრგუნვა [166]. ღრმა სედაციის ჯგუფში 35 მონაწილიდან სამს აღენიშნა სიცოცხლისათვის საშიში გვერდითი მოვლენები; არაღრმა სედაციის ჯგუფში კი 71 პაციენტიდან არც ერთს არ ჰქონია მსგავსი გართულებები (RR 14, 95%-ი CI 0.74-264, დაბალი ხარისხის მტკიცებულება).
ხარჯების ეფექტიანობა
მეთოდები, რომლებიც იყენებს ღრმა სედაციას და ანესთეზიას, ძვირადღირებულია. ავსტრალიაში ჩატარებული ანალიზის მიხედვით, ხარჯების მხრივ ამ მეთოდებს არანაირი უპირატესობა არ გააჩნია იმ მეთოდებთან შედარებით, სადაც ანტაგონისტები მინიმალურ სედაციასთან ერთად გამოიყენება [158].
შეზღუდული მონაცემები
მონაცემების უსაფრთხოების ზუსტად შესაფასებლად არ მოიპოვება საკმარისი რაოდენობის კვლევები. სხვადასხვა მეთოდი შეიძლება დაკავშირებული იყოს უსაფრთხოების და ეფექტიანობის სხვადასხვა ტიპთან.
მკურნალობის საკითხები
მეთოდები, რომლებიც ღრმა სედაციას მოიცავს, უნდა ჩატარდეს, სულ მცირე, იმგვარ გარემოში, სადაც შესაძლებელია სუნთქვის დათრგუნვის მკურნალობა (ინტენსიური თერაპიის ბლოკი). აღწერილია სიკვდილის ბევრი შემთხვევა, როცა ეს მეთოდი ინტენსიური თერაპიის არარსებობის პირობებში გამოიყენებოდა [166, 167].
დასკვნა
ოპიოიდური დეტოქსიკაციისათვის მეთადონით და ალფა-2 ადრენერგული აგონისტებით მკურნალობასთან შედარებით, ოპიოიდური ანტაგონისტების და ღრმა სედაციის გამოყენება შეიძლება ნიშნავდეს ნალტრექსონის ადრე დაწყების შესაძლებლობას. თუმცა, ოპიოიდური ანტაგონისტების და ღრმა სედაციის გამოყენება ნაკლები სარგებლის მომტანია, ვიდრე ბუპრენორფინით აღკვეთის სინდრომის მკურნალობა, ან ოპიოიდური ანტაგონისტების გამოყენება მინიმალურ სედაციასთან ერთად. ამასთანავე, ოპიოიდური ანტაგონისტების და ღრმა სედაციის გამოყენება გაცილებით ხშირად იწვევს გართულებებს. ამ შეფარდების გათვალისწინებით, მეთოდები, რომლებშიც ოპიოიდური ანტაგონისტები და ღრმა სედაცია კომბინირებულია, რეკომენდებული არ არის.
რეკომენდაცია ოპიოიდების აღკვეთის სინდრომის მართვისას კლინიცისტებმა არ უნდა გამოიყენონ ოპიოიდური ანტაგონისტების კომბინაცია ღრმა სედაციასთან ერთად.
|
 |
10.4.5 6.4.5 მკურნალობის პირობები ოპიოიდური აღკვეთის სინდრომის დროს |
▲back to top |
სად უნდა მოხდეს ოპიოიდების მოხსნა - სტაციონარში თუ ამბულატორიულ პირობებში?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.10 |
ეფექტიანობა
კოქრეინის კოლაბორაციის ბოლო მიმოხილვაში [168] გამოვლინდა ერთი რანდომიზებული კონტროლირებული კვლევა, რომელშიც პირდაპირ იყო განხილული, თუ სად უნდა მოხდეს ოპიოიდების მოხსნა - სტაციონარში თუ ამბულატორიულ პირობებში. მიმოხილვამ აჩვენა, რომ მკურნალობის დასრულების მაჩვენებელი უკეთესია სტაციონარის ჯგუფში (RR 1.91, 95%-ი CI 1.03-3.55, ძალიან დაბალი ხარისხის მტკიცებულება). სტაციონარის და ამბულატორიულ ჯგუფებში რეციდივის მაჩვენებლის მხრივ განსხვავება არ იყო (RR 1.07, 95%-ი CI 0.97-1.18).
უსაფრთხოება
მონაცემები, სადაც შედარებული იქნებოდა სტაციონარული და ამბულატორიული მკურნალობა, არ მოიძებნა. მოსალოდნელია, რომ სტაციონარის პირობებში მოხსნა უფრო უსაფრთხო იქნება, ვიდრე ამბულატორიულ პირობებში, თუმცა, მონაცემები ამასთან დაკავშირებით მოპოვებული არ არის.
ხარჯების ეფექტიანობა
ოპიოიდური დეტოქსიკაცია სტაციონარის პირობებში ბევრად უფრო ძვირია, ვიდრე ამბულატორიულ პირობებში. ავსტრალიის მონაცემები გვიჩვენებს, რომ დეტოქსიკაცია ამბულატორიულ პირობებში ხარჯების მხრივ გაცილებით ეფექტიანია [158].
შეზღუდული მონაცემები
რანდომიზებული კონტროლირებული კვლევები, რომელთაც ემყარება ეფექტიანობის მონაცემები, გარკვეული ნაკლოვანებებით ხასიათდება; შედეგად, დაბალია მტკიცებულების ხარისხი. არსებობს მონაცემები, რომ სტაციონარის ჯგუფში მოხვედრილმა ბევრმა პაციენტმა უარი თქვა სტაციონარულ მკურნალობაზე ან პროგრამიდან ოპიოიდების აღკვეთის მდგომარეობის დამთავრდებამდე გამოვიდა.
მკურნალობის საკითხები
სტაციონარული მკურნალობა ძვირია, რადგან მოითხოვს უსაფრთხო გარემოს, 24 საათიან მოვლას და ყოველდღიურ სამედიცინო მეთვალყურეობას. ოპიოიდების მოხსნის პროცესში პაციენტები, ჩვეულებრივ, მოუსვენრები და გაღიზიანებულები არიან და მუშაობა ამგვარ გარემოში შეიძლება გარკვეულ საფრთხეებთან იყოს დაკავშირებული. პერსონალის ჯანმრთელობის და უსაფრთხოების უზრუნველყოფა სტაციონარის პირობებში მოითხოვს შესაბამისად მომზადებულ თანამშრომლებს და სწავლების სათანადო დონეს.
სარგებელი
ოპიოიდების მოხსნა სტციონარში უფრო მაღალი ეფექტიანობით ხასიათდება და, სავარაუდოდ, უფრო უსაფრთხოც არის.
არასასურველი ეფექტები და შედეგები
ოპიოიდების მოხსნა სტაციონარში ძვირია და ბევრი პაციენტისთვის მოსახერხებელი არ არის.
დასკვნა
სტაციონარულ დეტოქსიკაციას, ამბულატორიულ დეტოქსიკაციასთან შედარებით, მკურნალობის დასრულების უფრო მაღალი მაჩვენებელი აქვს, მაგრამ რეციდივის სიხშირის მხრივ განსხვავება გამოვლენილი არ არის. არ არსებობს საკმარისი მონაცემები სტაციონარული და ამბულატორიული დეტოქსიკაციის ფარდობითი უსაფრთხოების შესადარებლად. ხარჯების მხრივ ბევრად ეფექტიანია ოპიოიდური დეტოქსიკაცია უმრავლეს შემთხვევაში ჩატარდეს ამბულატორიულად, სტაციონარული დეტოქსიკაცია კი გამოყენებული იქნეს შემდეგ შემთხვევებში:
როცა წარსულში ამბულატორიული დეტოქსიკაციის კურსი წარუმატებლად დამთავრდა;
ოპიოიდების აღკვეთის სინდრომის მკურნალობის დროს აღინიშნა გართულებები;
სოციალური მხარდაჭერა არასაკმარისია ან აღინიშნება თანმხლები სამედიცინო ან ფსიქიატრიული დაავადებები.
6.4.6 ფსიქოსოციალური დახმარება ოპიოიდური აღკვეთის სინდრომის ფარმაკოლოგიურ მკურნალობასთან ერთად
მკურნალობის რომელი ტიპი უფრო ეფექტიანია ოპიოიდების მოხსნის დროს - მხოლოდ ფსიქოსოციალური დახმარება თუ ფსიქოსოციალური დახმარება ფარმაკოლოგიურ მკურნალობასთან ერთად?
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.13 |
ეფექტიანობა
ხუთი რანდომიზებული კონტროლირებული კვლევის ჯგუფური ანალიზი (184 მონაწილე) მიუთითებს, რომ კომბინირებული ფსიქოსოციალური და ფარმაკოლოგიური მკურნალობა დაკავშირებულია მკურნალობის დასრულების უფრო მაღალ სიხშირესთან (RR 1.68, 95%-ი CI 1.11-2.55, საშუალო ხარისხის მტკიცებულება) და შემდგომ პერიოდზე დაკვირვებისას რეციდივის უფრო დაბალ მაჩვენებელთან (RR 0.41, 95%-ი CI 0.27-0.62, საშუალო ხარისხის მტკიცებულება), მიუხედავად იმისა, რომ დეტოქსიკაცის პერიოდს ოპიოიდების გამოყენების უფრო ხშირი ტენდენცია ახასიათებს(RR 1.3, 95%-ი CI 0.99-1.70, საშუალო ხარისხის მტკიცებულება). დეტოქსიკაციისას სხვა ნივთიერების გამოყენების სიხშირის მხრივ განსხვავება დაფიქსირებული არ არის [169].
მკურნალობის საკითხები
კვლევებში მოცემული ფსიქოსოციალური დახმარების ტიპებია: გაუთვალისწინებელი სიტუაციების მართვა, თემის გაძლიერება, ფსიქოთერაპიული კონსულტაცია და ოჯახური თერაპია. მონაცემები არ გვიჩვენებს ერთი მეთოდის გამოხატულ უპირატესობას მეორესთან შედარებით, თუმცა მტკიცებულებები (ოთხი კვლევიდან) ყველაზე უკეთესია გაუთვალისწინებელი სიტუაციების მართვის მეთოდისთვის მეთადონის ან ბუპრენორფინის კომბინაციით.
სარგებელი
ფსიქოსოციალურ დახმარებას შეუძლია:
ხელი შეუწყოს პაციენტს თავისი მიზნების განსაზღვრაში ნარკოტიკების მოხმარე ბასთან დაკავშირებით;
გაზარდოს პაციენტის მოტივაცია ნარკოტიკების მიღების შესაწყვეტად ან შესამცირებლად;
გაზარდოს ოპიოიდური დეტოქსიკაციის მცდელობის შედეგების ანგარიშგება.
ამასთანავე, ფსიქოსოციალურ დახმარებას შეუძლია აამაღლოს პაციენტების ცოდნა აღკვეთის მათთვის მოსალოდნელი სიმპტომების შესახებ; მიაწოდოს სასარგებლო მეთოდები აღკვეთის სიმპტომების მინიმუმამდე შესამცირებლად და დაეხმაროს მათ აღკვეთის არსებული მდგომარეობის ფენომენის ინტერპრეტაციაში. ასევე, ფსიქოსოციალურ დახმარებას შეუძლია გააადვილოს გადასვლა დეტოქსიკაციის შემდგომ მკურნალობაზე და დაეხმაროს პაციენტს სოციალურ რეინტეგრაციაში.
არასასურველი ეფექტები და შედეგები
არსებობს თეორიული რისკი, რომ ფსიქოსოციალურმა დახმარებამ პაციენტებისთვის, რომლებიც იმყოფებიან ოპიოიდების მოხსნის პროცესში, უნებლიედ ხელი შეუწყოს პაციენტების მიერ ოპიოიდური დეტოქსიკაციის გაგრძელებას უფრო ეფექტიან ხანგრძლივ მეთოდზე გადასვლის ნაცვლად, როგორიცაა ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა.
დასკვნა
მათთვის, ვისაც სურს ოპიოიდების მოხსნა, კომბინირებული ფსიქოსოციალური და ფარმაკოლოგიური მკურნალობა ზრდის ოპიოიდების მოხსნის წარმატებით დამთავრების შანსს. ყველაზე კარგი შედეგები მიღებულია გაუთვალისწინებელი შემთხვევების მართვასთან დაკავშირებით.
რეკომენდაცია ფსიქოსოციალური დახმარება რუტინულად უნდა შევთავაზოთ პაციენტს ოპიოიდების მოხსნის ფარმაკოლოგიურ მკურნალობასთან ერთად.
|
 |
10.5 6.5 მკურნალობა ოპიოიდური ანტაგონისტით (ნალტრექსონი) |
▲back to top |
უნდა გამოვიყენოთ თუ არა ოპიოიდური ანტაგონისტით მკურნალობა ოპიოიდური დამოკიდებულების დროს და რა ჩვენებები არსებობს მისი მოხმარებისათვის?
ნალტრექსონი მაღალსპეციფიკური ოპიოიდური ანტაგონისტია ოპიოიდური რეცეპტორების მიმართ მაღალი აფინურობით. იგი ეფექტიანად ბლოკავს უფრო დაბალი აფინურობის ოპიოიდური აგონისტების (მეთადონი და ჰეროინი) მოქმედებას. ნალტრექსონის ჰიდროქლორიდი ბევრ ქვეყანაშია ხელმისაწვდომი 25 და 50 მგ-იანი ტაბლეტების სახით; იგი ასევე გამოიყენება ალკოჰოლური დამოკიდებულების სამკურნალოდ.
იხ. მონაცემები 1-ლ დანართში, ნაწილი A1.11 |
 |
10.5.1 6.5.1 ოპიოიდური ანტაგონისტით მკურნალობის ჩვენებები |
▲back to top |
ეფექტიანობა
ნალტრექსონი შეადარეს პლაცებოს ოპიოიდების მოხსნისას (ფსიქოსოციალური დახმარებით ან მის გარეშე). მკურნალობის პროგრამაში დაყოვნებაზე ნალტრექსონს არანაირი ეფექტი არ ჰქონდა (RR 1.08, 95%-ი CI 0.74-1.57, საშუალო ხარისხის მტკიცებულება). აღინიშნა ჰეროინის გამოყენების შემცირება ნალტრექსონის მოხმარებისას (RR 0.72, 95%-ი CI 0.58-0.90, დაბალი ხარისხის მტკიცებულება). შემდგომი დაკვირვების პერიოდში რეციდივის სიხშირის მხრივ განსხვავება არ დაფიქსირდა (RR 0.94, 95%-ი CI 0.67-1.34, ძალიან დაბალი ხარისხის მტკიცებულება). ასევე, ნალტრექსონის გამოყენებისას აღინიშნა კრიმინალური ქცევის მნიშვნელოვანი შემცირება (RR 0.50, 95%-ი CI 0.27-0.91, ძალზე დაბალი ხარისხის მტკიცებულება).
უსაფრთხოება
გვერდითი მოვლენების შეტყობინებულ მაჩვენებლებს შორის განსხვავება არ აღინიშნა (RR 1.21, 95%-ი CI 0.81-1.81). თუმცა, დაკვირვების პრინციპით ჩატარებულმა ზოგიერთმა კვლევამ ოპიოიდური ზედოზირების მაღალი მაჩვენებელი აჩვენა ნალტრექსონით მკურნალობის შეწყვეტის შემდეგ.
შეზღუდული მონაცემები
ნალტრექსონი ოპიოიდური დამოკიდებულების რეციდივის სიხშირის მხრივ მხოლოდ მცირე რაოდენობით კვლევებში იქნა გამოკვლეული.
სარგებელი
ნალტრექსონით მკურნალობა იწვევს ჰეროინის მოხმარების და კრიმინალური აქტივობის შემცირებას. ოპიოიდების მომხმარებლების ოჯახის წევრებს ხშირად მოსწონთ ნალტრექსონით მკურნალობა, რადგან ნათელია, რომ თუ პაციენტი ნალტრექსონს იღებს, ე.ი. არ მოიხმარს ჰეროინს. ასევე, როცა ოჯახის წევრები უშუალოდ აკვირდებიან ნალტრექსონის მიღებას, ეს ზრდის მათ მონაწილეობას ინდივიდის მკურნალობაში. 50 მგ ნალტრექსონი ჰეროინის ეფექტს დაახლოებით 24 საათის განმავლობაში ბლოკავს.
არასასურველი ეფექტები და შედეგები
პაციენტები ხშირად წყვეტენ ნალტრექსონის მიღებას, რათა ისევ გამოიყენონ ჰეროინი. ამ შემთხვევაში მათთვის რთულია ჰეროინის დოზის განსაზღვრა, რადგან ნალტრექსონის ეფექტი თანდათან იხსნება. ჰეროინის ერთი და იგივე დოზა 12 საათის განმავლობაში შეიძლება დაიბლოკოს ან ფატალური აღმოჩნდეს. აღნიშნულმა
შესაძლოა გამოიწვიოს ოპიოიდების უნებლიე ზედოზირება იმ პაციენტთა შორის რომლებიც წყვეტენ ნალტრექსონით მკურნალობას.
არსებობს მოსაზრება, რომ ნალტრექსონი შეიძლება გამოყენებულ იქნეს იძულებითი თერაპიის სახით. ამგვარი იძულებითი ფარმაკოლოგიური ჩარევა არაეთიკურია. მეტიც, ამ სახით გამოყენებულ ნალტრექსონს შეიძლება არ ჰქონდეს იგივე შედეგი, რაც მისი ნებაყოფლობითი მოხმარებისას აღინიშნება.
მკურნალობის საკითხები
ნალტრექსონი გამოდის 25 და 50 მგ-იანი ტაბლეტების სახით. დღესდღეობით, მედიკამენტის ღირებულება 50 ცენტიდან 5 აშშ დოლარამდე მერყეობს. თითოეული აბი ჰეროინის ეფექტს 24-48 სთ-ის განმავლობაში ბლოკავს. რადგანაც ნალტრექსონი მთლიანად ბლოკავს ჰეროინის ეფექტებს, ის იმ პაციენტებს უნდა დაენიშნოთ, რომლებიც ოპიოიდების მთლიანად მოხსნას გეგმავენ; ამდენად, მისი გამოყენება შეზღუდულია და უფრო მოტივირებული პაციენტების სუბპოპულაციით შემოიფარგლება.
სხვა კვლევები და ფუნდამენტური კვლევის შედეგები
ნალტრექსონი შეიძლება უფრო ეფექტიანი იყოს, როცა მკურნალობაში ჩართულნი არიან ოჯახის წევრები და უშუალოდ აკვირდებიან პაციენტის მიერ ნალტრექსონის მიღებას. სხვადასხვა ქვეყანაში ნალტრექსონის გამოყენების კლინიკური გამოცდილება სხვადასხვაა. ზოგიერთ მათგანში მკურნალობის გაგრძელების მაჩვენებელი იგივეა, რაც აგონისტებით მკურნალობისას, ზოგან კი ეს მაჩვენებელი ძალიან დაბალია. ნალტრექსონით მკურნალობის ამგვარ განსხვავებულ ეფექტიანობას შესაძლებელია კულტურული და სოციალური განსხვავებები იწვევდეს. კლინიკური გამოცდილება მიუთითებს, რომ ნალტრექსონი შეიძლება უფრო ეფექტიანი იყოს იმ პაციენტებისათვის, რომლებიც მოტივირებულები არიან, შეწყვიტონ ოპიოიდების მოხმარება - მაგ., პროფესიონალები, რომლებიც სამსახურის დაკარგვის საფრთხის წინაშე არიან ან განსასჯელი პაციენტები, რომლებსაც პატიმრობა ემუქრებათ.
დასკვნა
არსებული მწირი მონაცემები გვიჩვენებს, რომ ოპიოიდებზე დამოკიდებულ იმ პაციენტთა შორის, რომლებმაც შეწყვიტეს ოპიოიდების მოხმარება, ისინი, ვინც ნალტრექსონზე არიან, ნაკლები სიხშირით მოიხმარენ ჰეროინს და ერთვებიან კრიმინალურ საქმიანობაში, იმ პაციენტებთან შედარებით, რომლებიც არ იღებენ ნალტრექსონს. ოპიოიდურ დამოკიდებულებას სიმძიმის სპექტრი აღენიშნება. დამოკიდებულების ადრეულ ეტაპზე ნალტრექსონით მიღებული შედეგი უკეთესია, ვიდრე უფრო მძიმე დამოკიდებულების დროს.
ნალტრექსონის შემთხვევაში მკურნალობის პროგრამაში დარჩენის მაჩვენებელი, ჩვეულებრივ, უფრო დაბალია, ვიდრე ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობის დროს; მიუხედავად ამისა, პაციენტებში, რომლებმაც შეწყვიტეს ოპიოიდების მოხმარება და მოტივირებულები არიან, საბოლოოდ უარი თქვან მათზე, რეციდივის პრევენცია ნალტრექსონით უკეთ ხდება, ვიდრე ნალტრექსონის გარეშე.
რეკომენდაცია ოპიოიდებზე დამოკიდებული პაციენტებისთვის, რომლებიც არ იწყებენ ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას, ოპიოიდების მოხსნის შემდეგ უნდა დაისვას ანტაგონისტით ფარმაკოთერაპიის საკითხი.
|
 |
10.5.2 6.5.2 ნალტრექსონით მკურნალობის ჩვენებები |
▲back to top |
პაციენტის შერჩევა
რეციდივის შემთხვევების დროს, ზედოზირების პოტენციალის გათვალისწინებით, ოპიოიდური ანტაგონისტით მკურნალობა ყველაზე ეფექტიანია იმ პაციენტთა შორის, რომელთაც ოპიოიდებისგან თავშეკავების რეალური შანსი აქვთ (ეს განაცხადი ეყრდნობა ექსპერტების აზრს). ეს ჯგუფები მოიცავს დასაქმებულ პაციენტებს, მათ, ვინც მხოლოდ მოკლე ხანია, რაც ნარკოტიკებს მოიხმარს (მაგ. ახალგაზრდა პაციენტები) და რომლებიც ლეგალური სანქციების საფრთხის წინაშე დგანან.
ნალტრექსონი ყველაზე ეფექტიანია, როცა არსებობს „ახლობელი“, რომელსაც შეუძლია პრეპარატის მიღებაზე ზედამხედველობა; მაგ., ოჯახის წევრი, ახლო მეგობარი ან ზოგიერთ შემთხვევაში - თანამშრომელი.
პაციენტები მძიმე ოპიოიდური დამოკიდებულებით სიფრთხილით უნდა მოეკიდონ ნალტრექსონით მკურნალობას; ასევე, ნალტრექსონი არ არის რეკომენდებული ციროზის დროს, როდესაც Child-ის სიმძიმის სკალის მიხედვით C-თი ან უფრო მაღალი მაჩვენებლით ფასდება.
ნალტრექსონის მოხმარება ორსულებში
მონაცემები ნალტრექსონის ორსულებში მოხმარებაზე შეზღუდულია, მაგრამ თანდაყოლილი პათოლოგიების რისკი, სავარაოდოდ, მცირეა. თუ ქალი, რომელიც ნალტრექსონით მკურნალობს, დაორსულდა, ნალტრექსონის გაგრძელების სარგებელი უნდა შეფასდეს შესაძლო გაუთვალისწინებელ რისკებთან მიმართებით.
ფსიქოსოციალური თერაპიის როლი ნალტრექსონით მკურნალობაში
როგორც სხვა ფარმაკოლოგიური მკურნალობის დროს, ამ შემთხვევაშიც ფსიქოსოციალური მკურნალობა რუტინულად უნდა შევთავაზოთ პაციენტს. მონაცემები არასაკმარისია ნალტრექსონთან კომბინაციაში სპეციფიკური ფსიქოსოციალური მეთოდების გამოყენების შესახებ რეკომენდაციებისათვის; თუმცა, აღმოჩნდა, რომ თავშეკავების შენარჩუნებასა და მკურნალობის პროგრამაში დარჩენაში ნალტრექსონზე მყოფ პაციენტებს ხელს უწყობს გაუთვალისწინებელი შემთხვევების მართვის მეთოდი [171]. მეორე კვლევაში, სტრუქტურირებულ ჯგუფურ კონსულტაციებს არ ჰქონდათ უკეთესი შედეგები, ვიდრე არჩევით არასტრუქტურირებულ ინდივიდუალურ კონსულტაციებს [172]. ერთ-ერთ კვლევაში ერთმანეთს შეადარეს ინდივიდუალური კონსულტაციები ნალტრექსონთან ერთად და ოჯახური კონსულტაციები ნალტრექსონთან ერთად. აღმოჩნდა, რომ ოჯახური კონსულტაციები უკეთესი იყო როგორც მკურნალობის დროს, ისე 12 თვიანი დაკვირვების პერიოდში [173].
6.6 ფსიქოსოციალური ჩარევა
ტერმინი „ფსიქოსოციალური ჩარევა“ ამ შემთხვევაში გულისხმობს ჩარევის ფართო სპექტრს სოციალურ და ფსიქოლოგიურ დონეზე. ჩარევა სოციალურ დონეზე მოიცავს დახმარებას ელემენტარული საჭიროებების უზრუნველყოფაში, როგორებიცაა: საკვები, ტანსაცმელი, საცხოვრებელი და დასაქმება; ასევე, საბაზისო ჯანდაცვა, მეგობრები, საზოგადოება და ბედნიერების შეგრძნება. ჩარევა ფსიქოლოგიურ დონეზე მოიცავს დახმარებას არასტრუქტურირებული დამხმარე ფსიქოთერაპიიდან მოტივაციურ ფსიქოლოგიურ მეთოდებამდე. კლინიცისტებმა და ჯანდაცვის მუშაკებმა უნდა შეარჩიონ, რომელი ფსიქოსოციალური ჩარევა შესთავაზონ პაციენტს. არჩევანი უნდა ემყარებოდეს კვლევის მონაცემებს, თუ რამდენად შეესაბამება მეთოდი პაციენტის ინდივიდუალურ სიტუაციას, რამდენად მისაღებია პაციენტისთვის, არის თუ არა ხელმისაწვდომი შესაბამისი ცოდნის მქონე პერსონალი; ასევე გათვალისწინებულ უნდა იქნეს მოცემული კულტურული თავისებურებები.
 |
10.5.3 6.6.1 ფსიქოლოგიური ჩარევა |
▲back to top |
ამ დოკუმენტის მიზანს არ წარმოადგენს ფსიქოლოგიური ჩარევის სპექტრის ფართო განხილვა. თუმცა, ლიტერატურაში დომინირებს ორი ტიპის თერაპია - კოგნიტურ-ქცევითი თერაპია და გაუთვალისწინებელი შემთხვევების მართვა.
კოგნიტურ-ქცევითი თერაპია მრავალი ფსიქიკური და ქცევითი დაავადების მკურნალობის წამყვანი მეთოდი გახდა. მათ შორის არის ფობიები, შფოთვა და ობსესიურ-კომპულსიური დაავადებები; ეს მეთოდი შეიძლება ეფექტიანი იყოს დეპრესიის და კვებასთან დაკავშირებული აშლილობების დროს. კოგნიტურ-ქცევითი თერაპია წამალდამოკიდებულების დროს დამყარებულია იმ პრინციპზე, რომ ნარკომანია დასწავლილი ქცევაა, რომლის მოდიფიცირებაც შესაძლებელია. კოგნიტური მეთოდები, პირველ რიგში, მიზნად ისახავს დამოკიდებულებითი ქცევის შეცვლას, რაც გულისხმობს იმ მცდარი შემეცნების შეცვლას, რომელიც ხელს უწყობს ქცევის შენარჩუნებას, ან იმ დადებითი შემეცნების ან მოტივაციის ხელშეწყობას, რომელიც შეცვლის ქცევას. ხშირად გამოყენებული ვარიანტებია კოგნიტური თერაპია და მოტივაციის გაზრდის თერაპია.
ქცევითი მეთოდები, უპირველესად, მიზნად ისახავს პირობითი დასწავლით გამყარებული ქცევების მოდიფიცირებას კლასიკური და ოპერაციული განპირობებით. ისინი მოიცავს ჩარევის ტიპებს, რომლებიც მიზნად ისახავს კლასიკურად განპირობებული პასუხის ჩაქრობას (მაგ., მინიშნებასთან კონტაქტის და პასუხის თავიდან აცილება) ან რომლებიც ემყარება ინსტრუმენტულ განპირობებას (მაგ., თემის მხარდაჭერა ან გაუთვალისწინებელი შემთხვევების მართვა) _ მეთოდი, რომლის დროსაც ნარკოტიკზე უარის თქმასთან დაკავშირებული ქცევა საჩუქრით არის წახალისებული. ქცევითი მეთოდები, რომლებიც მოიცავს ავერსიულ განპირობებას, ისტორიულად მნიშვნელოვანია, ძირითადად, ალკოჰოლიზმის მკურნალობაში, მაგრამ ისინი აღარ გამოიყენება ეთიკური მოსაზრებით. კოგნიტური ქცევითი მეთოდებისთვის საჭიროა პერსონალის სწავლება (მაგ., კლინიკური ფსიქოლოგიის სფეროში).
გაუთვალისწინებელი შემთხვევების მართვის დროს ხდება წახალისება ან დასჯა სტრუქტურირებული, გამჭვირვალე მეთოდის გამოყენებით სპეციფიკური ქცევების გამო, რაც აუმჯობესებს სასურველი ქცევების დასწავლას. პროგრამების უმრავლესობა კონცენტრირებულია დადებით ქცევებზე, სასურველი ქცევის განმტკიცებაზე. გაუთვალისწინებელი შემთხვევების მართვის პროგრამებია:
სასურველი ქცევის ნათლად განსაზღვრა (მაგ., ოპიოიდებისგან თავშეკავება);
რეგულარული მონიტორინგი სასურველი ქცევის არსებობა-არარსებობაზე (მაგ., შარდის რეგულარული გამოკვლევა);
სპეციფიკური წახალისება სასურველი ქცევისთვის (მაგ., ფული, ვაუჩერები, სახლში მისაღები მეთადონის დოზები, ან ლატარიის ბილეთები);
დადებითი პიროვნული რეაქცია პერსონალის მხრიდან სასურველი ქცევის გამო.
გაუთვალისწინებელი შემთხვევები პერსონალმა შეიძლება შედარებით მოკლე სწავლების შემდეგ მართოს.
კონსულტანტები უნდა იცნობდნენ არსებულ სოციალურ სერვისებს ან თემში არსებულ სოციალურ რესურსებს.
 |
10.5.4 6.6.2 სოციალური ჩარევა |
▲back to top |
პროფესიული სწავლება
პროფესიული სწავლება მოიცავს პროგრამებს, რომლებიც მიზნად ისახავს პაციენტების დახმარებას სამუშაოს მოძებნასა და შენარჩუნებაში. პროფესიული სწავლება შეიძლება მოიცავდეს ხელობის სწავლას, დაცულ გარემოში მუშაობას და მუშაობის დროს ნარკოტიკების მოხმარებაზე ზედამხედველობას [174, 175, 176].
საცხოვრებელი
საცხოვრებელში იგულისხმება თავშესაფარი უსახლკაროთა ჯგუფისთვის გამოყოფილი ბინიდან უფრო სტაბილურ, ხანგრძლივ საცხოვრებლამდე. საცხოვრებელი მნიშვნელოვანია იმდენად, რამდენადაც მის მოძიებაში დახმარება შეიძლება აუცილებელი იყოს ნარკოტიკებისგან თავშეკავების მცდელობისთვის სათანადო პირობების შესაქმნელად. ნარკომანების ერთ ბინაში განთავსება გარკვეულ რისკებთან არის დაკავშირებული. სასურველია სტაბილური, ნარკოტიკებისგან თავისუფალი გარემოს უზრუნველყოფა. მიღებული სტრატეგიები დამოკიდებული იქნება ადგილობრივ რესურსებზე და ნორმებზე.
საქმიანობა
პაციენტების უნარი, მონაწილეობა მიიღონ და გაერთონ სხვადასხვა საქმიანობით, ფსიქოსოციალური დახმარების მნიშვნელოვანი ასპექტია. პროგრამებს შეუძლია პაციენტებისთვის ხელმისაწვდომი გახადოს ამგვარი ჯანსაღი გასართობი საქმიანობები.
თვითდახმარების ჯგუფები
თვითდახმარების ჯგუფები (ოპიოიდური დამოკიდებულების კონტექსტში) ნებაყოფლობით შექმნილი მცირე ჯგუფებია, რომლებიც ყალიბდება პაციენტებისგან ერთმანეთის ოპიოიდური დამოკიდებულების წინააღმდეგ ბრძოლაში დასახმარებლად. ჩვეულებრივ, სიფხიზლეზე ორიენტირებული პაციენტები ხშირად მატერიალურად და ემოციურად ეხმარებიან ერთმანეთს, ავრცელებენ იდეოლოგიას და ღირებულებებს, რომლებიც წევრებისთვის შეიძლება პიროვნულად უფრო მისაღები იყოს [177].
პაციენტებს, რომლებიც ფარმაკოლოგიურად მკურნალობენ, უნდა ვურჩიოთ, რომ მონაწილეობა მიიღონ თვითდახმარების ჯგუფებში. მართალია, მკურნალობის ამ ფორმაზე ბევრი კვლევა არ არის ჩატარებული, მაგრამ დაკვირვების პრინციპით ჩატარებული კვლევები 12 საფეხურის ჯგუფში (მაგ., ანონიმური ნარკომანები) დადებით შედეგებს იძლევა „მკურნალობაში დაყოვნების“ დადებითი ეფექტებით. მკურნალობის ეს ფორმა ძვირი არ არის და მნიშვნელოვან ფსიქოსოციალურ დახმარებას უზრუნველყოფს.
სწავლება სოციალური ჩვევების შესახებ
სწავლება სოციალური ჩვევების შესახებ მოიცავს მეთოდებს, რომლებშიც სწავლების თეორიის პრინციპები გამოყენებულია სოციალურ და ინტერპერსონალურ სიტუაციებში საჭირო ჩვევების მიღების, განზოგადების და გამძლეობისთვის. სწავლება უნდა ჩატარდეს ყოველდღიური ცხოვრებისეული გამოცდილების კონტექსტში და არა დახურულ, არარეალურ პირობებში.
ტრადიციული მკურნალები
ტრადიციულ და სულიერ მკურნალებს, თუ ისინი კულტურულად მისაღებია პაციენტისთვის, შეიძლება გარკვეული როლი ჰქონდეთ ფსიქოსოციალური დახმარების უზრუნველყოფაში. მართალია, ამ მეთოდების შეფასება სცილდება ამ დოკუმენტის დანიშნულებას, მაგრამ კლინიკურ პერსონალს შეიძლება ჰქონდეს სურვილი, სცადოს ყველა ალტერნატივა, რამაც შეიძლება დახმარება გაუწიოს პაციენტს.
 |
10.5.5 6.6.3 ფსიქოსოციალური დახმარების უზრუნველყოფა |
▲back to top |
პერსონალს და მოხალისეებს ფსიქოსოციალური დახმარება თავიანთი პროფესიონალიზმის შესაბამისად შეუძლიათ. ყველას, ვინც ოპიოიდური დამოკიდებულების მქონე პაციენტს ფსიქოსოციალურ დახმარებას უწევს, სულ ცოტა, გავლილი უნდა ჰქონდეს მოკლე სასწავლო პროგრამა, რათა საკუთარი თავი საფრთხეში არ ჩაიგდონ ან უნებლიე ზიანი არ მიაყენონ ვინმეს. პროფესიონალი პერსონალი სპეციფიკური ფსიქოთერაპიული ტრენინგის გარეშეც, სავარაუდოდ, შეძლებს დამხმარე ფსიქოთერაპიის ან სტრუქტურული თერაპიის ჩატარებას შესაბამისი სახელმძღვანელოს მიხედვით (ხანმოკლე ტრენინგის შემდეგ, მაგ., 1-2 კვირა).
 |
10.6 6.7 ზედოზირების მკურნალობა |
▲back to top |
ოპიოიდური ზედოზირება იდენტიფიცირდება ნიშნების და სიმპტომების კომბინაციით, რაც ვიწრო გუგებსა და სუნთქვის დათრგუნვაში გამოიხატება. დილატირებული გუგები მიუთითებს ალტერნატიულ დიაგნოზზე. ოპიოიდურ ზედოზირებაზე ეჭვმიტანილი პაციენტები მკურნალობას საჭიროებენ, თუ სუნთქვის სიხშირე წუთში 10-ზე ნაკლებია, ან თუ პულსოქსიმეტრიით ჰიპოქსია აღინიშნება (ჟანგბადით გაჯერება <92%-ზე).
ჰიპოქსიური პაციენტების საწყისი მკურნალობა საჭიროების შემთხვევაში უნდა მოიცავდეს ჟანგბადის მიწოდებას და ხელოვნურ ვენტილაციას (ეს, ჩვეულებრივ, მოიცავს სასუნთქი გზების გასუფთავებას და ჟანგბადის ნიღბით მიწოდებას).
ნალოქსონი არასელექციური, ხანმოკლე მოქმედების ოპიოიდური რეცეპტორების ანტაგონისტია, რომელსაც ზედოზირების წარმატებული მკურნალობის ხანგრძლივი კლინიკური ისტორია აქვს. ეს ეფექტიანი ანტიდოტია ხანმოკლე მოქმედების ოპიოიდებით (ჰეროინი) ზედოზირების დროს. ოპიოიდური ზედოზირების მკურნალობისას მთავარია სუნთქვის და ჟანგბადის მიწოდების მოწესრიგება. სუნთქვის გაჩერების შემთხვევაში უნდა ჩატარდეს ხელოვნური ვენტილაცია და ოქსიგენაცია (ნალოქსონის შეყვანამდე ან მისი ეფექტების გამოვლენამდე). ტიპობრივ შემთხვევაში, ადეკვატური სუნთქვა აღდგება ნალოქსონის შეყვანიდან 30 წამში. ნალოქსონის იდეალური დოზა არის ის, რომელიც აუმჯობესებს ვენტილაციას აღკვეთის სიმპტომების გამოწვევის გარეშე. თუ ეჭვი გეპარებათ, უმჯობესია შეცდეთ და ძალიან მაღალი დოზა შეიყვანოთ, ვიდრე ძალიან დაბალი დოზა. ჰეროინით სავარაუდო ზედოზირებისას სტანდარტული დოზა არის 400 მკგ კუნთებში ან 800 მკგ კანქვეშ, რაც, თუ საჭროა, მეორდება 2 წუთის შემდეგ. თუ ინტრავენური შეყვანა შესაძლებელია და პაციენტის ვენტილაცია ადეკვატურია, შესაძლებელია 100 მკგ მცირე ალიქვოტების შეყვანა განმეორებითი დოზების სახით, ვიდრე პაციენტი არ დაიწყებს სუნთქვას წუთში 10-ზე მეტი სიხშირით, ოპიოიდების აღკვეთის სიმპტომების გამოწვევის გარეშე.
ნალოქსონის ძალიან მაღალი საწყისი დოზების (2 მგ) გამოყენებამ შეიძლება აღკვეთის მძიმე სიმპტომები გამოიწვიოს, ღებინებით და ას პირაციის რისკით; ძალიან მაღალი დოზები (>10 მგ) შეიძლება სიცოცხლისთვის საშიშიც კი აღმოჩნდეს [178].
ხანგრძლივი მოქმედების ოპიოიდების ზედოზირების მკურნალობა უფრო რთულია. ამგვარ სიტუაციაში სედაციის ხანგრძლივობა ნალოქსონის ეფექტებს აღემატება. ხანგრძლივი მოქმედების ოპიოიდებით ზედოზირების ყველაზე უსაფრთხო მეთოდი არის ხელოვნური ვენტილაცია, თუკი ეს შესაძლებელია. თუმცა, პაციენტების მკურნალობა ასევე შესაძლებელია ნალოქსონის განმეორებითი ბოლუსური შეყვანით ან ნალოქსონის ინფუზიებით. პაციენტი შეიძლება მოკვდეს, თუ ნალოქსონის ინფუზია რაიმე მიზეზის გამო შეწყდება.
იდეალურ პირობებში პაციენტებს ნალოქსონის შეყვანიდან 2 საათის განმავლობაში უნდა დავაკვირდეთ. პრაქტიკაში ამის მიღწევა რთულია, მაგრამ ძალიან მნიშვნელოვანია პაციენტებისათვის, რომლებთანაც ზედოზირება, სავარაუდოდ, გამოწვეულია ხანგრძლივი მოქმედების ოპიოიდებით.
ზოგიერთ ქვეყანაში პაციენტებს და ოჯახის წევრებს ურიგებენ შპრიცებს ნალოქსონით და ასწავლიან რეანიმაციის ელემენტარულ წესებს [78, 79]. მართალია, ნალოქსონის გამოყენება არასამედიცინო პერსონალის მიერ მაინც რისკთან არის დაკავშირებული [80, 178] და ზოგიერთ ქვეყანაში შეიძლება უკანონოც კი იყოს, მაგრამ ამ მეთოდმა შეიძლება თავიდან აგვაცილოს ზედოზირებით გამოწვეული სიკვდილი. ამგვარი დისტრიბუციის სისტემებს დადებითი შეფასება აქვს [78, 79], მით უფრო, რომ ნალოქსონის მიცემა ოპიოიდური ზედოზირების პრევენციისთვის ფინანსურადაც ხელმისაწვდომია, განსაკუთრებით იქ, სადაც ნალოქსონით შევსებული იაფი შპრიცები გამოიყენება.
 |
10.7 6.8 სპეციალური საკითხები სპეციფიკური ჯგუფებისა და სიტუაციებისთვის |
▲back to top |
 |
10.7.1 6.8.1 პაციენტები აივ/შიდსით, ჰეპატიტით და ტუბერკულოზით |
▲back to top |
როგორც 5.6.8 ნაწილში იყო აღწერილი, ოპიოიდური აგონისტებით მკურნალობა ზრდის ანტიინფექციური აგენტებით მკურნალობის მაჩვენებელს ოპიოიდური დამოკიდებულების მქონე პაციენტებში (უფრო დეტალური განხილვისთვის იხ. ნაწილი 5.6.8).
როცა შემოდის ტუბერკულოზით დაავადებული ნარკოტიკის აქტიური მომხმარებელი, სამკურნალო სამსახურის პირველი პრიორიტეტი უნდა იყოს აქტიური ტუბერკულოზის მკურნალობა მისი შემდგომი გავრცელების თავიდან ასაცილებლად. თუ ოპიოიდური დამოკიდებულების მკურნალობა დაიწყება სხვა პაციენტებისათვის დაავადების გადადების რისკის გარეშე, ეს იდეალური გამოსავალი იქნება. სხვა შემთხვევაში, შეიძლება უმჯობესი იყოს მკურნალობის გადადება, ვიდრე პაციენტი აღარ იქნება გადამდები.
როცა მკურნალობისთვის მოგვმართავს ნარკოტიკის აქტიური მომხმარებელი აივ-ით და ოპიოიდური დამოკიდებულებით, უფრო ადვილია ანტირეტროვირუსული მკურნალობის გადადება პაციენტის ოპიოიდური ჩანაცვლებითი მკურნალობით დასტაბილურებამდე. თუ ნაჩვენებია ანტიბიოტიკებით მკურნალობის დაწყება, მაგ., კო-ტრიმოქსაზოლით ან იზონიაზიდით, ის არ უნდა გადავდოთ.
 |
10.7.2 6.8.2 მოზარდები |
▲back to top |
12-18 წლის მოზარდები მკურნალობის სამსახურს მიმართავენ ოპიოიდური დამოკიდებულების სხვადასხვა სიმძიმით. ზოგიერთი მოზარდი კლინიკაში ოჯახის წევრებს მოჰყავთ. ამ შემთხვევაში ხშირად საქმე გვაქვს უკანასკნელ პერიოდში ნარკოტიკების მავნედ მოხმარებასთან, რასაც ჯერ არ მიუღწევია დამოკიდებულების დონემდე. ბევრი მოზარდი, რომელიც სამკურნალო დაწესებულებაში ხვდება, სოციალურად დაუცველ ფენას განეკუთვნება, ქუჩაში ცხოვრობს და შეიძლება უფრო მეტად იყოს წამალდამოკიდებული, ვიდრე ზრდასრული პაციენტები. ამ ორ ჯგუფს შორის (ოჯახში და ქუჩაში მცხოვრები მოზარდები) არის მესამე ჯგუფი - დისფუნქციურ ოჯახებში მცხოვრები მოზარდები. კვლევები მიუთითებს, რომ, რაც უფრო ადრე იწყება ნარკოტიკების მოხმარება, მით უფრო მაღალია დამოკიდებულების რისკი და ხშირია ჯანმრთელობისთვის მავნე შედეგები [179].
მოზარდებთან მუშაობა მოითხოვს ზოგადად მათ ჯანმრთელობასთან დაკავშირებულ საკითხებთან ფრთხილ მიდგომას, რადგან ნარკოტიკის მოხმარება ხშირად მოზარდის ცხოვრებაში არსებული სხვა პრობლემების შედეგია. შეფასება უნდა იყოს ფართო და მკურნალობა უნდა მოიცავდეს სამედიცინო, ფსიქოლოგიურ, განათლების, ოჯახის და მოზარდის ცხოვრების სხვა ასპექტების შეფასებას. მათი მკურნალობის სპეციალური საჭიროებების გათვალისწინებით, მოზარდები ოპიოიდური დამოკიდებულებით ხშირად მნიშვნელოვან სარგებელს იღებენ სოციალური ჯანმრთელობის სამსახურების უშუალოდ მათკენ მიმართული დახმარებიდან.
მკურნალობის მეთოდები უნდა ითვალისწინებდეს მოზარდებს, რომლებიც ხშირად მიდიან რისკზე, ეძებენ სიახლეს და იმყოფებიან უფრო თანატოლების, ვიდრე მოზრდილების გავლენის ქვეშ (შესაძლოა ინჰიბიტორული კონტროლის არასრული განვითარების გამო). ამრიგად, ფსიქოსოციალური ჩარევა უნდა მოიცავდეს ვარჯიშს თვითკონტროლში, მოქნილობაში და გადაწყვეტილების მიღებაში. მკურნალობის მაქსიმალური ეფექტიანობის უზრუნველსაყოფად, პროგრამა უნდა იყოს ინდივიდუალიზებული და გასაგები, მხედველობაში უნდა მივიღოთ მოზარდის შესაძლებლობები, ფსიქოსოციალური დახმარება, განათლება, ლეგალური და სამედიცინო სტატუსი და ანამნეზი, ასევე, გამოყენებული ნარკოტიკის ტიპი.
ბოლო ხანს ჩატარებულმა კვლევებმა მნიშვნელოვანი ინფორმაცია მოგვაწოდა ოპიოიდებზე დამოკიდებული მოზარდების კლინიკური სიმპტომების შესახებ და გამოავლინა ამ პოპულაციაში თანმხლები ფსიქიატრიული დაავადებების მაღალი სიხშირე. ფსიქიატრიული დაავადებები, რომლებიც ხშირად თან ახლავს ოპიოიდურ დამოკიდებულებას, მოიცავს დეპრესიას, პოსტტრავმულ სტრესულ აშლილობას, ქცევის დარღვევას და ყურადღების დეფიციტით მიმდინარე ჰიპერაქტიურ დაავადებას. ზოგიერთი ეს დაავადება (მაგ., დეპრესიული აშლილობები) უფრო გამოხატულია ოპიოიდდამოკიდებულ მდედრობითი სქესის მოზარდებში, ვიდრე მათ თანატოლ ვაჟებში. გაურკვეველია, რამდენად იწვევს მოზარდთა პოპულაციაში არსებული ფსიქიატრიული დაავადებები „თვითმკურნალობას“ ოპიოიდებით და სხვა მედიკამენტებით; თუმცა, ფაქტია, რომ ფსიქიატრიული თანმხლები დაავადებების და ნარკოტიკების მიღების ერთდროული მართვა კარგ შედეგებს იძლევა.
მოზარდები შეიძლება ცხოვრობდნენ ერთ ან ორ მშობელთან, შეიძლება ჯერ კიდევ მათი ლეგალური მეურვეობის ქვეშ იმყოფებოდნენ. მშობლებს, შეიძლება, მთავარი როლი ჰქონდეთ მოზარდების (ზრდასრული პაციენტებისგან განსხვავებით) წამალდამოკიდებულების სამკურნალო კლინიკაში მოსვლაში. მოზარდებს შეიძლება სჭირდებოდეთ კონსულტაციები ოჯახთან მშობლებთან ურთიერთობის გასაუმჯობესებლად. მშობლებმა უნდა ისწავლონ, როგორ უნდა გაუწიონ მაქსიმალური მხარდაჭერა მოზარდს წამალდამოკიდებულების მკურნალობის დროს. მშობლების ჩარევის მაღალი ხარისხი, მათი იზოლირების საპირისპიროდ, იცავს მოზარდებს ოპიოიდების მოხმარებისგან.
ნარკოტიკებით ექსპერიმენტირება ხშირად მოზარდობის ასაკში იწყება. ამდენად, ნარკომანია (ან წამალდამოკიდებულება) ხშირად განვითარების დაავადებად არის მიჩნეული. ეფექტიანი ჩარევა მოზარდის მიერ ნარკოტიკების მოხმარების დაწყების ადრეულ ეტაპზე უმნიშვნელოვანესია პროგრესირების თავიდან ასაცილებლად. ადრეულ ეტაპზე ჩარევა განსაკუთრებით მნიშვნელოვანია ბოლოდროინდელი კვლევების შედეგების გათვალისწინებით, რომლებიც მიუთითებს, რომ მოზარდებს, ზრდასრულებთან შედარებით, ნარკოტიკების მოხმარების დაწყებიდან მოკლე ხანში უვითარდებათ წამალდამოკიდებულება. გარდა ამისა, ნარკოტიკების მოხმარება მოზარდებში გავლენას ახდენს მათ კოგნიტურ, სოციალურ და ემოციურ განვითარებაზე [15, 180].
ეფექტიანი ადრეული ჩარევა ოპიოიდებზე დამოკიდებულ მოზარდებში, - ფარმაკოთერაპიის და ფსიქოსოციალური მკურნალობის კომბინირება, - შეიძლება დაეხმაროს მოზარდს, თავიდან აიცილოს ნარკოტიკებით ცხოვრება და ინტრანაზალური ან პერორალური ნარკოტიკებიდან ინტრავენურ ოპიოიდებზე გადასვლა. უფრო მეტიც, ადრეულ ფსიქოსოციალურ ჩარევას ახალგაზრდებში, რომლებსაც გამოუყენებიათ ჰეროინი, მაგრამ ჯერ არ არიან ოპიოიდებზე დამოკიდებულები, შეუძლია დაეხმაროს მათ, რომ არ განუვითარდეთ დამოკიდებულება.
განსხვავდება თუ არა ოპიოიდებზე დამოკიდებული მოზარდების ფარმაკოთერაპია მოზრდილების მკურნალობისგან?
ამ საკითხის ირგვლივ სისტემატური კვლევები ვერ მოიძებნა. მოიძებნა ზოგიერთი კლინიკური კვლევა, რომლებიც მხარს უჭერს აგონისტებით ფარმაკოთერაპიას როგორც ოპიოიდების მოხსნისთვის, ისე მხარდამჭერი მკურნალობისთვის. ერთმა რანდომიზებულმა კონტროლირებულმა კვლევამ აჩვენა, რომ კლონიდინის აპლიკაციებთან შედარებით, ბუპრენორფინის კლებითი დოზის მიცემა 28 დღის განმავლობაში უფრო ეფექტიანი იყო მკურნალობის პროგრამაში დარჩენის მხრივ (72%-ი და 39%-ი, შესაბამისად) და ნალტრექსონით მკურნალობის დაწყების თვალსაზრისით(61%-ი და 5%-ი, შესაბამისად) [181].
აგონისტებით ფარმაკოთერაპია კვლავაც რეკომენდებულ მკურნალობად ითვლება მოზარდთა ოპიოიდური დამოკიდებულების დროს. თუმცა, მოზარდები დამოკიდებულების მოკლე პერიოდით და მოზარდები, რომლებიც ოჯახთან ერთად ცხოვრობენ, შეიძლება კარგად დაექვემდებარონ ოპიოიდების აღკვეთას ნალტრექსონით ან მის გარეშე. ეს მიზანშეწონილი ალტერნატივაა. ოპიოიდური აგონისტებით ფარმაკოთერაპია ამ პოპულაციაში ასევე შეიძლება დაიწყოს დროებითი ან საცდელი მკურნალობის სახით. შეიძლება, სულ ხანმოკლე მკურნალობა იყოს საჭირო და კურსი წარმატებით დამთავრდეს.
მკურნალობის ამომწურავი პროგრამა, რომელიც მთელ კლინიკურ პროფილს მოიცავს, უფრო დიდი ალბათობით მოგვცემს დადებით შედეგებს, ვიდრე პროგრამა, რომელიც იზოლირებულად ერთ კლინიკურ პროგრამაზეა ფოკუსირებული.
 |
10.7.3 6.8.3 ქალები |
▲back to top |
აღმოჩნდა, რომ ქალები განსხვავდებიან მამაკაცებისგან ნარკოტიკების მოხმარების ტიპის მიხედვით. ქალები უფრო ნაკლები რაოდენობით მოიხმარენ ნარკოტიკს, მაგრამ უფრო სწრაფად ხდებიან დამოკიდებული, ასევე უფრო ხშირად იყენებენ სედატიურ საშუალებებს. ქალებს, რომლებიც, ოპიოიდებზე დამოკიდებულები ხდებიან, მიღებული აქვთ ნაკლები განათლება, გააჩნიათ ნაკლები ფინანსური რესურსები და სექსუალური და ფიზიკური ძალადობის გამოცდილების უფრო მაღალი მაჩვენებელი [183]. ხშირად, ქალებს წამალდამოკიდებულების მკურნალობისას განსხვავებული მიდგომა ესაჭიროებათ. მათ უფრო ხშირად აქვთ პასუხისმგებლობა ბავშვის მოვლაზე, რის გამოც მათთვის მკურნალობა ნაკლებად ხელმისაწვდომია. მათ შეიძლება, თავი აარიდონ ჯგუფურ ფსიქოსოციალურ საქმიანობას მამაკაცებთან ერთად. ისინი ხშირად აღნიშნავენ სექსუალურ ზეწოლას მამრობითი სქესის პერსონალის მხრიდან [183].
საკმარისი მონაცემები არ მოიპოვება ქალებისთვის სქესსპეციფიკური მკურნალობის ფარდობითი ეფექტიანობის შესაფასებლად. ქალების პროგრამაში ჩასართავად შეიძლება საჭირო გახდეს ინდივიდუალური ან მხოლოდ ქალებისგან შემდგარი კონსულტაციები, ასევე, მნიშვნელოვანია დახმარება დედებისთვის, რომელთაც მცირეწლოვანი შვილები ჰყავთ (მაგ. ბავშვის მოვლის საშუალებების მიწოდება). ზომები უნდა იქნეს მიღებული, რომ პაციენტი ქალები დაცულნი იყვნენ მამრობითი სქესის პერსონალის მხრიდან სექსუალური ზეწოლისგან.
 |
10.7.4 6.8.4 ორსულობა და ძუძუთი კვება |
▲back to top |
ორსულ ან მეძუძურ ქალებში ოპიოიდური აგონისტებით (კერძოდ მეთადონით) მხარდაჭერა ყველაზე მისაღებ მკურნალობად ითვლება. აქ გათვალისწინებულია ნაყოფზე ზემოქმედება, ნეონატალური აღკვეთის სინდრომი და გავლენა ჩვილის მოვლაზე ანტენატალურ პერიოდში. ოპიოიდებზე დამოკიდებულ ქალებს, რომლებიც არ გადიან მკურნალობის კურსს, უნდა ვურჩიოთ ოპიოიდური აგონისტებით ჩანაცვლებითი თერაპიის დაწყება მეთადონით ან ბუპრენორფინით. ორსულ ქალებს, კი რომლებსაც უტარდებათ ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობა, უნდა ვურჩიოთ, რომ არ შეწყვიტონ მკურნალობა ორსულობის განმავლობაში. ბევრ ქალს სურს, შეწყვიტოს ოპიოიდების მიღება, როცა ორსულობის შესახებ იგებენ, მაგრამ ოპიოიდების მოხსნა მეტად სარისკოა, რადგან დიდია ჰეროინის გამოყენების განახლების შანსი, რაც შეზღუდავს ბავშვზე ზრუნვის უნარს. ამასთანავე, ოპიოიდების მოხსნის სიმპტომები შეიძლება მოიცავდეს სპონტანურ აბორტს ორსულობის პირველ ტრიმესტრში ან ნაადრევ მშობიარობას მესამე ტრიმესტრში. ჰეროინის გამოყენების რეციდივმა ორსულობის დროს ასევე შეიძლება არასასურველი შედეგები მოიტანოს სამეანო თვალსაზრისით. მიჩნეულია, რომ ოპიოიდური აგონისტებით ჩანაცვლებით მკურნალობა გაცილებით უსაფრთხოა ბავშვის განვითარებისთვის, ვიდრე დედის მიერ ჰეროინის გამოყენება და ამასთან დაკავშირებული ზიანი.
მეთადონს უპირატესობა ენიჭება ბუპრენორფინთან შედარებით (რადგან მეთადონის უსაფრთხოება ორსულობის დროს უფრო მეტად არის შემოწმებული), მიუხედავად იმისა, რომ როგორც კვლევებმა აჩვენა, ბუპრენორფინს უფრო ნაკლებად ახასიათებს ნეონატალური აღკვეთის სინდრომი, ვიდრე მეთადონს. თუ ქალი ბუპრენორფინით მკურნალობს და კარგი შედეგი აქვს, მხედველობაში უნდა მივიღოთ უკვე მიმდინარე ეფექტიანი მკურნალობა.
მეორე და მესამე ტრიმესტრში შეიძლება საჭირო გახდეს მეთადონის დოზის გაზრდა გაზრდილი მეტაბოლიზმის და მოცირკულირე სისხლის მოცულობის გამო. ამ პერიოდში ოპიოიდების უფრო ადეკვატური ჩანაცვლება შეიძლება მოხდეს დღეში ორი 12 საათიანი დოზის მიცემით. მშობიარობის შემდეგ შეიძლება საჭირო გახდეს მეთადონის დოზის დარეგულირება, რადგან ზემოთ აღნიშნული ცვლილებები უკუგანვითარდება.
მართალია, მეთადონი და ბუპრენორფინი ქალის რძეში აღმოჩნდება, მაგრამ ძალიან მცირე რაოდენობით, რაც ჩვილზე მნიშვნელოვან გავლენას არ ახდენს. ძუძუთი კვებას, მეორე მხრივ, ბევრი დადებითი აქვს, მათ შორის დედა-შვილს შორის კონტაქტი, ბავშვის კვება და დაავადებების თავიდან აცილება. ოპიოიდებზე დამოკიდებულ დედებს უნდა ვურჩიოთ ძუძუთი კვება. თუ დედა აივ დადებითია ან იყენებს ალკოჰოლს, კოკაინს და ამფეტამინის ტიპის პრეპარატებს, საჭირო გახდება სპეციფიკური რჩევის მიცემა.
მკურნალობის გარეშე ნეონატალურმა აღკვეთის სინდრომმა შეიძლება ბავშვის მნიშვნელოვანი დისტრესი გამოიწვიოს, იშვიათ შემთხვევებში - გულყრებიც. კოქრეინის კოლაბორაციის მიმოხილვა მიუთითებს, რომ ოპიოიდები და ბარბიტურატები უფრო ეფექტიანია, ვიდრე პლაცებო და ბენზოდიაზეპინები; ამასთან, ოპიოიდები შესაძლოა უფრო ეფექტიანია, ვიდრე ბარბიტურატები.
რეკომენდაცია ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა გამოყენებულ უნდა იქნეს ორსულობის დროს ოპიოიდური დამოკიდებულების სამკურნალოდ.
რეკომენდაცია ორსულობის დროს, ოპიოიდური დამოკიდებულების მკურნალობისას, მეთადონით მხარდაჭერას უპირატესობა უნდა მიენიჭოს ბუპრენორფინთანშედარებით; მიუხედავად იმისა, რომ ბუპრენორფინის უსაფრთხოების ნაკლები მონაცემები არსებობს, მისი შეთავაზებაც შესაძლებელია.
|
 |
10.7.5 6.8.5 ოპიუმის მომხმარებლები |
▲back to top |
ოპიუმზე დამოკიდებულ ადამიანებს, რომლებსაც ამასთან დაკავშირებული უარყოფითი შედეგები აწუხებთ, შეიძლება ჩაუტარდეთ ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობა იმავე სახით, როგორც სხვა ოპიოიდებზე დამოკიდებულების დროს ტარდება. ორმა კვლევამ აჩვენა ამ პოპულაციაში ბუპრენორფინის ეფექტიანობა [184, 185].
მნიშვნელოვანია ოპიუმის მწეველის ოპიუმზე დამოკიდებულების კრიტერიუმებთან შესაბამისობის უზრუნველყოფა. თუ ეს საკითხი გარკვეული არ არის, შეიძლება მიზანშეწონილი იყოს, ოპიუმის მწეველმა ჯერ დეტოქსიკაცია სცადოს, შემდეგ კი ოპიოიდური აგონისტებით მხარდამჭერი ჩანაცვლებითი მკურნალობა.
 |
10.7.6 6.8.6 მანქანის მართვა და ტექნიკასთან მუშაობა |
▲back to top |
მეთადონით ან ბუპრენორფინით მკურნალობის დაწყებისას შეიძლება აღინიშნოს ოპიოიდური ინტოქსიკაცია. პაციენტებს უნდა ვურჩიოთ, სედაციის მდგომარეობაში არ მართონ ავტომანქანა. ასევე, რადგან პაციენტებმა არ იციან, რა გავლენას მოახდენს მათზე მეთადონის და ბუპრენორფინის პირველი რამდენიმე დოზა, უმჯობესი იქნება, ამ პერიოდშიც არ მართონ ავტომანქანა ან რაიმე სახის აპარატურა.
 |
10.7.7 6.8.7 ფსიქიატრიული თანმხლები დაავადებები ოპიოიდური დამოკიდებულების დროს |
▲back to top |
ფსიქიატრიული დაავადებები ხშირია ოპიოიდური დამოკიდებულების დროს; კერძოდ, მკურნალობის ადრეულ ეტაპზე და შემდეგ რეგულარულად განსაკუთრებული ყურადღება უნდა მიექცეს დეპრესიას, შფოთვას, პიროვნულ და პოსტტრავმულ სტრესულ აშლილობებს. როგორც სომატური თანმხლები დაავადებების დროს, მკურნალობას უკეთესი შედეგი ექნება, თუ იგი იმავე ექიმის მიერ იმავე დაწესებულებაში ტარდება ინტეგრირებული სერვისის სახით. თუ ეს არ ხერხდება, უნდა დამყარდეს მჭიდრო კავშირი სხვა კლინიკებთან, რათა გაადვილდეს პაციენტების გაგზავნა და შეიქმნას მუშაობის ერთობლივი სტრუქტურა; ამ დროს ყურადღება უნდა მიექცეს, რომელი ფსიქოაქტიური პრეპარატები ენიშნება პაციენტს, რის შესახებ თავად პაციენტიც საქმის კურსში უნდა იყოს.
 |
10.7.8 6.8.8 დამოკიდებულება რამდენიმე ნივთიერებაზე |
▲back to top |
მე-12 დანართში ჩამოთვლილია ოპიოიდების, ალკოჰოლის, ბენზოდიაზეპინების, სტიმულატორების და კანაფის მწვავე და ქრონიკული ურთიერთქმედება რამდენიმე ნივთიერებაზე დამოკიდებულების მკურნალობა შეიძლება დაიწყოს ოპიოიდური აგონისტებით მხარდამჭერი თერაპიით ოპიოიდებზე დამოკიდებულების კომპონენტისთვის, თუ აუცილებელია, სტაციონარის პირობებში. ამავე დროს, პაციენტს უტარდება მკურნალობა ალკოჰოლის, ბენზოდიაზეპინების და სტიმულატორების მოხსნისთვის.
ბენზოდიაზეპინების მაღალი დოზების მოსახსნელად შეიძლება აუცილებელი იყოს ამის თანდათანობით გაკეთება. თუ ბენზოდიაზეპინები ეძლევა ოპიოიდური აგონისტებით მხარდამჭერი ამბულატორიული მკურნალობის კურსში ჩართულ პაციენტებს, ეს სიფრთხილით უნდა გაკეთდეს, რადგან ამ პრეპარატების ხანგრძლივ მოხმარებაზე ბევრი მონაცემი არ არსებობს და ისინი ზრდის სედატიური ზედოზირების რისკს. თუ ბენზოდიაზეპინების უსაფრთხო მოხსნისთვის ბენზოდიაზეპინების კლებადი დოზებია დანიშნული, რეცეპტი უნდა გაიცეს ერთი და იმავე ექიმის მიერ, ხოლო დოზა კი, თუ ეს შესაძლებელია, იმავე ადგილიდან, საიდანაც მეთადონი. პაციენტებს უნდა ვურჩიოთ, არ დაასრულონ ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა ბენზოდიაზეპინების მიღების შეწყვეტამდე.
 |
10.8 6.9 ტკივილის მართვა ოპიოიდური დამოკიდებულების მქონე პაციენტებში |
▲back to top |
 |
10.8.1 6.9.1 მწვავე ტკივილი |
▲back to top |
ოპიოიდური დამოკიდებულების მქონე პაციენტებში ტკივილი ხშირად მწვავდება ტკივილის ზღურბლის დაქვეითების გამო, რაც ოპიოიდების მიმართ ტოლერანტობით არის გამოწვეული. ისინი უფრო რეზისტენტულები არიან ტკივილის ოპიოიდებით მკურნალობის მცდელობისას. ეს გამოწვეულია ან ოპიოიდების მიმართ მათი ტოლერანტობით ან ოპიოიდური დამოკიდებულების სამკურნალო პრეპარატების მაბლოკირებელი ეფექტებით (მათ შორის ბუპრენორფინი და ნალტრექსონი). ოპიოიდებზე დამოკიდებულ პაციენტებს აქვთ უფლება, მოითხოვონ ტკივილის ადეკვატურად მოხსნა. თუმცა, ზოგიერთი პაციენტი ცდილობს პერსონალის მანიპულირებას ოპიოიდის მიღების მიზნით. ზომები, რომლებსაც შეუძლია მსგავსი ქმედების მინიმუმამდე შემცირება, მოიცავს შემდეგს:
ტკივილის მართვა ერთ სამედიცინო დაწესებულებაში (საავადმყოფო ან პირველადი ჯანდაცვის დაწესებულება - სიმძიმის მიხედვით);
ტკივილის ბუნების ადეკვატური განსაზღვრა;
მწვავე ტკივილის სწრაფად მოხსნა და შემდეგ უფრო ხანგრძლივად მოქმედ ოპიოიდებზე გადასვლა, რომლებსაც არადანიშნულებით გამოყენების ნაკლები პოტენცია აქვს და იძლევა სტაბილურ ოპიოიდურ ეფექტებს (ინტოქსიკაციის და აღკვეთის ციკლური პატერნისგან განსხვავებით).
კლინიკური შეფასება გამოყენებულ უნდა იქნეს ოპიოიდური აღკვეთის მდგომარეობის გასარჩევად ოპიოიდური ინტოქსიკაციისგან. შესაბამისი დოზის განსაზღვრისათვის საჭიროა ოპიოიდების ტიტრაცია ტკივილზე ზემოქმედების მიხედვით აღკვეთის მდგომარეობის და ინტოქსიკაციის კლინიკურ ნიშნებზე დაკვირვებით.
პაციენტები, რომლებიც არ გადიან აგონისტებით მხარდამჭერ მკურნალობას
პაციენტებისთვის, რომლებიც იყენებენ აკრძალულ ოპიოიდებს და არ გადიან ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობის კურსს, ამ მკურნალობის მეთადონით დაწყება არის როგორც ოპიოიდური დამოკიდებულების, ისე ტკივილის მკურნალობის საშუალება. არაადეკვატური ანალგეზიის შემთხვევაში პაციენტი ცდილობს აკრძალული ოპიოიდების გამოყენებას.
პაციენტები, რომლებიც მკურნალობენ ანტაგონისტით (ნალტრექსონი)
პაციენტებს, რომლებიც ნალტრექსონით მკურნალობენ, ჩვეულებრივი გზით შეყვანილ ოპიოიდურ ანალგეტიკებზე შედეგი არ ექნებათ. მსუბუქი ტკივილის დროს, არაოპიოიდური ანალგეტიკები (მაგ., პარაცეტამოლი და არასტეროიდული ანთების საწინააღმდეგო პრეპარატები) უნდა გამოვიყენოთ. ამ პაციენტებს არც ოპიოიდების შემცველი პრეპარატებისგან (ხველის, გაციების საწინააღმდეგო და ანტიდიარეული) ექნებათ რაიმე სახის ეფექტი. გადაუდებელ სიტუაციაში ტკივილის მართვა შეიძლება მოიცავდეს: რეგიონულ ანალგეზიას; სედაციას არაოპიოიდური პრეპარატებით, როგორებიცაა: ბენზოდიაზეპინები ან კეტამინი და ზოგადი ანესთეზიის არაოპიოიდური მეთოდების გამოყენებას. ელექტიური ქირურგიული მკურნალობის დროს, თუ მოსალოდნელია, რომ საჭირო გახდება ოპიოიდური ანალგეზია, ნალტრექსონის მიღება უნდა შეწყდეს, სულ მცირე, 72 საათით ადრე ოპერაციის (მათ შორის სტომატოლოგიური ოპერაცია) დაწყებამდე. ქირურგმა ან მკურნალმა ექიმმა უსათუოდ უნდა იცოდეს, რომ პაციენტი ნალტრექსონს იღებდა. ამის შემდეგ, ვიდრე ნალტრექსონით მკურნალობა განახლდება, პაციენტმა სამიდან შვიდ დღემდე პერიოდის განმავლობაში არ უნდა მიიღოს ოპიოიდები - ხანგრძლივობა დამოკიდებულია გამოყენებული ოპიოიდის ნახევარდაშლის პერიოდზე. თუ ეჭვი გეპარებათ, შეგიძლიათ ჩაატაროთ ნალოქსონის ტესტი, რათა განსაზღვროთ რეკომენდებულია თუ არა ნალტრექსონი ოპიოიდების აღკვეთის სინდრომის ინდუქციის გარეშე.
პაციენტები, რომლებიც იღებენ ნაწილობრივ აგონისტებს (ბუპრენორფინი)
რადგან ბუპრენორფინს ოპიოიდური რეცეპტორების მიმართ მაღალი აფინურობა ახასიათებს, ამ პრეპარატით ნამკურნალებ პაციენტებს ტკივილის მკურნალობისთვის უფრო მაღალი ეფექტიანობის ოპიოიდური აქტივობა ესაჭიროებათ. მაღალი აფინურობის ოპიოიდური აგონისტი ფენტანილი ამ სიტუაციაში შეიძლება უფრო ეფექტიანი იყოს, ვიდრე სხვა ოპიოიდები. მსუბუქი ტკივილისთვის შეიძლება ეფექტიანი იყოს ბუპრენორფინის დოზის გაზრდა ან სუსტი ოპიოიდების (მაგ. ტრამადოლი) დამატება, თუმცა ეს მეთოდი სისტემურად გამოკვლეული არ არის.
მწვავე ტკივილის დროს, რომელიც ზემოთ მოცემულ მკურნალობას არ ექვემდებარება, შეიძლება ვცადოთ შემდეგი ვარიანტები:
ბუპრენორფინის შეწყვეტა და სრული ოპიოიდური აგონისტის, მაგ., მეთადონის ან მორფინის გამოყენება, ტკივილის მოხსნის შემდეგ ისევ ბუპრენორფინზე გადასვლა.
ბუპრენორფინის გაგრძელება ოპიოიდების მაღალ დოზებთან ერთად (მაგრამ რადგან დროთა განმავლობაში ბუპრენორფინის მაბლოკირებელი ეფექტი მცირდება, ყურადღება უნდა მიექცეს, არ მოხდეს ზედოზირება, თუ ბუპრენორფინის მიცემა შეწყდა და ოპიოიდების მაღალი დოზით მიცემა გრძელდება).
ბუპრენორფინის გაგრძელება და არაოპიოიდური ანალგეზიის გამოყენება, როგორიცაა კეტამინის გადასხმა; ან კლონიდინის თუ ბენზოდიაზეპინების დამატებით გამოყენება.
პაციენტები, რომლებიც იღებენ სრულ აგონისტებს (მეთადონი)
მსუბუქი ან მწვავე ტკივილისთვის სცადეთ არაოპიოიდური ანალგეტიკები (მაგ., პარაცეტამოლი). თუ პარენტერალური ანალგეტიკებია საჭირო, მიმართეთ არასტეროიდულ ანთებისსაწინააღმდეგო კეტოროლაკს. ოპერაციული ჩარევის დროს რეკომენდებულია ტკივილის მართვა საავადმყოფოში. მეთადონზე მყოფი პაციენტები მწვავე ტკივილის დროს საავადმყოფოში ხშირად იღებენ ოპიოიდების არაადეკვატურ დოზებს. ამ პაციენტებისთვის ანალგეზიის იმავე მეთოდებით უნდა ვისარგებლოთ, რაც სხვა პაციენტებისთვის გამოიყენება; ეს მეთოდები მოიცავს ინექციურ და პაციენტის მიერ კონტროლირებულ ანალგეზიას. ოპიოიდების მიმართ ტოლერანტობის გამო, მეთადონზე მყოფ პაციენტს ოპიოიდური ანალგეზიისთვის უფრო მაღალი დოზები დასჭირდება ტკივილის ადეკვატურად მოსახსნელად.
ნაკლებად უნდა გამოვიყენოთ ნაწილობრივი აგონისტები (ბუპრენორფინი), რადგან მათ შეუძლია აღკვეთის სიმპტომების დაჩქარება. არსებობს მონაცემები მეთადონსა და ანესთეზიურ აგენტებს შორის ჯვარედინი ტოლერანტობის შესახებ; ამდენად, მეთადონზე მყოფ პაციენტებს სტომატოლოგიური ან ქირურგიული პროცედურების დროს შეიძლება დასჭირდეთ ანესთეზიური საშუალებების უფრო მაღალი დოზები. პაციენტებისთვის, რომელთაც მეთადონი ქრონიკული ტკივილის სამკურნალოდ სჭირდებათ, უნდა შემუშავდეს ტკივილის მართვის ინდივიდუალური გეგმა, რომელშიც გათვალისწინებული იქნება სპეციალისტის აზრი.
 |
10.8.2 6.9.2 ქრონიკური ტკივილი |
▲back to top |
ბოლო პერიოდში მსოფლიოს ზოგიერთ ნაწილში ოპიოიდების ფართო გამოყენება ქრონიკული ტკივილის მკურნალობისთვის [186] მიუთითებს, რომ ქრონიკული ტკივილის მკურნალობასა და დანიშნულ ოპიოიდებზე დამოკიდებულების განვითარებას შორის მნიშვნელოვანი კავშირი არსებობს. ამ დოკუმენტის მიზანი არ არის ქრონიკული ტკივილის მკურნალობისას ოპიოიდების გამოყენების საკითხის განხილვა. თუმცა, პაციენტები ქრონიკული ტკივილით, რომლებიც მოიხმარენ ამ მიზნით დანიშნულ ოპიოიდებს და აკმაყოფილებენ ოპიოიდებზე დამოკიდებულების კრიტერიუმებს (ანუ მდგომარეობა აღემატება მხოლოდ ტოლერანტობის და აღკვეთის სინდრომის კრიტერიუმებს), ხშირად იგზავნებიან (ან თვითონ მიდიან) ოპიოიდური დამოკიდებულების სამკურნალო დაწესებულებებში. ჩვეულებრივ, ისინი შემოდიან პრობლემებით, როგორებიცაა დანიშნული ოპიოიდების ვენაში შეყვანა და გამოწერილზე უფრო დიდი რაოდენობით ოპიოიდების მიღება (რაც იწვევს ინტოქსიკაციას ან ზედოზირებას). ისინი აგრეთვე შეიძლება შემოვიდნენ ოპიოიდების არადანიშნულებით გამოყენებაზე მიმანიშნებელი სხვა მახასიათებლებით, რასაც თვითონ პაციენტი ზოგჯერ უარყოფს.
ამ პაციენტების მკურნალობის დროს პირველი ნაბიჯი იმის განსაზღვრა იქნება, თუ რამდენად ამომწურავად იქნა გამოკვლეული ტკივილის (როგორც ფიზიკური, ისე ფსიქოლოგიური) მიზეზი და რამდენად სწორად არის ნამკურნალები ფიზიკური მიზეზები. პაციენტებისთვის, რომლებიც არ სარგებლობენ ოპიოიდური აგონისტებით ჩანაცვლებითი მკურნალობით, შემდეგი ნაბიჯი იქნება მეთადონის ან ბუპრენორფინის დანიშვნა ზედამხედველობით, ნაცვლად ოპიოიდების ზედამხედველობის გარეშე მიღებისა. ამით უზრუნველყოფილი იქნება სტაბილური ოპიოიდური ეფექტების მიღწევა, აღკვეთის და ინტოქსიკაციის ციკლების თავიდან აცილება. როცა ტკივილი გრძელდება, მიუხედავად ოპიოიდური აგონისტებით ადეკვატური მხარდამჭერი თერაპიისა, უნდა დაისვას ოპიოიდური როტაციის საკითხი.
ზოგიერთ შემთხვევაში ოპიოიდებით მკურნალობა შეიძლება აღარ იყოს ეფექტიანი მათი არადანიშნულებით მოხმარების ან იმის გამო, რომ ტკივილი შეიძლება მწვავდებოდეს ოპიოიდებით ინდუცირებული ჰიპერალგეზიით [187]. ოპიოიდებით გამოწვეული ჰიპერალგეზიის სამკურნალოდ შეიძლება დაისვას ოპიოიდების მოხსნის საკითხი, თუმცა, ამან შეიძლება გამოიწვიოს აკრძალული ოპიოიდების გამოყენების განახლება.
ზომები, რომლებიც შეიძლება მივიღოთ სამედიცინო მიზნით დანიშნული ოპიოიდების არასათანადო გამოყენების თავიდან ასაცილებლად, მოიცავს შემდეგს: სისტემის შემუშავება, რომლის მიხედვითაც ოპიოიდური ანალგეზია ჩატარდება ყოველთვის ერთი და იმავე ექიმის მიერ; დოზაზე ზედამხედველობა; იმგვარი ფორმების გამოწერა, რომლებიც ნაკლებად ექვემდებარება არადანიშნულებით გამოყენებას (მაგ.., თხევადი მეთადონი) და პაციენტის ყურადღებით შერჩევა.
 |
11 დანართი 1. არსებული მონაცემები |
▲back to top |
მონაცემები მიღებულია GRADE-ის სამუშაო ჯგუფის მეთოდის გამოყენებით დასმული საკითხების ირგვლივ არსებული მონაცემების ხარისხის განსაზღვრისათვის. დამატებითი ინფორმაცია ამ მეთოდის შესახებ მოცემულია სამუშაო ჯგუფის მასალებში, სადაც მითითებულია მონაცემების ხარისხი.
A1.1 აქვს თუ არა მეთადონს ეფექტი ოპიოიდური დამოკიდებულების მკურნალობისას?
GRADE-ის მონაცემები
ავტორები: ლ. ამატო
თარიღი: 23 აგვისტო, 2006
კითხვა: თერაპიის რომელი ტიპი უნდა გამოვიყენოთ ოპიოიდური დამოკიდებულების დროს - მეთადონით მხარდამჭერი მკურნალობა თუ ოპიოიდების მოხსნა? თუ ოპიოიდური დამოკიდებულების მკურნალობა საერთოდ არ არის საჭირო?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Mattick RP et al. (გამოქვეყნების პროცესში) მეთადონით მხარდამჭერი თერაპია ოპიოიდური დამოკიდებულების ჩანაცვლებითი თერაპიის გარეშე დატოვებასთან შედარებით (CLIB 3, 2003) [105], Bargagli AM et al. (2007) ოპიოიდური დამოკიდებულების მკურნალობაზე ჩატარებული ობსერვაციული კვლევების სისტემატური მიმოხილვა [197].
(ამ დანართში „- 1“ მიუთითებს, რომ ქულა შემცირებულია ერთი ერთეულით სუსტი მონაცემების გამო).
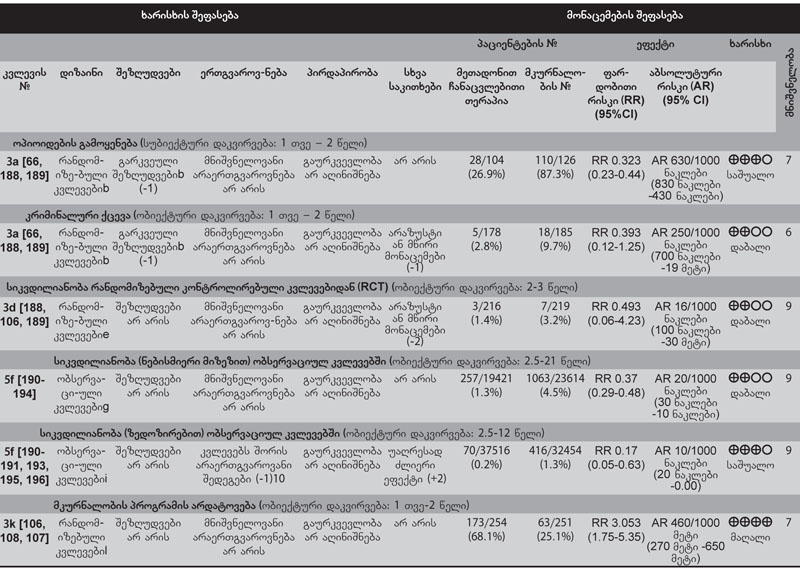
a სამი კვლევა ამბულატორიულ პირობებში; ორი ჩატარდა შეერთებულ შტატებში, ერთი კი - შვედეთში.
b სამი რანდომიზებული კონტროლირებული კვლევა: ერთი ადეკვატური დაფარვით, ერთი გაურკვეველი და ერთი არაადეკვატური დაფარვით.
c რანდომული ეფექტის მოდელი.
d სამი რანდომიზებული კონტროლირებული კვლევა; ერთი ჩატარდა შეერთებულ შტატებში, ერთი - შვედეთში, ერთი კი - ჩინეთში.
e ერთი ადეკვატური და ორი გაურკვეველი დაფარვით.
f ხუთი კვლევა ამბულატორიულ პირობებში; ჩატარდა იტალიაში, ავსტრალიაში, შვედეთში, შეერთებულ შტატებში და ესპანეთში (თითოეულში თითო კვლევა).
g კვლვების ხარისხი ნიუკასლი-ოტავას სკალის გამოყენებით: შერჩევა - ორი კვლევა შეფასდა 3, ხოლო სამი კვლევა, - 2 ქულით; შედარება - ერთი კვლევა შეფასდა 3, სამი კვლევა - 1, ერთი კი - 0 ქულით.
h ხუთი კვლევა ამბულატორიულ პირობებში: ორი ჩატარდა ნიდერლანდებში, თითო კი - იტალიაში, შეერთებულ შტატებში და ესპანეთში.
i კვლევების ხარისხი ნიუკასლი-ოტავას შკალის გამოყენებით: შერჩევა - ოთხი კვლევა შეფასდა 3, ხოლო ერთი კვლევა - 2 ქულით; შედარებაა - ორი კვლევა შეფასდა 2, სამი კვლევა კი - 1 ქულით; გამოსავალი - ერთი კვლევა შეფასდა 2, ოთხი კვლევა კი - 1 ქულით.
j მაღალი სტატისტიკური ჰეტეროგენობა პ<0.00001, მაგრამ ყველგან იყო ერთგვაროვანი შედეგი.
k სამი კვლევა ამბულატორიულ პირობებში, ჩატარებული ჰონგ-კონგში (ტაილანდი) და შეერთებულ შტატებში (თითო კვლევა ორივე ქვეყანაში).
l სამი რანდომიზებული კონტროლირებული კვლევა, ყველა გაურკვეველი დაფარვით.
A1.2 ამცირებს თუ არა აივ-ის გავრცელებას ოპიოიდური აგონისტებით მხარდამჭერი მკურნალობა?
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 22 მაისი, 2006
კითხვა: უნდა გამოვიყენოთ თუ არა აგონისტებით მხარდამჭერი მკურნალობა აივ ინფექციის პრევენციისთვის და მაღალი რისკის მატარებელი ქცევის შესამცირებლად?
პაციენტები ან პოპულაცია: საინექციო ოპიოიდებზე დამოკიდებული ადამიანები მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Gowing L et al. (2004) ჩანაცვლებითი თერაპია საინექციო ოპიოიდების მომხმარებლებისათვის აივ ინფექციის პრევენციის მიზნით (CLIB 4, 2004) [203]
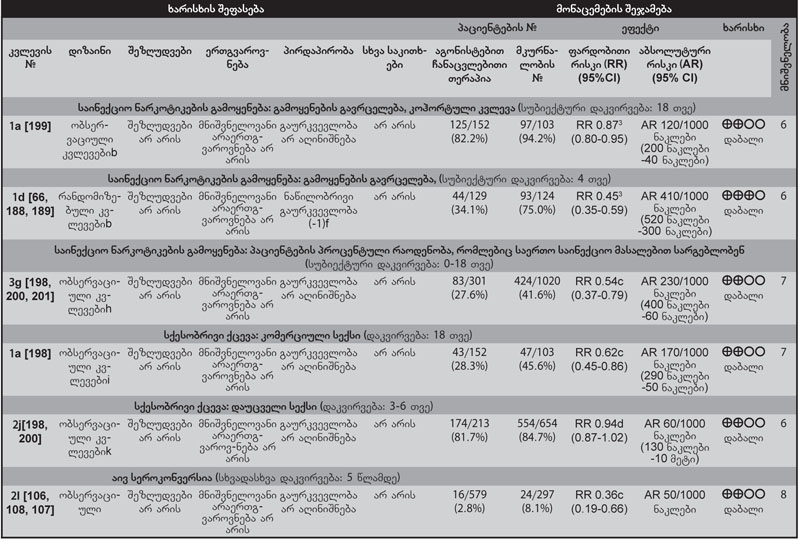
a ერთი კვლევა ამბულატორიულ პირობებში; ჩატარდა შეერთებულ შტატებში (Metzger, 1993) [193].
b ერთი აღწერილობითი კვლევა, რომელშიც ავტორმა კვლევის ხარისხი შეაფასა ექვსი პუნქტის მიხედვით (პოპულაციის აღწერა, შერჩევის კრიტერიუმების აღწერა, confounding-ის დარეგულირება, 20%25-ზე ნაკლები დანაკარგი დაკვირვების დროს, თანაჩარევის არსებობა, ჯგუფებს შორის მონაცემების შეგროვებაში შეუთავსებლობა) 0-დან 1-მდე, სადაც 0=ტენდენციურობის არარსებობას ნიშნავს. ამ შეფასების სისტემით კვლევა შეფასდა 1 ქულით.
c რანდომული ეფექტის მოდელი.
d ერთი კვლევა ჩატარდა ავსტრალიაში ამბულატორიულ პირობებში (ციხეში).
e კვლევა შეფასდა 1 ქულით (იხ. სქოლიო 2).
f ოპიოიდდამოკიდებული პატიმრები.
გ სამივე კვლევა ჩატარდა ამბულატორიულ პირობებში, ორი შეერთებულ შტატებში, ერთი - გერმანიაში.
h სამი კოჰორტული კვლევა, ორი შეფასდა 1, ერთი კი - 2 ქულით (იხ. სქოლიო 2).
i ერთი კოჰორტული კვლევა შეფასდა 1 ქულით (იხ. სქოლიო 2).
j ორივე ამბულატორიული, ერთი ჩატარდა შეერთებულ შტატებში, ერთი - გერმანიაში.
k ორივე შეფასდა 1 ქულით (იხ. სქოლიო 2).
l ორი კოჰორტული კვლევა: Metzger (1993) [198] საკონტროლო ჯგუფი, შერჩეული მეთადონის ჯგუფის მიერ და Moss (1994) [202] საკონტროლო ჯგუფი, შერჩეული ოპიოიდების მოხსნის ჯგუფიდან.
A1.3 აქვს თუ არა ბუპრენორფინს ეფექტი ოპიოიდური დამოკიდებულების მკურნალობისას?
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 23 მაისი, 2006
კითხვა: არის თუ არა ეფექტიანი ბუპრენორფინით მხარდამჭერი მკურნალობა პლაცებოსთან შედარებით ოპიოიდური დამოკიდებულების დროს?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული და სტაციონარული
სისტემატური მიმოხილვა: Mattick RP et al. ბუპრენორფინით მხარდამჭერი თერაპია თუ მეთადონით მხარდამჭერი თერაპია ოპიოიდური დამოკიდებულების დროს (2008, გამოქვეყნების პროცესში) [118]
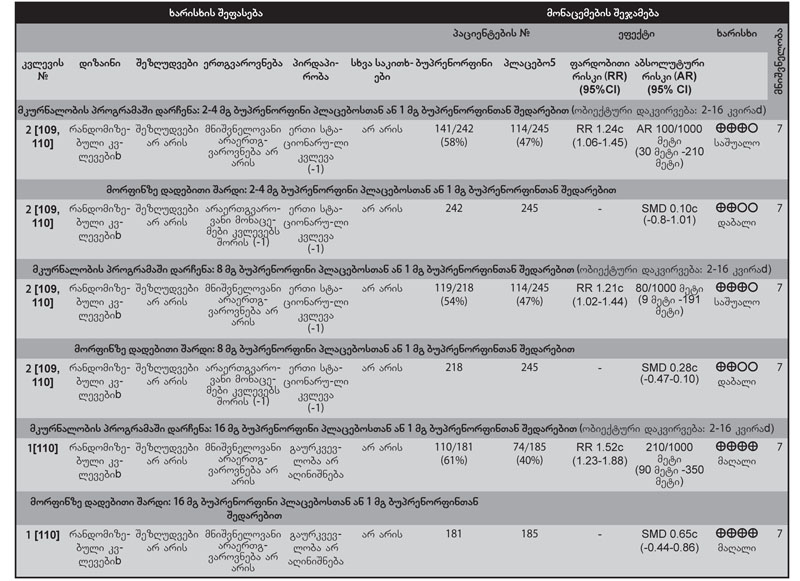
a ორი რანდომიზებული კონტროლირებული კვლევა, ერთი ამბულატორიული, ორივე ჩატარდა შეერთებულ შტატებში.
b ორივე დაუზუსტებელი დაფარვით.
c რანდომული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e პლაცებო ან დღეში 1 მგ ბუპრენორფინი.
A1.4 მეთადონი ბუპრენორფინთან შედარებით
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 22 მარტი, 2006
კითხვა: რას უნდა მოვანიჭოთ უპირატესობა ოპიოიდური მხარდამჭერი თერაპიის დროს: ბუპრენორფინის თავისუფალ დოზებს თუ მეთადონის თავისუფალ დოზებს?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Mattick RP et al. ბუპრენორფინით მხარდამჭერი თერაპია თუ მეთადონით მხარდამჭერი თერაპია ოპიოიდური დამოკიდებულების დროს (2008, გამოქვეყნების პროცესში) [118]

a ყველა ამბულატორიული; ქვეყნები, სადაც ეს კვლევები ჩატარდა: სამი - შეერთებულ შტატებში, ერთი - ავსტრიაში, ერთი -შვეიცარიაში, ერთი - ავსტრალიაში, ერთი - გაერთიანებულ სამეფოში.
b ორი კვლევა ადეკვატური დაფარვით, ხუთი დანარჩენისთვის ეს ინფორმაცია არ არის; 5/7 ორმაგი ბრმა.
c რანდომული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e ყველა ამბულატორიული; ქვეყნები, სადაც ეს კვლევები ჩატარდა: სამი - შეერთებულ შტატებში, ერთი - ავსტრიაში, ერთი - ავსტრალიაში, ერთი შვეიცარიაში.
g 5/6 ორმაგი ბრმა; ერთი ადეკვატური დაფარვით, ხუთზე ინფორმაცია არ არის.
h მონაცემები დამყარებულია შარდის ანალიზზე.
i ყველა ამბულატორიული; ქვეყანა, სადაც ეს კვლევები ჩატარდა: სამი - შეერთებულ შტატებში, ერთი - ავსტრიაში, ერთი - ავსტრალიაში.
j 4/5 ორმაგი ბრმა; ერთი ადეკვატური დაფარვით, ხუთზე ინფორმაცია არ არის.
j ყველა ამბულატორიული; ქვეყანა, სადაც ეს კვლევები ჩატარდა: ორი შეერთებულ შტატებში, ერთი ავსტრიაში, ერთი ავსტრალიაში.
k 3/4 ორმაგი ბრმა; ერთი ადეკვატური დაფარვით, ხუთზე ინფორმაცია არ არის.
k ამბულატორიული, ჩატარდა ავსტრალიაში.
m ორმაგი ბრმა, ადეკვატური დაფარვით.
n მხოლოდ ერთი კვლევა სტატისტიკურად არამნიშვნელოვანი შედეგებით.
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 23 მარტი, 2006
კითხვა: რას უნდა მოვანიჭოთ უპირატესობა ოპიოიდური დამოკიდებულების მკურნალობის დროს: ბუპრენორფინის მხარდამჭერ საშუალო დოზებს (6-12 მგ/დღეში) თუ მეთადონის მხარდამჭერ საშუალო დოზებს (50-80 მგ/დღეში)?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Mattick RP et al. ბუპრენორფინით მხარდამჭერი თერაპია თუ მეთადონით მხარდამჭერი თერაპია ოპიოიდური დამოკიდებულების დროს (2008, გამოქვეყნების პროცესში) [118]

a ყველა ამბულატორიული; ექვსი ჩატარდა შეერთებულ შტატებში, ერთი - იტალიაში.
b ყველა ორმაგი ბრმა, ერთი კვლევა ადეკვატური დაფარვით, სხვებისთვის ეს ინფორმაცია არ არის.
c მაღალი ჰეტეროგენურობა პ = 0.04.
d რანდომული ეფექტის მოდელი.
e მკურნალობის ხანგრძლივობა.
f ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
g დამყარებული შარდის ანალიზზე.
h სამი ორმაგად ბრმა, ერთი ადეკვატური დაფარვით, სხვების შესახებ ინფორმაცია არ არის.
i ამბულატორიული, ჩატარდა შეერთებულ შტატებში.
j ორმაგი ბრმა, დაფარვის შესახებ ინფორმაცია არ არის.
k მხოლოდ ერთი კვლევა, რამდენიმე პაციენტი, შედეგები არ არის სტატისტიკურად მნიშვნელოვანი.
A1.5 მეთადონის როგორი შემანარჩუნებელი დოზები უნდა გამოვიყენოთ?
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 24 მარტი, 2006
კითხვა: მეთადონის რა დოზით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების დროს მხარდამჭერი მკურნალობისას: 40-59 მგ/ დღეში თუ 1-39 მგ/დღეში?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Faggiano F et al. მეთადონით მხარდამჭერი თერაპია სხვადასხვა დოზის გამოყენებით ჰეროინზე დამოკიდებულების დროს (CLIB 3, 2003) [140]

a ამბულატორიული; ჩატარდა შეერთებულ შტატებში.
b ორმაგი ბრმა კვლევისა და დაფარვის შესახებ ინფორმაცია არ არის.
c მხოლოდ ერთი კვლევა.
d ფიქსირებული ეფექტის მოდელი.
e ერთი კონტროლირებული პროსპექტული კვლევა, ამბულატორიული, ჩატარდა ჰოლანდიაში; კონტროლირებული პროსპექტული კვლევისთვის საშუალო დოზები = 55-70 მგ/დღეში, დაბალი დოზები = 5-55 მგ/დღეში.
f ერთი საშუალო ხარისხის კონტროლირებული პროსპექტული კვლევა.
g დიდი საიმედოობის ინტერვალი.
h კონტროლირებული პროსპექტული კვლევა.
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 24 მარტი, 2006
კითხვა: მეთადონის რა დოზით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების დროს მხარდამჭერი მკურნალობისას: 60-120 მგ/ დღეში თუ 1-39 მგ/დღეში?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Faggiano F et al. მეთადონით მხარდამჭერი თერაპია სხვადასხვა დოზის გამოყენებით ჰეროინზე დამოკიდებულების დროს (CLIB 3, 2003) [140]

a მნიშვნელოვანი ჰეტეროგენურობა.
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 24 მარტი, 2006
კითხვა: მეთადონის რა დოზით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების დროს მხარდამჭერი მკურნალობისას: 60-120 მგ/ დღეში თუ 40-59 მგ/დღეში?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Faggiano F et al. მეთადონით მხარდამჭერი თერაპია სხვადასხვა დოზის გამოყენებით ჰეროინზე დამოკიდებულების დროს (CLIB 3, 2003) [140]

a ორივე ამბულატორიული და ორივე ჩატარდა აშშ-ში.
b ორივე ორმაგი ბრმა, დაფარვის შესახებ ინფორმაცია არ არის.
c ფიქსირებული ეფექტის მოდელი.
d ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
e ადეკვატური დაფარვა, 2 უცნობია; 2 ორმაგი ბრმა, 1 ერთმაგი ბრმა.
f ამბულატორიული, ჩატარდა აშშ-ში.
g შარდის ანალიზზე დამყარებული.
h ორმაგი ბრმა, დაფარვა უცნობია.
i მხლოდ ერთი კვლევა, დაფარვა უცნობია.
j მკურნალობის განმავლობაში.
k ამბულატორიული, ჩატარდა აშშ-ში.
l კრიმინალური აქტივობის საშუალო რაოდენობა კვირაში.
m 1 კონტროლირებული პროსპექტული კვლევა, ჩატარებული ჰოლანდიაში. პროსპექტული კონტროლირებული კვლევები მაღალი დოზების გამოყენებით =>75 მგ/დღეში, საშუალო დოზა = 55-70 მგ/დღეში.
n 1 კონტროლირებული პროსპექტული კვლევა, საშუალო ხარისხის.
o რამდენიმე შემთხვევა.
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 24 მარტი, 2006
კითხვა: მეთადონის რომელი მაღალი დოზით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების დროს მხარდამჭერი მკურნალობისას: > 109 მგ/დღეში თუ 60-109 მგ/დღეში?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Faggiano F et al. მეთადონით მხარდამჭერი თერაპია სხვადასხვა დოზის გამოყენებით ჰეროინზე დამოკიდებულების დროს (CLIB 3, 2003) [140]

a ორივე ამბულატორიული და ორივე ჩატარდა აშშ-ში.
b ორივე ორმაგი ბრმა, დაფარვის შესახებ ინფორმაცია არ არის.
c ფიქსირებული ეფექტის მოდელი.
d ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
e ადეკვატური დაფარვა, 2 უცნობია; 2 ორმაგი ბრმა, 1 ერთმაგი ბრმა.
f ამბულატორიული, ჩატარდა აშშ-ში.
g შარდის ანალიზზე დამყარებული.
h ორმაგი ბრმა, დაფარვა უცნობია.
i მხლოდ ერთი კვლევა, დაფარვა უცნობია.
j მკურნალობის განმავლობაში.
k ამბულატორიული, ჩატარდა აშშ-ში.
l კრიმინალური აქტივობის საშუალო რაოდენობა კვირაში.
m 1 კონტროლირებული პროსპექტული კვლევა, ჩატარებული ჰოლანდიაში. პროსპექტული კონტროლირებული კვლევები მაღალი დოზების გამოყენებით =>75 მგ/დღეში, საშუალო დოზა = 55-70 მგ/დღეში.
n 1 კონტროლირებული პროსპექტული კვლევა, საშუალო ხარისხის.
o რამდენიმე შემთხვევა.
GRADE-ის მონაცემები
ავტორები: ლ. ამატო, ს. მინოზი
თარიღი: 24 მარტი, 2006
კითხვა: მეთადონის რომელი მაღალი დოზით უნდა ვისარგებლოთ ოპიოიდური დამოკიდებულების დროს მხარდამჭერი მკურნალობისას: > 109 მგ/დღეში თუ 60-109 მგ/დღეში?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პირები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Faggiano F et al. მეთადონით მხარდამჭერი თერაპია სხვადასხვა დოზის გამოყენებით ჰეროინზე დამოკიდებულების დროს (CLIB 3, 2003) [140]

a ამბულატორიული, ჩატარდა აშშ-ში.
b ერთმაგად ბრმა, ადეკვატური დაფარვა.
c 1 კვლევა, რამდენიმე მონაწილე.
d ფიქსირებული ეფექტის მოდელი.
A1.6 მეთადონის კლებადი დოზების გამოყენება ალფა 2 ადრენერგულ აგონისტებთან შედარებით ოპიოიდების მოხსნის დროს
GRADE-ის მონაცემები
ავტორ(ებ)ი: ლ. ამატო
თარიღი: 2 თებერვალი, 2006
კითხვა: რომლის გამოყენებაა უმჯობესი ოპიოიდების მომხმარებლებში: მეთადონის კლებადი დოზების თუ ალფა 2 ადრენერგული აგონისტების?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული ნებისმიერი პაციენტი, რომელსაც სურს ოპიოიდების მიღების შეწყვეტა
მკურნალობის ტიპი: ამბულატორიული ან სტაციონარული
სისტემატური მიმოხილვა: Gowing L; ალფა 2 ადრენერგული აგონისტები ოპიოიდების მოხსნის მართვისთვის (CLIB 4, 2004) [222], Amato etal; მეთადონის კლებადი დოზები ოპიოიდების მოხსნის მართვისთვის (CLIB 3, 2005) [222].
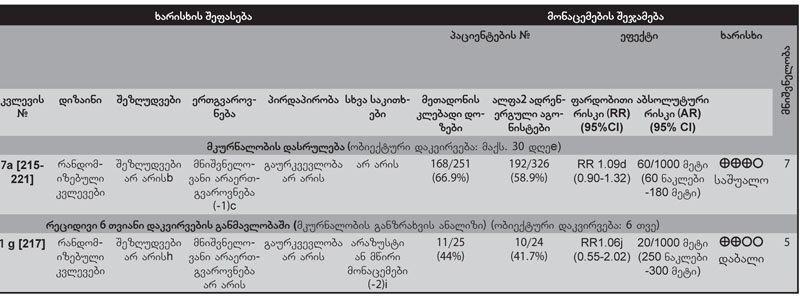
a 5/7 კვლევა ჩატარდა სტაციონარულ პირობებში, 2 ამბულატორიულად; ქვეყნები, სადაც კვლევები ჩატარდა: აშშ (3), გაერთიანებული სამეფო (2), ესპანეთი (2). კიდევ ორი კვლევაა, რომელშიც ეს საკითხია განხილული, მაგრამ ეს ობსერვაციული კვლევებია და ამიტომ ისინი მეტაანალიზიდან გამოირიცხა.
b 2/7 კვლევა ადეკვატური დაფარვით, 5/7-ში მეთოდი გაურკვეველია; ყველა ორმაგად ბრმა.
c მნიშვნელოვანი ჰეტეროგენურობა: პ = 0.0045 და არანაირი სტატისტიკურად მნიშვნელოვანი შედეგები.
dრანდომული ეფექტის მოდელი.
e მკურნალობის ხანგრძლივობა.
f შეტყობინების ხარისხი ამ გამოსავლისთვის იყო ძალიან ცუდი. შედეგების შეტყობინების ტიპი იყო მეტად ჰეტეროგენური და ხელს უშლიდა შედეგების მეტაანალიზისთვის დაჯგუფებას. შვიდიდან ოთხმა კვლევამ აჩვენა, რომ ალფა 2 ადრენერგულ აგონისტებს უფრო ძლიერი ჰიპოტენზიური ეფექტი აქვს, ვიდრე მეთადონს.
g კვლევა ჩატრდა აშშ-ში ამბულატორიულ პირობებში.
h ორმაგად ბრმა, დაფარვა უცნობია.
i მხოლოდ ერთი კვლევა რამდენიმე მონაწილით (49).
j ფიქსირებული ეფექტის მოდელი.
A1.7 მედიკამენტები ოპიოიდების მოხსნისთვის
GRADE-ის მონაცემები
ავტორ(ებ)ი: ლ. ამატო
თარიღი: 2 თებერვალი, 2006 16.01.56
კითხვა: რომლის გამოყენებაა უმჯობესი ოპიოიდებზე დამოკიდებულ პაციენტებში: მეთადონის კლებადი დოზების თუ ბუპრენორფინის კლებადი დოზების?
პაციენტები ან პოპულაცია: ოპიოიდების მომხმარებლები
მკურნალობის ტიპი: ამბულატორიული ან სტაციონარული
სისტემატური მიმოხილვა: Gowing et al. ბუპრენორფინი ოპიოიდების მოხსნის მართვისთვის (CLIB 2, 2006) [159], Amato et al; მეთადონის კლებადი დოზები ოპიოიდების მოხსნის მართვისთვის (CLIB 3, 2005) [224].

a ორივე კვლევა ჩატარდა სტაციონარის პირობებში - გერმანიაში (1) და აშშ-ში (1).
b 2/2 დაფარვის შესახებ ინფორმაცია გაურკვეველია, ორივე ორმაგი ბრმა.
c რანდომული ეფექტის მოდელი.
d ცოტა პაციენტი (63).
e კვლევა ჩატარდა აშშ-ში სტაციონარის პირობებში.
f ორმაგი ბრმა, დაფარვის შესახებ ინფორმაცია გაურკვეველია.
g მხოლოდ ერთი კვლევა მონაწილეთა მცირე რაოდენობით (39).
h მკურნალობის ხანგრძლივობა.
GRADE-ის მონაცემები
ავტორ(ებ)ი: ლ. ამატო
თარიღი: 13/09/2007
კითხვა: რომლის გამოყენებაა უმჯობესი ოპიოიდების მოხსნის დროს: ბუპრენორფინის კლებადი დოზების თუ ალფა 2 ადრენერგული აგონისტების?
პაციენტები ან პოპულაცია: ოპიოიდების მომხმარებლები
მკურნალობის ტიპი: ამბულატორიული ან სტაციონარული
სისტემატური მიმოხილვა: Gowing et al. ბუპრენორფინი ოპიოიდების მოხსნის მართვისთვის (CLIB 2, 2006) [159].
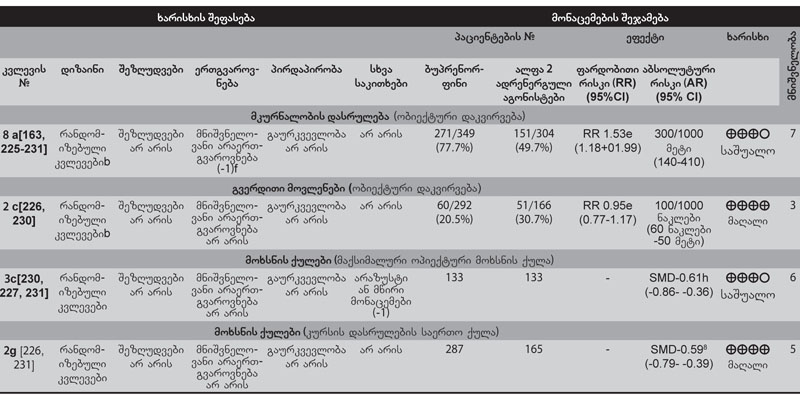
a 8 კვლევა, 5 ჩატარდა აშშ-ში, 1 - ავსტრალიაში, 1 - ინდოეთში და 1 - იტალიაში.
b დაფარვის მხრივ 3 შეფასდა, როგორც ა, 6 ბ და 1 ც.
c 3 კვლევა, 1 ჩატარდა ავსტრალიაში, 2 - აშშ-ში.
d რანდომიზებული კონტროლირებული კვლევა. 1 შეფასდა, როგორც ა, 1 როგორც ბ.
e რანდომული ეფექტის მოდელი.
f მნივნელოვანი ჰეტეროგენურობა.
g 2 კვლევა, ერთი ჩატარდა აშშ-ში, 1 - ავსტრალიაში.
h ფიქსირებული ეფექტის მოდელი.
A1.8 უნდა გამოვიყენოთ თუ არა ანტაგონისტები მინიმალური სედაციით ოპიოიდების მოხსნისთვის
GRADE-ის მონაცემები
ავტორ(ებ)ი: მ. დავოლი, ლ. ამატო
თარიღი: 2 თებერვალი, 2006
კითხვა: საჭიროა თუ არა ოპიოიდების ანტაგონისტების გამოყენება მინიმალური სედაციით ოპიოიდების მოხსნის დროს?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პაციენტები, რომლებიც ოპიოიდების მართვითი მოხსნის პროცესში იმყოფებიან
მკურნალობის ტიპი: სტაციონარული
სისტემატური მიმოხილვა: Gowing et al. ოპიოიდების ანტაგონისტების გამოყენება მინიმალურ სედაციასთან ერთად ოპიოიდების მოხსნის დროს (CLIB 1, 2006) [160].

a ქვეყნები, სადაც კვლევები ჩატარდა: იტალია (2), გაერთიანებული სამეფო (1) და აშშ (1); 3 კვლევა ჩატარდა ამბულატორიულ პირობებში, 1 სტაციონარის პირობებში.
b 3/4 დაფარვის შესახებ ინფორმაცია არ არის, 1/4-ში არაადეკვატურია; 2 ორმაგად ბრმა, 2-ში ინფორმაცია დაფარვის შესახებ მოცემული არ არის.
c სტატისტიკურად მნიშვნელოვანი ჰეტეროგენურობა.
d რანდომული ეფექტის მოდელი.
e მკურნალობის ხანგრძლივობა.
f ამასთანავე, დიდი განსხვავებაა მკურნალობის სქემებსა და დამატებითი თერაპიის ტიპს შორის.
g განსაზღვრულია სუბიექტური სიმპტომების საფუძველზე სხვადასხვა სკალების გამოყენებით, რაც ხელს უშლის მონაცემების დაჯგუფებას.
h 2 კონტროლირებული პროსპექტული კვლევა, ორივე ჩატარდა აშშ-ში და ამბულატორიულ პირობებში.
i დაფარვის შესახებ ინფორმაცია ერთ კვლევაში საკმარისი არ არის, დაფარვა არაადეკვატურია მეორე კვლევაში.
j RR 3-ზე მაღალია.
k კვლევა ჩატარდა იტალიაში აბულატორიულ პირობებში.
l დაფარვა გაურკვეველია.
m მხოლოდ ერთი კვლევა, რამდენიმე მონაწილე (98) და ჩატარდა აბულატორიულ პირობებში.
n ობსერვაციული კვლევები.
A1.9 უნდა გამოვიყენოთ თუ არა ოპიოიდების ანტაგონისტები ღრმა სედაციით ან ანესთეზიით ოპიოიდების მოხსნის დროს?
GRADE-ის მონაცემები
ავტორ(ებ)ი: მ. დავოლი, ლ. ამატო
თარიღი: 2 თებერვალი, 2006
კითხვა: საჭიროა თუ არა ოპიოიდების ანტაგონისტების გამოყენება ღრმა სედაციის ფონზე ოპიოიდების მოხსნის დროს?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პაციენტები, რომელთაც უტარდებათ ოპიოიდების მართვითი მოხსნა
მკურნალობის ტიპი: სტაციონარული
სისტემატური მიმოხილვა: Gowing et al. ოპიოიდების ანტაგონისტების გამოყენება ღრმა სედაციის ან ანესთეზიის ფონზე ოპიოიდების მოხსნის დროს (CLIB 2, 2006) [161].

a ქვეყნები, სადაც 2 კვლევა ტარდება: აშშ (1), ავსტრალია (1), ორივე იყო სტაციონარული.
b არც ერთ კვლევაში არ იყო მოცემული დაფარვის მეთოდი, 1 კვლევა იყო ერთმაგად ბრმა (პაციენტები), ხოლო მეორეში ბრმა მეთოდი გამოყენებული არ იყო.
c ფიქსირებული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e გამოსავალი ამ კონტექსტში შესაბამისი არ არის.
f კვლევა ჩატარდა აშშ-ში სტაციონარის პირობებში.
g დაფარვის მეთოდი მოცემული არ არის, ბრმა მეთოდი გამოყენებული არ არის.
h მხოლოდ ერთი კვლევა და მონაცემები დამყარებული თვითშეტყობინებაზე.
i 2 რანდომიზებულ კონტროლირებულ კვლევაში, რომლითაც შეისწავლეს მოხსნის სიმპტომები და ხანგრძლივობა, გამოყენებულ იქნა თვითშეტყობინება და დოზაზე არადამოკიდებული ეფექტი.
j მხოლოდ ერთი კვლევა და რამდენიმე მონაწილე (106).
k ეს არის შესაბამისი გამოსავალი.
l დოზაზე დამოკიდებული ეფექტი ნაჩვენებია 2 რანდომიზებულ კონტროლირებულ კვლევაში, სადაც შედარებულია სხვადასხვა დოზები.
m მონაცემები ემყარება კვლევას, სადაც პაციენტების დიდ ნაწილზე დაკვირვების განხორციელება ვერ მოხერხდა.
n მხოლოდ ორი კვლევა, ცოტა მონაწილე (78).
A1.10 ოპიოიდების მოხსნა სტაციონარის პირობებში უნდა ჩატარდეს თუ ამბულატორიულ პირობებში?
GRADE-ის მონაცემები
ავტორ(ებ)ი: ლ. ამატო
თარიღი: 2 თებერვალი, 2006
კითხვა: მკურნალობის რომელი მეთოდია უმჯობესი ოპიოიდური დეტოქსიკაციის დროს: სტაციონარული დეტოქსიკაცია თუ ამბულატორიული დეტოქსიკაცია?
პაციენტები ან პოპულაცია: ოპიოიდების მომხმარებლები
მკურნალობის ტიპი: სტაციონარული ამბულატორიულთან შედარებით
სისტემატური მიმოხილვა: Day E. et al. სტაციონარული მკურნალობის გამოყენება დეტოქსიკაციისთვის ოპიოიდური დამოკიდებულების
დროს სხვა პირობებთან შედარებით (CLIB 2, 2005) [168].

a ეს კვლევა ჩატარდა აშშ-ში.
b რანდომიზაციის მეთოდთან დაკავშირებით აღინიშნება მნიშნელოვანი მეთოდოლოგიური პრობლემები.
c ფიქსირებული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e ძალიან მცირე რაოდენობით მონაწილე (40).
A1.11 უნდა გამოვიყენოთ თუ არა ანტაგონისტებით (ნალტრექსონით) ფარმაკოთერაპია ოპიოიდური დამოკიდებულების დროს?
GRADE-ის მონაცემები
ავტორ(ებ)ი: ს. მინოზი, ლ. ამატო
თარიღი: 23 მარტი, 2006
კითხვა: უნდა გამოვიყენოთ თუ არა პერორალური ნალტრექსონი ოპიოიდური დამოკიდებულების დროს?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პაციენტები
მკურნალობის ტიპი: სტაციონარული
სისტემატური მიმოხილვა: Minozzi et al. პერორალური ნალტრექსონით მკურნალობა ოპიოიდური დამოკიდებულების დროს (CLIB 1, 2006) [170].

a ამბულატორიული. კვლევა ჩატარდა: ისრაელში - 2, აშშ-ში - 1, რუსეთში - 1, ესპანეთში - 1.
b 2 ადეკვატური დაფარვა, სხვა კვლევაში ინფორმაცია არ არის; ყველა ორმაგად ბრმა.
c ფიქსირებული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e ყველა ამბულატორიული. ჩატარდა: ისრაელში - 2, აშშ-ში - 1, ჩინეთში - 1, რუსეთში - 1, ესპანეთში - 1.
f ემყარება შარდის ანალიზს.
g 2 ადეკვატური დაფარვა, სხვა კვლევაში ინფორმაცია არ არის; ყველა ორმაგად ბრმა. ITT ანალიზი გამოყენებული არ არის.
h ორივე ამბულატორიული, ერთი ჩატარდა ისრაელში, მეორე - ესპანეთში.
i 1 ადეკვატური დაფარვით, 1 გაურკვეველი, ორივე ორმაგად ბრმა.
j რამდენიმე პაციენტი, შედეგები სტატისტიკურად მნიშვნელოვანი არ არის.
k ყველა ამბულატორიული, ჩატარდა აშშ-ში, ჩინეთში და რუსეთში.
l 1 ჩატარდა ადეკვატური დაფარვით, 2-ში დაფარვა გაურკვეველია, ყველა ჩატარდა ორმაგი ბრმა მეთოდით.
m სუბიექტების რაოდენობა, სულ ცოტა, ერთი გვერდითი ეფექტით.
n ორივე ამბულატორიული და ორივე ჩატარდა აშშ-ში.
o ხელახლა ციხეში მოხვედრილების რაოდენობა.
p გაურკვეველი დაფარვა და ღია დიზაინი.
q 2 კვლევა, პაციენტების მცირე რაოდენობა
A1.12 საჭიროა თუ არა ფსიქოსოციალური მკურნალობის გამოყენება ფარმაკოლოგიურ ჩანაცვლებით თერაპიასთან ერთად?
GRADE-ის მონაცემები
ავტორ(ებ)ი: ლ. ამატო, ს. მინოზი
თარიღი: 23 მარტი, 2006
კითხვა: რომლის გამოყენებაა უმჯობესი ოპიოიდური დამოკიდებულების დროს: ფსიქოსოციალური და ფარმაკოლოგიური მხარდამჭერი თერაპიის კომბინაციის თუ მხოლოდ ფარმაკოლოგიური მხარდამჭერი თერაპიის?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პაციენტები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Amato et al. ფსიქოსოციალურ დახმარებასთან კომბინირებული აგონისტებით მხარდამჭერი მკურნალობა თუ მხოლოდ აგონისტებით მხარდამჭერი მკურნალობა ოპიოიდური დამოკიდებულების დროს (CLIB 4, 2004) [257].

a ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
b ერთის გარდა ყველაში დაფარვა გაურკვეველია, 1 არაადეკვატურია; 2 ორმაგად ბრმა.
c ფიქსირებული ეფექტის მოდელი.
d მკურნალობის ხანგრძლივობა.
e არაადეკვატური დაფარვის მქონე კვლევის გამორიცხვა არ ცვლის შედეგს.
f ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
g შარდის ანალიზზე დაყრდნობით.
h ყველა გაურკვეველი დაფარვით, 1 ორმაგი ბრმა.
i რანდომული ეფექტის მოდელი.
j ყველა ამბულატორიული და ყველა ჩატარდა აშშ-ში.
k ყველა გაურკვეველი დაფარვით, 1 ორმაგად ბრმა.
l ორივე ამბულატორიული და ორივე ჩატარდა აშშ-ში.
m 1 ორმაგად ბრმა, 2 გაურკვეველი დაფარვით.
n ორი კვლევა ურთიერთსაპირისპირო შედეგებით.
A1.13 არის თუ არა ფარმაკოლოგიურ მკურნალობასთან კომბინირებული ფსიქოსოციალური დახმარება უფრო ეფექტიანი მხოლოდ ფარმაკოლოგიურ მკურნალობასთან შედარებით ოპიოიდების მოხსნის დროს?
GRADE-ის მონაცემები
ავტორ(ებ)ი: ს. ჰილი, მ. დავოლი, ლ. ამატო
თარიღი: 2 თებერვალი, 2006
კითხვა: მკურნალობის რომელ სახეობას უნდა მივმართოთ ოპიოიდური დამოკიდებულების მქონე პაციენტებში რომლებსაც ოპიოიდების მოხსნა სურთ: ფარმაკოლოგიური და ფსიქო-სოციალური დახმარების კომბინაციას თუ მხოლოდ ფარმაკოლოგიურ მკურნალობას?
პაციენტები ან პოპულაცია: ოპიოიდებზე დამოკიდებული პაციენტები
მკურნალობის ტიპი: ამბულატორიული
სისტემატური მიმოხილვა: Amato et al. ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა მხოლოდ ფარმაკოლოგიურ მკურნალობასთან შედარებით ოპიოიდური დეტოქსიკაციის დროს (CLIB 2, 2004) [169].

a ყველა კვლევა ჩატარდა აშშ-ში, ყველა ამბულატორიულ პირობებში.
b ოთხი კვლევა გაურკვეველი დაფარვით და ერთი არაადეკვატური დაფარვით; 2 კვლევა ერთმაგად ბრმა (მონაწილეებისთვის დაფარული იყო მხოლოდ ფარმაკოლოგიური მკურნალობა), ხოლო 3 კვლევის დაფარვის მონაცემები მოწოდებული არ იყო.
c ფიქსირებული ეფექტის მოდელი.
d მგრძნობელობის ანალიზის ჩატარება არაადეკვატური დაფარვის მქონე კვლევის (კლასი C) გამორიცხვით მეტაანალიზიდან (Robles 2002, 48 მონაწილე) [262]. შედეგი არ შეიცვალა და სარწმუნო უპირატესობა დარჩა კომბინირებული მკურნალობის სასარგებლოდ (RR 0.46 (95%25-ი CI 0.27-0.79).
e მკურნალობის ხანგრძლივობა.
f ყველა კვლევა გაურკვეველი დაფარვით, 2 ერთმაგად ბრმა და 1 დაბრმავების გარეშე.
g პაციენტების მცირე რაოდენობა (109).
h კვლევა ჩატარდა აშშ-ში ამბულატორიულ პირობებში (Bიცკელ 1997) [258].
i გაურკვეველი დაფარვა, ერთმაგად ბრმა.
j მხოლოდ ერთი კვლევა, რამდენიმე მონაწილე და ფართო საიმედოობის ინტერვალი.
k შეთავაზებული მკურნალობის რეჟიმების დაბალი განზოგადებადობა.
l მხოლოდ ერთი კვლევა, რამდენიმე მონაწილე.
m მგრძნობელობის ანალიზის ჩატარება არაადეკვატური დაფარვის მქონე კვლევის (კლასი C) გამორიცხვით მეტაანალიზიდან (Yandoli 2002, 119 მონაწილე) [263]. შედეგი გახდა სტატისტიკურად არასარწმუნო (RR 0.84 (95%25 -ი CI 0.68-1.04).
n არაადეკვატური დაფარვა, ღია კვლევა.
o რამდენიმე პაციენტი და ფართო საიმედოობის ინტერვალი.
p კვლევა ჩატარდა აშშ-ში ამბულატორიულ პირობებში (Yandoli, 2002) [263].
 |
12 დანართი 2. განაწილება, დოზირება და რეცეპტის გამოწერა |
▲back to top |
A2.1 განაწილება
მეთადონი და ბუპრენორფინი შესაძლებელია განაწილდეს სხვადასხვა კლინიკურ ან თემზე ორიენტირებულ დაწესებულებებში.
სპეციალიზებული კლინიკის პირობებში, ადგილზე არსებულ აფთიაქში ან გასაცემ პუნქტში თითოეული დოზა პაციენტს შეიძლება ზედამხედველობით მიეცეს. ზედამხედველობა ნიშნავს, რომ კლინიკის პერსონალი ინტენსიურად აკვირდება და სრულყოფილად აფასებს პაციენტს. განაწილება შეიძლება მოხდეს სათემო აფთიაქებში, ზოგ ქვეყანაში ბუპრენორფინი პირდაპირ ექიმის კაბინეტიდან გაიცემა.
წამლის გამცემ პერსონალს დიდი წვლილის შეტანა შეუძლია მულტიდისციპლინური მკურნალობის დაგეგმვაში, რომელიც კლინიკის პირობებში უკეთესად ტარდება. თემის პირობებში, სადაც აგონისტებით სათემო აფთიაქებში მკურნალობენ, სამედიცინო პერსონალს უნდა ვურჩიოთ, რეგულარულად ესაუბრონ ფარმაცევტს პაციენტების შესახებ იმის გამოსავლენად, თუ რამდენი დოზა გამოტოვა ან აღენიშნებოდა თუ არა პაციენტს ინტოქსიკაცია, როდესაც დოზის მისაღებად მოდიოდა. თუ აფთიაქი (საიდანაც მეთადონი ან ბუპრენორფინი გაიცემა) არ ეკუთვნის დაწესებულებას, სადაც ხდება მეთადონის ან ბუპრენორფინის გამოწერა, პაციენტს მკურნალობის დაწყებამდე უნდა ვაცნობოთ, რომ ამ აფთიაქთან კომუნიკაცია მკურნალობის შემადგენელი ნაწილია.
მეთადონი და ბუპრენორფინი საიმედო სეიფში უნდა იყოს შენახული ადგილობრივი მოთხოვნების შესაბამისად. მეორე მხარის მიერ ყოველდღიურად მოწმდება და დასტურდება მათი რაოდენობა.
ფარმაცევტები და სხვა წამლის გამცემი პერსონალი უნდა გადიოდნენ სწავლებას მეთადონის და ბუპრენორფინის გაცემის შესახებ.
მეთადონის და ბუპრენორფინის გაცემამდე პერსონალმა უნდა უზრუნველყოს შემდეგი:
პაციენტის ვინაობის დადგენა და რეცეპტთან თანხვედრის შემოწმება;
დადასტურება, რომ პაციენტს არ აღენიშნება ინტოქსიკაცია;
შემოწმება, რომ რეცეპტი ძალაშია და მოცემული დღე ნამდვილად დოზის გაცემის დღეა (დღეგამოშვებით ან კვირაში სამჯერ გამოწერილი ბუპრენორფინის შემთხვევაში);
დოზის რეცეპტთან შესაბამისობის შემოწმება.
დოზირებასთან დაკავშირებული შეცდომების შესამცირებლად და ჩანაწერების წარმოების გასაადვილებლად არსებობს კომპიუტერიზებული სისტემები, რომლებიც ადასტურებს პაციენტის ვინაობას ბადურის ან ფერადი გარსის სკანირების საშუალებით და ავტომატურად გასცემს რეცეპტში მითითებულ დოზას (ფარმაცევტის მიერ ინფორმაციის შეყვანის შემდეგ).
ძალიან მნიშვნელოვანია, რომ მეთადონი და ბუპრენორფინი არ გაიცეს პაციენტებზე, რომლებსაც სედაცია ან ინტოქსიკაცია აღენიშნებათ, რადგან ამან შეიძლება ჭარბი სედაცია გამოიწვიოს. დოზის გამცემი პერსონალი უნდა იყოს გამოცდილი სედაციის ხარისხის შეფასებაში და ამგვარ პაციენტებს გადაჭრით უთხრას უარი დოზის მიცემაზე. თუ პაციენტი სვამს, შეიძლება ეფექტიანი იყოს ჩასუნთქვით ალკოჰოლის დოზის განსაზღვრა. პაციენტებს უნდა სთხოვონ, დოზის მისაღებად ინტოქსიკაციის ან სედაციის მოხსნის შემდეგ დაბრუნდნენ.
გაცემული დოზა უნდა დაფიქსირდეს კანონით მოთხოვნილი წესის მიხედვით.
A2.2 ბუპრენორფინის გაცემა
ბუპრენორფინის ტაბლეტები უნდა გაიცეს მშრალი დოზისათვის განკუთვნილი ჭიქით აბების რაოდენობისა და დოზირების გადამოწმების შემდეგ. აბის მიცემამდე პაციენტს სთხოვეთ, აბი ენის ქვეშ ჩაიდოს და არ გადაყლაპოს, სანამ ის არ გაიხსნება (საშუალოდ 5 წუთი, მაგრამ შეიძლება 15 წუთამდეც დასჭირდეს). ფარმაცევტმა უნდა შეამოწმოს პაციენტის პირის ღრუ, რომ მას პირში არ ჰქონდეს საკვები ან რაიმე, რისი საშუალებითაც ბუპრენორფინს დამალავს. აბის მიცემის შემდეგ ფარმაცევტმა კვლავ უნდა შეამოწმოს პაციენტის პირის ღრუ, რათა განსაზღვროს, გაიხსნა თუ არა ბუპრენორფინი. შემდეგ პაციენტს პირში გამოსავლებად სითხე უნდა შევთავაზოთ.
დოზასთან დაკავშირებული გაურკვევლობის თავიდან ასაცილებლად პაციენტმა რაიმე სახით უნდა დააფიქსიროს, რომ მიიღო დოზა (მაგ., დოზირების ბარათზე ხელმოწერით). თუ პაციენტი ეცდება, დოზა გადმოაფურთხოს ან დატოვოს გასაცემი ოთახი დოზის გახსნამდე, ამის შესახებ უნდა ეცნობოს პრეპარატის გამომწერ ექიმს. ბუპრენორფინის არადანიშნულებით გამოყენების თავიდან ასაცილებლად ზოგჯერ აბებს ფშვნიან, მაგრამ ამ მეთოდის ეფექტიანობა შეფასებული არ არის.
A2.3 რეცეპტები
კანონის მოთხოვნები რეცეპტის გამოწერასთან დაკავშირებით სხვადასხვაგვარია; თუმცა, ზოგადად, ოპიოიდური აგონისტით თერაპიის დროს რეცეპტზე მითითებული უნდა იყოს შემდეგი:
რეცეპტის გამომწერი ექიმის სახელი და გვარი, მისამართი და ტელეფონის ნომერი;
აფთიაქის დასახელება, საიდანაც ხდება მეთადონის ან ბუპრენორფინის გაცემა და პაციენტის მისამართი;
რეცეპტის გამოწერის თარიღი;
გასაცემი პრეპარატი (მაგ., მეთადონი თხევადი ფორმით ან ბუპრენორფინის სუბლინგვური ტაბლეტები);
გასაცემი დოზა მილიგრამებით (სიტყვიერად და რიცხვობრივად);
გაცემის სიხშირე (ყოველდღე, დღეში ორჯერ, ყოველ მეორე დღეს, კვირაში სამჯერ);
დოზების გაცემის დაწყების და დასრულების თარიღები მოცემული რეცეპტის მიხედვით;
საჭიროა თუ არა დოზებზე ზედამხედველობა ან შეიძლება თუ არა ზოგიერთი დოზის სახლში მისაღებად გატანება (განსაზღვრეთ სახლში წასაღები დასაშვები მაქსიმალური რაოდენობა კვირაში).
დოზის გაცემაში შეცდომის დაშვების პოტენციური საფრთხის გამო, ზოგჯერ კანონი მოითხოვს, რომ რეცეპტის გამომწერმა ექიმმა რეცეპტს დაურთოს პაციენტის ფოტო, რომელიც იგზავნება აფთიაქში ან წამლის გამცემ სხვა ობიექტზე. ზოგიერთი კანონმდებლობით საჭიროა, ოპიოიდების დოზები მოცემული იყოს როგორც სიტყვიერად, ისე რიცხვობრივად. ყალბი რეცეპტის გამოყენების თავიდან ასაცილებლად, შეიძლება ეფექტიანი იყოს რეცეპტის ასლის აფთიაქში ფაქსით ან დაცული ელფოსტით გაგზავნა.
 |
13 დანართი 3. ICD-10-ის კოდები ამ სახელმძღვანელოში მოცემული დაავადებებისთვის |
▲back to top |
დანართში მოცემულია კოდები დაავადებების საერთაშორისო კლასიფიკაციის მე-10 გადასინჯვიდან (დსკ-10) ამ სახელმძღვანელოში მოცემული დაავადებებისთვის [14].
F11.0 ინტოქსიკაცია (ოპიოიდები)
მდგომარეობა, რომელიც ფსიქოაქტიური ნივთიერების მიღებისას ვითარდება, გამოიხატება ქცევის მოშლით, აღქმის, ცნობიერების და კოგნიტური ან სხვა ფსიქოფიზიოლოგიური ფუნქციების და რეაქციების დარღვევით. ეს დარღვევები პირდაპირ უკავშირდება ნივთიერების მწვავე ფარმაკოლოგიურ ეფექტებს და დროთა განმავლობაში უკუგანვითარდება სრული აღდგენით, გარდა იმ შემთხვევებისა, როცა ქსოვილის დაზიანება და სხვა გართულებები აღინიშნება. გართულებები შეიძლება მოიცავდეს ტრავმას, პირნაღები მასების ინჰალაციას, დელირიუმს, კომას, კრუნჩხვებს და სხვა სომატურ გართულებებს. ამ გართულებების ტიპი დამოკიდებულია ნივთიერების ფარმაკოლოგიურ კლასზე და შეყვანის გზაზე.
არ შეიცავს: ინტოქსიკაციას მოწამვლის მნიშვნელობით (T36-T50).
F11.2 დამოკიდებულების სინდრომი (ოპიოიდები)
ქცევითი, კოგნიტური და ფიზიოლოგიური ფენომენების ერთობლიობა, რომელიც ვითარდება ნივთიერების რეგულარული გამოყენების დროს და რომელიც, როგორც წესი, მოიცავს ნარკოტიკის მიღების ძლიერ სურვილს, მოხმარების კონტროლის სირთულეს, მიღების გაგრძელებას (მიუხედავად მავნე შედეგებისა) და პრიორიტეტის მინიჭებას ნარკოტიკის მოხმარებისთვის, სხვა ქმედებებთან და ვალდებულებებთან შედარებით; ასევე გაზრდილ ტოლერანტობას და ზოგჯერ ფიზიკური აღკვეთის მდგომარეობას.
დამოკიდებულების სინდრომი შეიძლება განვითარდეს სპეციფიკური ფსიქოაქტიური ნივთიერების (მაგ., თამბაქრო, ალკოჰოლი ან დიაზეპამი), ნივთიერებათა გარკვეული კლასის (მაგ. ოპიოიდები) ან ფარმაკოლოგიურად განსხვავებული ფსიქოაქტიური ნივთიერებების უფრო ფართო სპექტრის გამოყენებისას.
დსკ-10-ის მიხედვით ოპიოიდური დამოკიდებულების დიაგნოსტიკური კრიტერიუმებია:
ოპიოიდების მიღების ძლიერი სურვილი ან კომპულსიური ლტოლვა;
ოპიოიდების გამოყენებასთან დაკავშირებული ქცევის კონტროლის სირთულე. (ქცევაში იგულისხმება პრეპარატის მიღების დაწყება, დასრულება და მიღების ინტენსივობა);
ფიზიოლოგიური აღკვეთის მდგომარეობა ოპიოიდების მიღების შეწყვეტის ან დოზის შემცირებისას, რაც გამოვლინდება ერთ-ერთით ქვემოთ ჩემოთვლილთაგან:
- დამახასიათებელი აღკვეთის სინდრომი;
- ოპიოიდების (ან მათი მონათესავე ნივთიერებების) გამოყენება აღკვეთის სიმპტომების შემსუბუქების ან თავიდან აცილების მიზნით.
ტოლერანტობის განვითარების ნიშნები, კერძოდ, ოპიოიდების დოზის მზარდი საჭიროება იმ ეფექტების მისაღწევად, რაც მანამდე უფრო დაბალი დოზებით მიიღწეოდა;
სხვა სიამოვნების ან ინტერესების პროგრესირებადი უგულებელყოფა ოპიოიდების გამოყენების გამო; ოპიოიდების მოსაპოვებლად ან მათი ეფექტებისგან გასათავისუფლებლად სულ უფრო მეტი დროის დახარჯვა;
ოპიოიდების მიღების გაგრძელება მიუხედავად აშკარა უარყოფითი შედეგებისა, როგორებიცაა დეპრესიული გუნებაგანწყობა ნარკოტიკების დიდი რაოდენობით მოხმარების შემდეგ ან კოგნიტური ფუნქციების ნარკოტიკებთან დაკავშირებული მოშლა (უნდა ვეცადოთ, განვსაზღვროთ, იცის თუ არა მომხმარებელმა ან შეიძლება თუ არა სცოდნოდა ზიანის ბუნება და მასშტაბი).
აგრეთვე, დამოკიდებულებისთვის დამახასიათებელი ნიშანია პიროვნების ინტერესების შევიწროება და ოპიოიდების გარკვეულ ტიპზე კონცენტრირება.
ოპიოიდური დამოკიდებულება არ ვითარდება რეგულარული მოხმარების პერიოდის გარეშე, თუმცა, მხოლოდ რეგულარული გამოყენება არ არის საკმარისი დამოკიდებულების ინდუქციისთვის.
დამოკიდებულების საბოლოო დიაგნოზი უნდა დაისვას მხოლოდ მაშინ, თუ ბოლო 12 თვის გარკვეული პერიოდის განმავლობაში ერთდოულად დაფიქსირდა სამი ან მეტი დიაგნოსტიკური კრიტერიუმი.
F11.3 აღკვეთის მდგომარეობა (ოპიოიდები)
სხვადასხვა ტიპის და სიმძიმის სიმპტომების ერთობლიობა, რომელიც აღინიშნება ფსიქოაქტიური ნივთიერების მიღების მთლიანად ან ნაწილობრივ შეწყვეტისას. აღკვეთის სიმპტომების დაწყება და მიმდინარეობა გარკვეული დროით შემოიფარგლება და დამოკიდებულია ფსიქოაქტიურ ნივთიერებაზე და მის დოზაზე, რომელიც ნარკოტიკის შეწყვეტამდე ან შემცირებამდე იქნა მიღებული. აღკვეთის სინდრომი შეიძლება გართულდეს კრუნჩხვით.
 |
14 დანართი 4. ოპიოიდური დამოკიდებულების მკურნალობისათვის რეკომენდებული მედიკამენტების ფარმაკოლოგია |
▲back to top |
A4.1 მეთადონი
მეთადონი ძლიერი სინთეზური ოპიოიდური აგონისტია. იგი ორი პერორალური ფორმით გამოდის - აბი და ხსნარი. ოპიოიდური დამოკიდებულებისთვის რეკომენდებულია ხსნარი, რადგან სითხის მიღებაზე ზედამხედველობა უფრო ადვილია, ვიდრე აბზე. ასევე, სახლში მისაღები დოზა შეიძლება განზავდეს და ამით შემცირდეს ვენაში შესაყვანად მისი გამოყენების რისკი. ორივე პერორალურ ფორმას მწარე გემო აქვს.
ადამიანებისათვის, რომელთაც ოპიოიდები არ მიუღიათ, მეთადონს ხარისხობრივად იგივე ეფექტი აქვს, რაც მორფინს და სხვა ოპიოიდებს; თუმცა, ოპიოიდებზე დამოკიდებულ პაციენტებში მეთადონი ხელს უშლის აღკვეთის სიმპტომების განვითარებას, მაგრამ არ იწვევს მნიშვნელოვან სედაციას ან ინტოქსიკაციას.
მეთადონი გამოირჩევა მაღალი (85%25-ი) ბიოშეღწევადობით (ანუ თერაპიულად აქტიური პრეპარატის რაოდენობა, რომელიც აღწევს სისტემურ ცირკულაციაში და მოქმედებს პერორალურად მიღების შემდეგ). სისხლში მაქსიმალური კონცენტრაცია მიიღწევა დოზის მიღებიდან 2-4 საათის შემდეგ. მეთადონი ქსოვილებში ნაწილდება და 60-90%25-ი ცილებთან შეკავშირდება. მეთადონის დემეთილირება ხდება ღვიძლის ციტოქრომ P450 3A4 და 2D6 (CYP2D6)
ფერმენტებით მის ძირითად მეტაბოლიტამდე - 2-ეთილიდინ-1,5 დიმეთილ-3,3-დიფენილპიროლიდინამდე (EDDP). ეს არააქტიური მეტაბოლიტი გამოიყოფა განავლით და შარდით შეუცვლელ მეთადონთან ერთად. ამ ფერმენტებზე მოქმედი სხვა პრეპარატების ერთდროულმა გამოყენებამ შეიძლება კლინიკურად მნიშვნელოვანი ურთიერთქმედება გამოიწვიოს. მეთადონის დოზა შესაბამისად უნდა იყოს დარეგულირებული.
მეთადონით მხარდამჭერი თერაპიის დროს აღწერილია შრატში მისი კონცენტრაციის დაქვეითება, რაც მიუთითებს ტოლერანტობის განვითარებაზე, შესაძლოა, ღვიძლის მიკროსომული ფერმენტების აუტოინდუქციის გამო.
მეთადონის მიმართ პაციენტებს ახასიათებთ გამოხატული ვარიაციები შეწოვის, განაწილების, ცირკულაციის, მეტაბოლიზმის და ელიმინაციის (კინეტიკა) მხრივ, - დაფიქსირებულია 15-დან 60 საათამდე დიაპაზონი, - და ამდენად, აუცილებელია დასაწყისისთვის დოზის ფრთხილად დარეგულირება, რის შემდეგაც ქსოვილებში აღინიშნება თანდათანობითი აკუმულაცია.
მეთადონი შედის ნარკოტიკული პრეპარატების პირველი კონვენციის (1961) I სიაში (იხ. დანართი 7).
A4.2 ბუპრენორფინი
ბუპრენორფინი ძლიერი სინთეზური ნაწილობრივი აგონისტია, რომელსაც მაღალი რეცეპტორული აფინურობა და ნელი რეცეპტორული დისოციაცია ახასიათებს. ეს ნიშნავს, რომ მისი კლინიკური ეფექტები ცვალებადია როგორც ბუპრენორფინის მომხმარებელი ადამიანის ნეიროადაპტაციის (ტოლერანტობა), ისე რეცეპტორების დაკავების (დრო ოპიოიდის ბოლო გამოყენებიდან) მხრივ. ბუპრენორფინის ნაწილობრივი აქტივობა ნიშნავს, რომ იგი იმდენად არ ახდენს ოპიოიდებისადმი ტოლერანტობის განვითარების ინდუქციას, როგორც მეთადონი. მისი მაღალი რეცეპტორული აფინურობა ნიშნავს, რომ ბუპრენორფინს შეუძლია დამატებითი ოპიოიდების გამოყენების ეფექტების დაბლოკვა იმ დონის ტოლერანტობის გამოწვევის გარეშე, რასაც მეთადონი იწვევს. მისი ერთდროულად ნელი რეცეპტორული დისოციაცია და ნაწილობრივი აქტივობა ნიშნავს, რომ მისი აღკვეთის სინდრომი უფრო მსუბუქია, ვიდრე მეთადონის.
ოპიოიდური ნეიროადაპტაციის დაბალი დონის პირობებში ბუპრენორფინის ყველა დოზა აგონისტურ ეფექტებს წარმოქმნის იმგვარად, რომ მაღალი დოზები ხარისხობრივად იმავე ეფექტს იძლევა, როგორსაც დაბალი, მაგრამ უფრო დიდი ხნის განმავლობაში. თუმცა, ნეიროადაპტაციის მაღალი დონის პირობებში, როცა ოპიოიდების გამოყენება უკანასკნელ დრომდე გრძელდება, ბუპრენორფინის მაღალ დოზებს შეუძლია ჰეროინის და სხვა ოპიოიდების რეცეპტორებთან დაკავშირებისთვის ხელის შეშლა, რაც იწვევს ოპიოიდური ეფექტის სწრაფ ვარდნას, რაც ოპიოიდური აღკვეთის მდგომარეობის სახით გამოიხატება.
ბუპრენორფინის დაბალ დოზებს ბევრ ქვეყანაში იყენებენ მწვავე ტკივილის სამკურნალოდ.
ბუპრენორფინის პოტენციური უპირატესობა არის ის, რომ მას უსაფრთხოების ძალიან კარგი დიაპაზონი აქვს. მისი ნაწილობრივ აგონისტური მოქმედება μ-ოპიოიდურ რეცეპტორებზე ხელს უშლის პოტენციურად ფატალური სუნთქვის დათრგუნვის გამოწვევას, რაც სრული აგონისტი ოპიოიდების ჭარბი მიღებისას აღინიშნება. უსაფრთხოების დიაპაზონი ასევე იძლევა უფრო მაღალი დოზების მიცემის საშუალებას გახანგრძლივებული მოქმედების უზრუნველსაყოფად ოპიოიდური ეფექტის მნიშვნელოვნად გაზრდის გარეშე. ამ გზით შესაძლებელია ბუპრენორფინის ორმაგი დოზის მიცემა ყოველ მეორე დღეს.
ბუპრენორფინი შედის ნარკოტიკული პრეპარატების კონვენციის (1961) III სიაში, (იხ. დანართი 7).
A4.3 ბუპრენორფინი - ნალოქსონი 4:1 კომბინირებული პროდუქტი
ბუპრენორფინის და ნალოქსონის კომბინირებული პროდუქტი 4:1 თანაფარდობით ორი დოზით გამოდის (2 მგ ბუპრენორფინი : 0.5 მგ ნალოქსონი და 8 მგ ბუპრენორფინი : 2 მგ ნალოქსონი). ამ მედიკამენტის ეფექტიანობა მოცემულ სახელმძღვანელოში განხილული არ არის კლინიკური კვლევების არარსებობის გამო; თუმცა, რადგან ეს პრეპარატი რეგისტრირებულია და გამოიყენება რამდენიმე ქვეყანაში, მიზანშეწონილად მივიჩნიეთ მისი ფარმაკოლოგიის განხილვა.
მაშინ, როდესაც ბუპრენორფინი ენის ქვეშ მიიღება, ენის ქვეშ მიღებისას ნალოქსონის მხოლოდ 5-10%25-ი შეიწოვება [267]. არსებობს მოსაზრება, რომ ეს ძალიან დაბალი დოზაა რეალური კლინიკური ეფექტის მისაღებად. მიუხედავად იმისა, რომ ბუპრენორფინს და ნალოქსონს ოპიოიდური რეცეპტორების მიმართ მსგავსი აფინურობა ახასიათებს, დომინირებს ბუპრენორფინის ეფექტი სისხლში მისი კონცენტრაციის გაცილებით მაღალი დონის გამო. თუმცა, ბუპრენორფინი/ნალოქსონის კომბინირებული პროდუქტის ინექციის შემთხვევაში ნალოქსონის დოზამ შეიძლება ოპიოიდური აღკვეთის მდგომარეობა გამოიწვიოს (გარემოებების მიხედვით).
ჰეროინზე ან სხვა ოპიოიდურ აგონისტებზე დამოკიდებულ მომხმარებელში ბუპრენორფინი-ნალოქსონის კომბინირებული პროდუქტი იწვევს ოპიოიდების აღკვეთის სინდრომს [268, 269]. ბუპრენორფინი-ნალოქსონის უფრო მაღალი დოზები უფრო მძიმე აღკვეთის სინდრომს იწვევს [270]. ოპიოიდებზე არადამოკიდებულ მომხმარებელში ბუპრენორფინი-ნალოქსონის პროდუქტის ინექცია არ იწვევს აღკვეთის სინდრომს, მაგრამ ნალოქსონი ამცირებს ბუპრენორფინის ოპიოიდურ ეფექტს, რაც გამოიხატება ოპიოიდური ეფექტის გვიანი დასაწყისითა და ნაკლები ინტენსივობით [271]. პაციენტებში, რომლებიც მკურნალობის კურსს ბუპრენორფინით გადიან ან უკანონო ბუპრენორფინის მომხმარებლებში ბუპრენორფინი-ნალოქსონის პროდუქტის ინექცია არ იწვევს აღკვეთის სინდრომს [272] იმის გამო, რომ ბუპრენორფინის ჩანაცვლებას ნალოქსონის უფრო მაღალი დოზები სჭირდება ან ნალოქსონის ნახევარდაშლის პერიოდი ძალიან მოკლეა ბუპრენორფინის ოპიოიდური რეცეპტორებიდან ნელ დისოციაციასთან შედარებით.
A4.4 ოპიოიდების ანტაგონისტი მედიკამენტები
ნალტრექსონი
ნალტრექსონი არის პერორალური ოპიოიდური ანტაგონისტი 24-48 საათიანი ეფექტის ხანგრძლივობით, რაც იძლევა მისი დღეში ერთხელ გამოყენების საშუალებას. მას ძალიან მაღალი აფინურობა აქვს ოპიოიდური რეცეპტორების მიმართ და რამდენიმე წუთში ჩაანაცვლებს ჰეროინს და მეთადონს, 1-4 საათში კი - ბუპრენორფინს. იგი გამოიყენება ოპიოიდების მოხსნის შემდეგ რეციდივის განმეორების თავიდან ასაცილებლად.
ნალოქსონი
ნალოქსონი ხანმოკლე მოქმედების საინექციო ოპიოიდური ანტაგონისტია, რომელიც გამოიყენება ოპიოიდური ზედოზირების მკურნალობისთვის ოპიოიდების ეფექტის მოსახსნელად. პერორალური მიღებისას ცუდად შეიწოვება და ამიტომ კეთდება კუნთში ან ვენაში. მისი ნახევარდაშლის პერიოდი, დაახლოებით, ერთი საათია, მაგრამ რეცეპტორების 50%25-ი შეყვანიდან 2 საათის შემდეგაც დაკავებული აქვს [273].
A4.5 მედიკამენტები ოპიოიდების აღკვეთის სინდრომის მართვისათვის
ალფა ადრენერგული აგონისტები
ალფა ადრენერგული აგონისტები კლონიდინი, ლოფექსიდინი და გუანფაცინი ცენტრალურ და პერიფერიულ ავტონომიურ ნერვულ სისტემაზე მოქმედებს, ამცირებს ადრენალინის და ნორადრენალინის ენდოგენურ გამოყოფას, რაც აღკვეთის მდგომარეობის დროს შედარებით დიდი რაოდენობით ხდება. ეს პრეპარატები აიშვიათებს გულისცემას, აქვეითებს არტერიულ წნევას, ამცირებს კუნთების ტონუსს და იწვევს სედაციას. ლოფექსიდინს უფრო სპეციფიკურად პერიფერიული მოქმედება აქვს და არ იწვევს ისეთ ჰიპოტენზიას, როგორსაც ამ ჯგუფის სხვა პრეპარატები. როგორც ლოფექსიდინი, ისე კლონიდინი ხანმოკლე მოქმედების პრეპარატებია და დღეში ოთხჯერ მიიღება. გუანფაცინი კი დღეში ერთხელ ინიშნება.
 |
15 დანართი 5. წამალთა ურთიერთქმედება მეთადონსა და ბუპრენორფინთან |
▲back to top |
წამალთა ურთიერთქმედება იმის გამო აღინიშნება, რომ მათ ახასიათებს სინერგიული ან ანტაგონისტური ეფექტები (ე.წ. ფარმაკოდინამიკური ურთიერთქმედება) ან ერთი მედიკამენტი მოქმედებს მეორე მედიკამენტის შეწოვაზე, განაწილებაზე, ცირკულაციაზე, მეტაბოლიზმსა და ელიმინაციაზე (ე.წ. ფარმაკოკინეტიკური ურთიერთქმედება).
A5.1 ფარმაკოდინამიკური ურთიერთქმედება
სედაცია
სედაციის გამომწვევმა ყველა პრეპარატმა მეთადონთან და ბუპრენორფინთან ერთად მიღებისას შეიძლება გამოიწვიოს დამატებითი სედაცია და ამით გაზარდოს ზედოზირების რისკი. ამგვარ პრეპარატებს განეკუთვნება ბენზოდიაზეპინები, ალკოჰოლი, სხვა სედაციური ფსიქოტროპული მედიკამენტები (მაგ., ფენოთიაზინები და სხვა ანტიფსიქოზური ნივთიერებები), ტრიციკლური და სხვა სედაციური მოქმედების ანტიდეპრესანტები, ალფა ადრენერგული აგონისტები (მაგ. კლონიდინი და ლოფექსიდინი) და სედაციური ანტიჰისტამინური საშუალებები. ზედოზირებით გამოწვეული სიკვდილი უმრავლეს შემთხვევაში დაკავშირებულია მეთადონთან და ბუპრენორფინთან ერთად ერთ-ერთი ამ სედატიური მოქმედების პრეპარატის გამოყენებასთან.
ოპიოიდური აღკვეთის სინდრომი
ოპიოიდური ანტაგონისტები, როგორიცაა ნალტრექსონი, მეთადონზე ან ბუპრენორფინზე მყოფ პაციენტებში იწვევს ოპიოიდური აღკვეთის სინდრომს. ნალტრექსონს ვერ გამოვიყენებთ ამ პოპულაციაში ალკოჰოლური დამოკიდებულების სამკურნალოდ. აგონისტების და ნაწილობრივი აგონისტების კომბინაციამ ასევე შეიძლება გამოიწვიოს ოპიოიდური აღკვეთის მდგომარეობა. მეთადონის კომბინირება არ უნდა მოხდეს ნაწილობრივ აგონისტებთან, როგორებიცაა: ბუპრენორფინი, პენტაზოცინი, ნალბუფინი ან ბუტორფანოლი. ბუპრენორფინზე მყოფ პაციენტებს, რომლებიც ასევე იღებენ ოპიოიდურ აგონისტებს ტკივილის გამო, შეიძლება ტკივილი მთლიანად არ მოეხსნათ.
QT ინტერვალის გახანგრძლივება
მედიკამენტების ზოგიერთი ჯგუფი მოქმედებს დროზე, რომელიც საჭიროა გულის პარკუჭის კუნთის დეპოლარიზაციის და შემდგომი რეპოლარიზაციისთვის - QT ინტერვალი ელექტროკარდიოგრამაზე. QT ინტერვალის გახანგრძლივება ქმნის წინაპირობას მძიმე არითმიის განვითარებისთვის (torsades de pointes-ი და სხვა პარკუჭოვანი ტაქიარითმიები, რომლებიც მკურნალობის გარეშე შეიძლება ფატალური აღმოჩნდეს). მეთადონი ერთ-ერთი ასეთი მედიკამენტია. მეთადონის კომბინირება სხვა პრეპარატებთან, რომლებიც ასევე იწვევს QT ინტერვალის გახანგრძლივებას, სიფრთხილით უნდა მოხდეს, რადგან ამით შეიძლება გაიზარდოს QT ინტერვალის გახნგრძლივებით გამოწვეული არითმიების რისკი. ეს მედიკამენტებია: ძირითადად I ან III კლასის ანტიარითმიული პრეპარატები, კალციუმის არხის ბლოკატორები, ზოგიერთი ანტიფსიქოზური აგენტი და ზოგიერთი ანტიდეპრესანტი (უფრო სრული სიისთვის იხ. ცხრილი A5.1). ელექტროლიტური ბალანსის დარღვევის (მაგ., ჰიპოკალიემია და ჰიპომაგნიემია) გამომწვევი პრეპარატები ასევე იწვევს QT ინტერვალის გახანგრძლივებასთან დაკავშირებული არითმიების რისკის მომატებას (ასეთებია: შარდმდენები, ყაბზობის საწინააღმდეგო საშუალებები, კორტიკოსტეროიდები მინერალოკორტიკოიდული აქტივობით). ბუპრენორფინი არ იწვევს QT ინტერვალის კლინიკურად მნიშვნელოვან გახანგრძლივებას.
A5.2 ფარმაკოკინეტიკური ურთიერთქმედებები
მეთადონი და ბუპრენორფინი ძირითადად ციტოქრომ P450 ენზიმური სისტემით მეტაბოლიზდება. მრავალი სახის მედიკამენტი ახდენს P450 ენზიმების ინდუქციას ან ინჰიბიციას. ინდუქციის პროცესი შედარებით ნელია, რადგან დამოკიდებულია ახალი ენზიმური პროტეინების სინთეზზე და მიმდინარეობს დღეების განმავლობაში, მაშინ როცა ინჰიბიცია სწრაფად ვითარდება და დამოკიდებულია მაინჰიბირებელი ნივთიერების კონცენტრაციაზე.
მეთადონი ძირითადად მეტაბოლიზდება აქტიურ და არააქტიურ მეტაბოლიტებად CYP3A4-ის საშუალებით, უფრო ნაკლებად CYP1A2, CYP2D6, CYP2B6, CYP2C8-ის, ასევე შესაძლოა CYP2C9 და CYP2C19-ის საშუალებით [275, 276, 277, 278, 279, 280, 281, 282, 283]. CYP ენზიმის მაინდუცირებელ პრეპარატებს შეუძლია სისხლში მეთადონის დონის შემცირება, ხოლო ინჰიბიტორებს - მისი დონის გაზრდა. სედაციური ზედოზირების რისკის გამო, მეთადონზე მყოფ პაციენტებში განსაკუთრებული დაკვირვებაა საჭირო ციტოქრომ P450-ის ინჰიბიტორებით მკურნალობის დაწყებისას. ამ შემთხვევაში, შესაძლოა დადგეს მეთადონის დოზის შემცირების საკითხი. ახალი მედიკამენტის დანიშვნისას, რომელსაც პოტენციურად აქვს ურთიერთქმედების უნარი, მნიშვნელოვანია პაციენტზე დაკვირვება და, თუ საჭიროა, მეთადონის დოზის დარეგულირება.
ბუპრენორფინი ღვიძლში, ძირითადად, CYP3A4 იზოფერმენტის საშუალებით მეტაბოლიზდება [282]. აქტიური მეტაბოლიტი, ნორბუპრენორფინი, განსხვავებული გზით მეტაბოლიზდება. პრეპარატებს, რომლებიც ახდენს CYP3A4-ს ინჰიბიციას (მაგ. კეტოკონაზოლი, ერითრომიცინი, ზოგიერთი პროტეაზის ინჰიბიტორი), შეუძლია ბუპრენორფინის კონცენტრაციის გაზრდა, ამიტომ მათი გამოყენებისას საჭიროა ბუპრენორფინის დოზის შემცირება. მედიკამენტებს, რომლებიც ახდენს CYP3A4-ს ინდუქციას (მაგ. რიფამპიცინი, ფენიტოინი, ფენობარბიტალი, კარბამაზეპინი), შეუძლია ბუპრენორფინის კონცენტრაციის დაქვეითება. შეზღუდულია იმ კვლევების რაოდენობა, რომლებშიც შესწავლილია ბუპრენორფინის ურთიერთქმედება სხვა მედიკამენტებთან.
ცხრილში A5.2 მოცემულია იმ პრეპარატების უფრო დაწვრილებითი ჩამონათვალი, რომლებიც მოქმედებს ციტოქრომ P450-ის სისტემაზე [282].
CYP450-ის ინდუქტორები
ალკოჰოლი
როგორც ცნობილია, ალკოჰოლის ქრონიკული მოხმარება ზრდის მეთადონის მეტაბოლიზმს, მწვავე ინტოქსიკაცია კი იწვევს მეთადონის მრუდის ქვეშ (AUჩ)1 ფართობის გაზრდას, რაც, თავის მხრივ, გვერდითი მოვლენების გაზრდილ რისკთან არის დაკავშირებული.
ანტიკონვულსანტები
ფენიტოინი, კარბამაზეპინი და ფენობარბიტალი CYP3A4-ის მნიშვნელოვანი ინდუქტორებია. ყველა მათგანს შეუძლია აღკვეთის სიმპტომების გამოწვევა მეთადონზე მყოფ პაციენტში.
ანტიდეპრესანტები
სერტრალინი, ფლუოქსეტინი და ფლუოქსამინი CYP3A4-ის ინდუქტორებია. მეთადონს შეუძლია ტრიციკლური ანტიდეპრესანტების ეფექტების გაძლიერება.
ანტიმიკობაქტერიული პრეპარატები
რიფამპიცინი (რიფამპინი) იწვევს მეთადონის კონცენტრაციის კლინიკურად მნიშვნელოვან შემცირებას.
ცხრილი A5.1 პრეპარატები, რომლებიც ზრდის torsades de points-ს ან QT ინტერვალის გახანგრძლივების რისკს |
|||
ამიოდარონი |
დარიშხანის ტრიოქსიდი |
ბეპრიდილი |
ქლოროქინი |
ქლორპრომაზინი |
ცისაპრიდი |
კლარიტრომიცინი |
დიზოპირამიდი |
დოფეტილიდი |
დომპერიდონი |
დროპერიდოლი |
ერითრომიცინი |
ჰალოფანტრინი |
ჰალოპერიდოლი |
იბუტილიდი |
მეზორიდაზინი |
მეთადონი |
პენტამიდინი |
პიმოზიდი |
პროკაინამიდი |
ქინიდინი |
სოტალოლი |
სპარფლოქსაცინი |
თიორიდაზინი |
ანტირეტროვირუსულები
ბევრი ანტირეტროვირუსული პრეპარატი ურთიერთქმედებს მეთადონთან და ბუპრენორფინთან, იხ. ცხრილები A5.2 და A5.3.
სხვა პრეპარატები
St John's wort (Hypericum) ასევე ახდენს CYP3A4-ის ინდუქციას.
CYP450-ის ინჰიბიტორები
სოკოს საწინააღმდეგო საშუალებები
აზოლის პრეპარატები, მათ შორის, კეტოკონაზოლი, ფლუკონაზოლი და იტრაკონაზოლი CYP3A4-ის მნიშვნელოვანი ინჰიბიტორებია და ზრდის როგორც მეთადონის, ისე ბუპრენორფინის ეფექტებს. შეიძლება დადგეს დოზის შემცირების საკითხი.
ანტირეტროვირუსულები
ბევრი ანტირეტროვირუსული მედიკამენტი ურთიერთქმედებს მეთადონთან და ბუპრენორფინთან, იხ. ცხრილები A5.2 და A5.3.
მაკროლიდების ჯგუფის ანტიბიოტიკები
მაკროლიდების უმრავლესობა (ერითრომიცინი, კლარითრომიცინი, დირითომიცინი, როქსიტრომიცინი) ახდენს CYP3A4-ის ინჰიბიციას (აზიტრომიცინის გარდა).
სხვა პრეპარატები
გრეიფრუტის წვენი P450-ის ფერმენტების მნიშვნელოვანი ინჰიბიტორია.
ცხრილი A5.2 ურთიერთქმედება ანტირეტროვირუსულ აგენტებსა და მეთადონს შორის |
||||||||
ანტირეტროვირუსული აგენტი |
მოქმედება მეთადონზე |
მეთადონის ეფექტი ანტირეტროვირუსულ აგენტებზე |
კომენტარი |
|||||
ნუკლეოზიდის/ნუკლეოტიდის შებრუნებითი ტრანსკრიპტაზას ინჰიბიტორები |
||||||||
აბაკავირი (ABC) |
მეთადონის კლირენსი იზრდება 22%25-ით. |
კონცენტრაცია მცირედ დაქვეითებულია |
პაციენტებს უნდა დააკვირდნენ მეთადონის |
|||||
დიდანოზინი (ddl) |
არ არის |
ddl-ის კონცენტრაცია მცირდება 57%25-ით, |
ddl-ის დოზა შეიძლება |
|||||
ემტრიციტაბინი (FTC) |
არ არის |
არ არის |
ურთიერთქმედება ცნობილი არ არის |
|||||
ლამივუდინი (3TC) |
არ არის. |
არ არის |
ურთიერთქმედება ცნობილი არ არის |
|||||
სტავუდინი (d4T) |
არ არის |
მეთადონის მიღებამ შეამცირა |
კლინიკურად მნიშვნელოვანი |
|||||
ტენოფოვირი (TDF) |
არ არის |
არ არის |
|
|||||
ზიდოვუდინი (AZT) |
არ არის |
კონცენტრაცია გაიზარდა 29-43%25-ით. |
მონიტორნიგი AZT-ის გვერდით მოვლენებზე, |
|||||
არანუკლეოზიდური რევერსიული ტრანსკრიპტაზას ინჰიბიტორები (NNRTIs) |
||||||||
ეფავირენზი (EFV) |
მეთადონის Cmax (45%25)-ის და AUC (52%25)- |
არ არის |
აღკვეთის სიმპტომები შეიძლება |
|||||
ეტრავირინი (TMC-125) |
კლინიკურად მნიშვნელოვანი ეფექტი არ არის. |
მნიშვნელოვანი ეფექტი არ არის. |
დააკვირდით, მაგრამ დოზის დარეგულირების |
|||||
ნევირაპინი (NVP) |
დაქვეითება, აღწერილია |
არ არის |
აღკვეთის სიმპტომები ხშირია; ჩვეულებრივ,
მეთადონის ქრონიკულ მომხმარებლებში, |
|||||
პროტეაზას ინჰიბიტორები (PIs) |
||||||||
ატაზანავირი (ATV) |
არ არის |
არ არის |
--- (თუ დამატებულია ღთV, იხ. RTV№). |
|||||
დარუნავირი (DRV) |
არ არის |
არ არის |
--- (თუ დამატებულია RTV, იხ. RTV№). |
|||||
ფოსამპრენავირი (FPV) |
მცირედ |
ამპრენავირის |
დააკვირდით და მოახდინეთ დოზის ტიტრაცია მეთადონთან |
|||||
ინდინავირი (IDV) |
არ არის |
კლინიკურად უმნიშვნელო ურთიერთქმედება |
--- (თუ დამატებულია RTV, იხ. RTV№). |
|||||
ლოპინავირი/რიტონავირი (LPV/r). |
მნიშვნელოვანი შემცირება |
არ არის |
შესაძლებელია მეთადონის აღკვეთის სინდრომის |
|||||
ნელფინავირი (NFV) |
ამცირებს მეთადონის |
მცირედ დაქვეითებული, მაგრამ არა |
აღკვეთის სინდრომი კლინიკურად იშვიათად აღინიშნება; |
|||||
რიტონავირი (RTV) |
ამცირებს მეთადონის |
არ არის |
შეიძლება საჭირო გახდეს მეთადონის უფრო მაღალი |
|||||
საქვინავირი (SQV) |
არ არის |
არ არის |
--- (თუ დამატებულია RTV, იხ. RTV№. |
|||||
ტიპრანავირი (TPV) |
არ არის |
არ არის |
--- (თუ დამატებულია RTV, იხ. RTV№) |
|||||
ინტეგრაზას ინჰიბიტორები |
||||||||
მარავიროკი (MRV) |
მონაცემები არ არის - |
მონაცემები არ არის - პოტენციურად |
|
|||||
რალტეგრავირი (RAL). |
არ არის |
არ არის |
|
|||||
- = კომენტარის გარეშე; --- = უცნობია; AUC = ფართობი მრუდის ქვეშ EC = ენტერული შემოგარსული; RTV = რიტინოვირი; RTVდამატებული = რიტინოვირი გამოყენებული სხვა მედიკამენტთან კომბინაციაში.
ცხრილი ადაპტირებულია შემდეგი წყაროებიდან: ინტრავენური ნარკოტიკების მომხმარებელი მოზარდების და მოზრდილების აივ-ის მკურნალობის სახელმძღვანელო [284], ლივერპულის აივ ფარმაკოლოგიური ჯგუფის ინტერნეტგვერდი, 2006 წლის ჯანდაცვის მსოფლიო ორგანიზაციის ანტირეტროვირუსული თერაპიის [285] და ჯანმრთელობის და ადამიანის მომსახურების დეპარტამენტის სახელმძღვანელოები ანტირეტროვირუსული აგენტების გამოყენების შესახებ აივ-1-ით ინფიცირებულ მოზრდილებში და მოზარდებში [286].
ცხრილი A5.3 ურთიერთქმედება ანტირეტროვირუსულ აგენტებსა და ბუპრენორფინს შორის |
|||
ანტირეტროვირუსული |
მოქმედება ბუპრენორფინზე |
ბუპრენორფინის |
კომენტარი |
ნუკლეოზიდის/ნუკლეოტიდის შებრუნებითი ტრანსკრიპტაზას ინჰიბიტორები |
|||
აბაკავირი (ABC) |
--- |
--- |
პოტენციური ურთიერთქმედება, რის გამოც შეიძლება |
დიდანოზინი (ddl) |
არ არის |
არ არის |
_ |
ემტრიციტაბინი (FTC) |
არ არის |
არ არის |
_ |
ლამივუდინი (3TC) |
არ არის |
არ არის |
_ |
სტავუდინი (d4T) |
არ არის |
არ არის |
_ |
ტენოფოვირი (TDF) |
არ არის |
არ არის |
_ |
ზიდოვუდინი (AZT) |
არ არის |
არ არის |
_ |
არანუკლეოზიდური რევერსიული ტრანსკრიპტაზას ინჰიბიტორები (NNRTIs) |
|||
ეფავირენზი (EFV) |
ბუპრენორფინის |
არ არის |
დააკვირდით, შეიძლება საჭირო |
ეტრავირინი (TMC-125) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
ნევირაპინი (NVP) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
პროტეაზას ინჰიბიტორები (PIs) |
|||
ატაზანავირი (ATV) |
ბუპრენორფინის ეფექტის |
არ არის |
დააკვირდით. შეიძლება, |
დარუნავირი (DRV) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
ფოსამპრენავირი (FPV) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
ინდინავირი (IDV) |
ბუპრენორფინის |
მონაცემები არ არის. |
დააკვირდით, |
ლოპინავირი/რიტონავირი (LPV/r) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
ნელფინავირი (NFV) |
მონაცემები არ |
მონაცემები არ არის. |
დააკვირდით |
რიტონავირი (RTV) |
ბუპრენორფინის ეფექტების |
მონაცემები არ არის. |
დააკვირდით, შეიძლება საჭირო |
საქვინავირი (SQV) |
ბუპრენორფინის |
მონაცემები არ არის. |
დააკვირდით, ხომ არ ვლინდება |
ტიპრანავირი (TPV) |
ბუპრენორფინის ეფექტების |
მონაცემები არ არის. |
დააკვირდით, ხომ არ ვლინდება |
ინტეგრაზას ინჰიბიტორები |
|||
მარავიროკი (MRV) |
მონაცემები არ |
მონაცემები არ არის. |
|
რალტეგრავირი (RAL). |
არ არის |
არ არის |
|
- = კომენტარის გარეშე, --- = უცნობია; EC = ენტერული შემოგარსული; RTV = რიტინოვირი; RTV-დამატებული = რიტინოვირი გამოყენებული სხვა მედიკამენტთან კომბინაციაში.
ცხრილი ადაპტირებულია შემდეგი წყაროებიდან: ინტრავენური ნარკოტიკების მომხმარებელი მოზარდების და მოზრდილების აივ-ის მკურნალობის სახელმძღვანელო [284], ლივერპულის აივ ფარმაკოლოგიური ჯგუფის ინტერნეტგვერდი, 2006 წლის ჯანდაცვის მსოფლიო ორგანიზაციის ანტირეტროვირუსული თერაპიის [285] და ჯანმრთელობის და ადამიანის მომსახურების დეპარტამენტის სახელმძღვანელოები ანტირეტროვირუსული აგენტების გამოყენების შესახებ აივ-1-ით ინფიცირებულ მოზრდილებში და მოზარდებში [286].
დანართი 6. ოპიოიდური დამოკიდებულების მკურნალობის ალტერნატივები, რომლებიც არ არის შესული მოცემულ სახელმძღვანელოში A6.1 ჰეროინით მხარდაჭერა
შეზღუდული მონაცემების გამო, არაადეკვატური იქნებოდა რაიმე რეკომენდაციის გაცემა ჰეროინით მხარდამჭერ მკურნალობაზე. |
ჰეროინის დანიშვნასთან დაკავშირებულმა კოქრეინის მიმოხილვამ გამოავლინა ხუთი რანდომიზებული კონტროლირებული კვლევა, რომლებშიც ჰეროინი შედარებული იყო მეთადონთან [287]. არსებული ექსპერიმენტული კვლევების შეუსაბამობის გამო, ჰეროინის დანიშვნის საერთო ეფექტიანობის შესახებ გადამწყვეტი დასკვნის გაკეთება არ იყო შესაძლებელი. ჰეროინის გამოყენება კლინიკურ პრაქტიკაში მრავალ ქვეყანაში ჯერ კიდევ კვლევის საგანია. ჰეროინით მკურნალობაზე (მეთადონთან შედარებით) დადებითი შედეგები მიღებულია იმ პაციენტებში, რომელთა მეთადონით მკურნალობა წარუმატებლად დამთავრდა.
A6.2 ნელი ან მდგრადი მოქმედების პერორალური მორფინი
შეზღუდული მონაცემების გამო, არაადეკვატური იქნებოდა რაიმე რეკომენდაციის გაცემა ნელი ან მდგრადი მოქმედების პერორალურ მორფინზე. |
მორფინის ახალი ფორმები შეიძლება გამოვიყენოთ დღეში ერთხელ მისაღებად ქრონიკული ტკივილის მკურნალობისთვის [288, 289, 290]. ბევრი კვლევაა ჩატარებული ამ ფორმების გამოყენებაზე ოპიოიდური დამოკიდებულების დროს [210, 291, 292, 293]. ამ კვლევების შედეგები იმედისმომცემია, ავლენს მორფინის ხანგრძლივ მოქმედებას და მეთადონთან შედარებით ჰეროინის მოხმარების ნაკლებ შემთხვევებს. ნარკომანიის მკურნალობისთვის მორფინის გამოყენება სიძნელეებთან არის დაკავშირებული, რადგან გართულებულია ჰეროინის მოხმარების შეფასება და დოზებზე ზედამხედველობა.
A6.3 ლევო-ალფა-აცეტილმეტადოლი
მართალია, ლევო-ალფა-აცეტილმეტადოლი (LAAM) შეერთებულ შტატებში ჯერ კიდევ რეგისტრირებულია, მაგრამ სიცოცხლისათვის საშიში არითმიების რისკის გამო მწარმოებლის მიერ ამოღებულია ბაზრიდან. |
ლევო-ალფა-აცეტილმეტადოლი (LAAM) გახანგრძლივებული მოქმედების ოპიოიდური აგონისტია, რომლის გამოყენება ნებადართულია ოპიოიდური ჩანაცვლებითი თერაპიისთვის. იმ პაციენტებში, რომლებშიც მეთადონი და ბუპრენორფინი ეფექტს არ იძლევა, აღმოჩნდა, რომ LAAM უკეთესად ახდენს ჰეროინის სუპრესიას ვიდრე მეთადონი ([294, 295]), მაგრამ ამჟამად მისი გამოყენება შეზღუდულია QT ინტერვალის გახანგრძლივების გამო [296]. აქტიურ მეტაბოლიტს - ნორაცეტილმეტადოლს არ აქვს ისეთივე ეფექტი QT ინტერვალის გახანგრძლივებაზე [131, 297] და შეიძლება იმედისმომცემი ალტერნატივა იყოს.
A6.4 ბუპრენორფინ-ნალოქსონის კომბინაცია
შეზღუდული მონაცემების გამო, არაადეკვატური იქნებოდა ბუპრენორფინ-ნალოქსონის კომბინაციასთან დაკავშირებით რაიმე რეკომენდაციის გაცემა. თუმცა, როგორც ჩანს, კომბინაცია მხოლოდ ბუპრენორფინის მიღების მსგავსი ეფექტიანობით ხასიათდება. |
ბევრ ქვეყანაში, მეთადონის მსგავსად, დაფიქსირებულია ბუპრენორფინის ინტრავენური შეყვანის შემთხვევები [119, 128, 298, 299, 300, 301, 302, 303]. ბუპრენორფინი-ნალოქსონი შეიცავს ნაწილობრივ აგონისტს ბუპრენორფინს ოპიოიდურ ანტაგონისტ ნალოქსონთან კომბინაციაში შეფარდებით 4:1. ეს კომბინაცია იმ იმედით შეიქმნა, რომ ნალოქსონის დამატებით მიღებული პროდუქტი ნაკლებად იქნებოდა გამოყენებული ვენაში ინექციისთვის, ვიდრე მხოლოდ ბუპრენორფინი. კომბინაციის ენის ქვეშ მიღებისას ნალოქსონის აბსორბცია მინიმალურია და მას ბუპრენორფინის ოპიოიდური აგონისტის ეფექტი გადაწონის. თუმცა, როცა ბუპრენორფინი-ნალოქსონის ტაბლეტი ინტრავენურად შეიყვანება, სხვა ოპიოიდებზე დამოკიდებულ ადამიანებში (ბუპრენორფინის გარდა) ნალოქსონი გამოიწვევს აბსტინენციის სინდრომს.
ბუპრენორფინი-ნალოქსონის ეფექტიანობა ოპიოიდური დამოკიდებულების ჩანაცვლებით თერაპიაში აღწერილია სამ რანდომიზებულ კონტროლირებულ კვლევაში. ამ კვლევებში კომბინაცია შეადარეს პლაცებოს [305] და კლონიდინს [226], ასევე, მხოლოდ მეთადონის გამოყენებას [306]. გამოქვეყნებულია სამი კვლევა, სადაც გამოკვლეული იყო კომბინაციის ეფექტიანობა სხვადასხვა კონსულტაციებთან ან მედიკამენტის განაწილების რეჟიმებთან ერთად [307, 308, 309].
A6.5 ნელი მოქმედების ნალტრექსონის იმპლანტები და ინექციები
შეზღუდული მონაცემების გამო, არაადეკვატური იქნებოდა რაიმე რეკომენდაციის გაცემა ნალტრექსონის იმპლანტების და ინექციების გამოყენებაზე |
კლინიკურ კვლევებში საინექციო, ნელი მოქმედების ნალტრექსონის ფორმა იძლევა ოპიოიდების კლინიკურად მნიშვნელოვან ბლოკადას 3-6 კვირის განმავლობაში (დოზის მიხედვით) [310, 311, 312, 313, 314].
ნალტრექსონის მრავალი იმპლანტია შემუშავებული, რომლებიც კანქვეშ თავსდება ადგილობრივი ანესთეზიის პირობებში ოპიოიდების მოხსნის შემდეგ ან როგორც ანტაგონისტით მოხსნის ნაწილი. ნალტრექსონის ეფექტიანობის შემფასებელი რანდომიზებული კონტროლირებული კვლევები არ არის, თუმცა, გარკვეული იმედისმომცემი შედეგები არსებობს [315, 316, 317, 318]. აღწერილია ადგილობრივი იმპლანტებით გამოწვეული ადგილობრივი ალერგიები და ინფექციები.
 |
16 დანართი 7. მეთადონი, ბუპრენორფინი და ნარკოტიკების კონტროლის საერთაშორისო კონვენციები |
▲back to top |
ერთობლივი კონვენცია ნარკოტიკული პრეპარატების შესახებ (1961, რომელიც შესწორებული იქნა 1972 წ. პროტოკოლის მიხედვით) და 1971 წლის კონვენცია ფსიქოტროპული ნივთიერებების შესახებ მოიცავს სპეციფიკური კონტროლის პირობებს ზოგიერთი ფსიქოაქტიური ნივთიერებებისთვის [321, 322]. ამ კონვენციების მიხედვით, ნარკოტიკული პრეპარატების კომისიას (CND) აქვს უფლებამოსილება, ჯანდაცვის მსოფლიო ორგანიზაციის რეკომენდაციით გადაწყვიტოს საჭიროა თუ არა, ნივთიერების, როგორც ნარკოტიკის ან ფსიქოტროპული ნივთიერების დარეგისტრირება.
მეთადონი დღესდღეობით მიჩნეულია „ნარკოტიკულ ნივთიერებად“ და რეგულირდება ნარკოტიკული ნივთიერებების ერთობლივი კონვენციით, ხოლო ბუპრენორფინი მიჩნეულია „ფსიქოტროპულ ნივთიერებად“ და რეგულირდება ფსიქოტროპული ნივთიერებების კონვენციით.
ნარკოტიკების კონტროლის საერთაშორისო საბჭოს (INCB) ფუნქციაა, დააკვირდეს მთავრობების მიერ ზემოთ ჩამოთვლილი საერთაშორისო შეთანხმებების შესრულებას, უზრუნველყოს, ერთი მხრივ, კონტროლირებული ნივთიერებების ხელმისაწვდომობა სამედიცინო და სამეცნიერო მიზნებისათვის, მეორე მხრივ, კი ამ ნივთიერებების კანონიერი გამოყენებიდან უკანონო გამოყენებაზე გადასვლის თავიდან აცილება [321].
A7.1 ერთობლივი კონვენცია ნარკოტიკულ ნივთიერებებზე (1961)
ერთობლივი კონვენცია ნარკოტიკულ ნივთიერებებზე არის ოპიოიდების კონტროლის მარეგულირებელი მთავარი საერთაშორისო შეთანხმება. მისი მიზანია, რომ ნარკოტიკული პრეპარატების წარმოება, დამზადება, ექსპორტი, იმპორტი, განაწილება, ვაჭრობა, გამოყენება და ფლობა შემოიფარგლებოდეს მხოლოდ სამედიცინო და სამეცნიერო მიზნებით. 1961 წლის ერთობლივი კონვენციის მიხედვით, ნარკოტიკულ პრეპარატებად მიიჩნევა ჰეროინი, ოპიუმი, მორფინი, ოქსიკოდონი, მეთადონი და სხვა ძლიერი ფარმაცევტული ოპიოიდების უმრავლესობა (ბუპრენორფინის გამოკლებით).
მეთადონის კონვენციასთან შესაბამისობისათვის საჭიროა, რომ ქვეყნებმა შეასრულონ შემდეგი პირობები:
მეთადონზე ყოველწლიური სამედიცინო და სამეცნიერო მოთხოვნილების დათვლა და შედეგების გაგზავნა INCB-ში დასამტკიცებლად;
მეთადონის წარმოების და იმპორტის შეზღუდვა მხოლოდ საჭირო რაოდენობამდე, საექსპორტო რაოდენობის გათვალისწინებით;
უზრუნველყოფა, რომ ყველა ეტაპზე, - წარმოებიდან ან შემოტანიდან განაწილებამდე, - მეთადონი ლიცენზირებული მფლობელის ხელში იყოს;
მეთადონის რეცეპტის საფუძველზე გაცემის უზრუნველყოფა;
ანგარიშის მიწოდება INCB-თვის, თუ რამდენი მეთადონი იქნა შემოტანილი, გატანილი, წარმოებული და გამოყენებული და რა მარაგი არსებობს;
ნარკოტიკული პრეპარატების მწარმოებლების, ექსპორტიორების, იმპორტიორების და საბითუმო და საცალო მოვაჭრეების, ასევე, სამედიცინო დაწესებულებების (სადაც ასეთი ნივთიერებები გამოიყენება) ინსპექტირების სისტემის არსებობა; ტერიტორიის, მარაგების და ჩანაწერების შემოწმება;
მეთადონის არასათანადო გამოყენების თავიდან აცილების უზრუნველყოფა.
ოპიოიდების სამედიცინო საჭიროების შეფასება ქვეყანაში
წამლის მარეგულირებელმა ეროვნულმა სააგენტომ ყოველ წელს უნდა მოამზადოს მომდევნო წელს ქვეყანაში მეთადონზე მოთხოვნის შეფასება. ეს შეფასება უნდა გაიგზავნოს INCB-ში შეფასების პერიოდამდე ექვსი თვით ადრე, თუმცა, დამატებითი შეფასების გაგზავნა ნებისმიერ დროსაა შესაძლებელია. ექსპორტიორი ქვეყნების საყურადღებოდ INCB ყოველთვიურად აქვეყნებს მთავრობიდან მიღებულ შეფასებებს. ქვეყანაში სამედიცინო და სამეცნიერო მიზნით საჭირო ოპიოიდების რაოდენობის განსაზღვრა მთლიანად ქვეყნის მთავრობის პასუხისმგებლობაა, მაგრამ INCB-ს დანართი 7. მეთადონი, ბუპრენორფინი და ნარკოტიკების კონტროლის საერთაშორისო კონვენციები ინფორმაცია უნდა მიეწოდოს შეფასებისთვის გამოყენებული მეთოდის შესახებ. INCB ნარკოტიკულ პრეპარატებზე ყოველწლიურ მოთხოვნილებას იმ ქვეყნებისთვის აფასებს, რომლებსაც თავად არ შეუძლია ამ შეფასების გაკეთება. თუ რომელიმე ქვეყნისთვის შეფასება INCB-ის მიერ არის გაკეთებული, საბჭო ამ ინფორმაციას განსახილველად ამ ქვეყნის ხელმძღვანელობას უგზავნის.
მეთადონის მარაგის მიღება
მას შემდეგ, რაც ქვეყანა INCB-გან მიიღებს შეფასების დადასტურებას, შესაძლებელია წარმოების ან იმპორტის პროცედურების დაწყება. ორივე შემთხვევაში, მნიშვნელოვანია, რომ მოწოდება საიმედო იყოს, რადგან მეთადონის მოწოდების შეფერხება დიდი სტრესია პაციენტებისთვის და ქმნის უკანონო ოპიოიდების გამოყენების განახლების რისკს.
ადგილობრივი წარმოება
მეთადონის საჭირო რაოდენობა ან მისი ნაწილი შეიძლება იწარმოებოდეს ქვეყანაში არსებულ საწარმოებში მთავრობის ზედამხედველობით. ოპიოიდების წარმოების რეგულირება გულისხმობს ლიცენზირებას, მოთხოვნებს ჩანაწერების წარმოებასა და ანგარიშგებაზე, უსაფრთხო შენახვაზე და ხარისხის კონტროლზე.
იმპორტის/ექსპორტის სისტემა
კონვენციაში გათვალისწინებულია ეტაპების სპეციფიკური თანმიმდევრობა ნარკოტიკული პრეპარატების იმპორტისა და ექსპორტისათვის, თუმცა, ამა თუ იმ ქვეყანას შეიძლება დამატებითი მოთხოვნებიც ჰქონდეს. მეთადონის იმპორტი და ექსპორტი მხოლოდ წამლის ეროვნული მარეგულირებელი უწყების ნებართვით და ქვეყანაში ამ პრეპარატზე მოთხოვნილების შეფასების გათვალისწინებითაა შესაძლებელი. თითოეულ გასაგზავნ პარტიას თან უნდა ახლდეს ნებართვა ექსპორტზე.
იმპორტის და ექსპორტის ნებართვა უნდა მოიცავდეს შემდეგ ინფორმაციას:
პრეპარატის დასახელება;
პრეპარატის საერთაშორისო დასახელება;
იმპორტირებული ან ექსპორტირებული პრეპარატის რაოდენობა;
იმპორტიორის ან ექსპორტიორის დასახელება და მისამართი;
ნებართვის ძალაში ყოფნის პერიოდი.
ექსპორტის ნებართვაში ასევე შეიძლება იყოს ნებართვის ნომერი, გაცემის თარიღი და ვის მიერ იქნა გაცემული.
იმპორტის/ექსპორტის პროცესის ეტაპები
იმპორტი/ექსპორტის პროცესი მოცემულია ქვემოთ A7.1 სურათზე. ბევრ ქვეყანაში ასევე მოქმედებს ნებართვის/სერტიფიცირების პროცედურა, რომლის მიზანია არასწორი ეტიკეტით, ყალბი ან სტანდარტებთან შეუსაბამო ფარმაცევტული პროდუქტების ბაზარზე მოხვედრის თავიდან აცილება:
1. ორგანიზაცია, რომელსაც სურს პირველი კონვენციით კონტროლირებული ნივთიერების იმპორტი, მიმართავს მარეგულირებელ ორგანოს იმპორტზე ნებართვისთვის.
2. მარეგულირებელი ორგანო განიხილავს, არის თუ არა კომპანია სათანადოდ ლიცენზირებული; შეესაბამება თუ არა პრეპარატი და მისი რაოდენობა ქვეყანაში არსებული მოთხოვნის შეფასებას; დასტურის შემთხვევაში, გაიცემა იმპორტზე ნებართვის ორიგინალი და ასლების შესაბამისი რაოდენობა. ორიგინალი და ერთი ასლი უნდა გაეგზავნოს იმპორტიორს, რომელიც ორიგინალს უგზავნის ექსპორტიორს, ერთი ასლი ინახება საბაჟოზე წარსადგენად, ერთი ასლი უნდა გაეგზავნოს შემომტანი ქვეყნის საბაჟოს, ხოლო კიდევ ერთი ასლი უნდა შეინახონ შემომტანი ქვეყნის შესაბამისი უწყების დოკუმენტებში.
3. შემოტანის ნებართვის ორიგინალს იმპორტიორი უგზავნის ნივთიერების ექსპორტზე პასუხისმგებელ კომპანიას.
4. ექსპორტიორი მიმართავს თავისი ქვეყნის მარეგულირებელ ორგანოს ექსპორტზე ნებართვისთვის.
5. ექსპორტიორი ქვეყნის მარეგულირებელი ორგანო ამოწმებს, გაცემულია თუ არა ნებართვა იმპორტზე და აქვს თუ არა ექსპორტიორს შესაბამისი ლიცენზია, ასევე, არის თუ არა მოთხოვნილების შესაბამისი იმპორტიორი ქვეყნის მიერ შესყიდული რაოდენობა; თუ განაცხადი დამტკიცდა, გაიცემა ნებართვა ექსპორტზე.
6. მარეგულირებელი ორგანო ექსპორტიორ ქვეყანაში ექსპორტის ნებართვის ასლს უგზავნის იმპორტიორი ქვეყნის მარეგულირებელ ორგანოს. ექსპორტიორს უნდა მიეწოდოს ორი ასლი, რომელთაგან ერთი თან უნდა ახლდეს ტვირთს. ერთი ასლი უნდა გაეგზავნოს ექსპორტიორი ქვეყნის საბაჟოს, ხოლო კიდევ ერთი ასლი უნდა შეინახონ ქვეყანაში შესაბამისი უწყების დოკუმენტებში.
7. ექსპორტიორი პრეპარატს იმპორტიორს ექსპორტზე ნებართვასთან ერთად უგზავნის.
8. ტვირთმა უნდა გაიაროს საბაჟო შემოწმება.
9. იმპორტიორი ექსპორტის ნებართვას უგზავნის თავის მარეგულირებელ უწყებას. იმპორტიორი ქვეყნის მარეგულირებელი ორგანო ექსპორტზე ნებართვას უბრუნებს ექსპორტიორი ქვეყნის მარეგულირებელ ორგანოს დოკუმენტით, რომელიც ადასტურებს ფაქტობრივად შემოტანილ რაოდენობას.
სურათი A7.1 ოპიოიდების იმპორტის ეტაპები

შეტყობინების სისტემები
ყოველ კვარტალში წამლის ეროვნულმა მარეგულირებელმა ორგანომ INCB-ს უნდა მიაწოდოს ანგარიში მეთადონის იმპორტის და ექსპორტის თითოეული შემთხვევის შესახებ. მათ ასევე მოეთხოვებათ ყოველწლიურად წარმოებული, მოხმარებული და მარაგში დაგროვილი ოპიოიდების საერთო რაოდენობის აღწერა და ანგარიშის მომზადება. ყოველწლიური აღწერა არ მოიცავს აფთიაქებში შენახულ მედიკამენტებს, რომლებიც ოფიციალურად განიხილება, როგორც მოხმარებული.
სამედიცინო პერსონალის მუშაობის რეგულირება
კონვენცია განმარტავს, რომ ცალკეული ქვეყნის მთავრობამ უნდა გადაწყვიტოს ოპიოიდების განაწილებაში უშუალოდ ჩართული პერსონალის (ფარმაცევტები, ექიმები და ექთნები) მუშაობის რეგულირების (კონტროლის) დონე. თუმცა, მასში გაცხადებულია რამდენიმე პრინციპი, რომელთა დაცვა აუცილებელია:
საჭიროა, პიროვნებას ჰქონდეს ოპიოიდების გაცემის უფლება - ეს უფლება შეიძლება მიენიჭოს პროფესიული ლიცენზიის საშუალებით ან ამისათვის სპეციალური ლიცენზიის გაცემით.
ერთი ადგილიდან მეორეზე გადატანისას ოპიოიდები ყოველთვის უნდა იყოს უფლებამოსილი მხარეების ხელში.
ოპიოიდების გასაცემად საჭიროა სამედიცინო რეცეპტი.
მედიკამენტი, როგორც ნარკოტიკული და როგორც პაციენტისთვის საჭირო ნივთიერება
კონვენციაში გაცხადებულია, რომ მთავრობებს აქვთ უფლება (თუ საჭიროდ მიიჩნევენ) დააწესონ დამატებითი შეზღუდვები ოპიოიდების არასათანადო და არასწორი გამოყენების თავიდან ასაცილებლად. თუმცა, ეს უფლება მუდმივად უნდა იყოს გაწონასწორებული მთავრობის პასუხისმგებლობასთან, რათა მუდმივად იყოს ხელმისაწვდომი სამედიცინო მიზნებისთვის საჭირო ოპიოიდები.
კონტროლის ინტენსივობის განსაზღვრის პროცესში მთავრობებს უნდა ახსოვდეთ კონვენციის ორმაგი მიზანი. INCB-ის დაკვირვებით ზოგიერთ ქვეყანაში ნარკომანიის მიმართ შიშმა იმგვარი კანონების და წესების (ან მათი ინტერპრეტაციის) მიღება გამოიწვია, რომლებიც არასაჭირო სირთულეებს ქმნის ოპიოიდების სამედიცინო მიზნებით გამოყენებისას.
„... ოპიოიდების კანონიერი გამოყენების ხელმისაწვდომობის შეზღუდვა ყოველთვის არ ნიშნავს ოპიოიდების უკანონო მოხმარების შეზღუდვას. ზოგადად, ოპიოიდების კანონიერ ხელმისაწვდომობაზე ზედმეტი შეზღუდვების დაწესებამ შეიძლება მოსახლეობის დიდი ნაწილისთვის ოპიოიდები მიუწვდომელი გახადოს სამედიცინო მიზნით გამოსაყენებლად“ [324].
A7.2 კონვენცია ფსიქოტროპული ნივთიერებების შესახებ (1971)
ითვალისწინებს რა მათი არადანიშნულებით მოხმარების პოტენციალს და თერაპიულ მნიშვნელობას, ეს კონვენცია აწესებს საერთაშორისო კონტროლის სისტემას ფსიქოტროპულ ნივთიერებებზე. ბუპრენორფინი შესულია ფსიქოტროპული ნივთიერებების ჩამონათვალში და კონვენციის III ცხრილში.
ბუპრენორფინის გამოყენებისას, კონვენციასთან შესაბამისობისათვის, ქვეყნებს მოეთხოვება შემდეგი:
წარმოებიდან შემოტანამდე და განაწილებამდე ბუპრენორფინი მუდმივად უნდა რჩებოდეს ლიცენზირებული უწყების ხელში;
ბუპრენორფინის მხოლოდ სამედიცინო რეცეპტით გაცემის უზრუნველყოფა;
ფართო საზოგადოებისთვის ბუპრენორფინის რეკლამირების აკრძალვა;
მოთხოვნის დაწესება, რომ ყველა უწყებამ, რომელიც ჩართულია ბუპრენორფინის წარმოებაში, ვაჭრობაში ან განაწილებაში, აწარმოოს ჩანაწერები თითოეული პარტიის მიღებაგაცემაზე და შეინახოს, სულ ცოტა, ბოლო ორი წლის დოკუმენტაცია;
INCB-ისთვის ყოველწლიური ანგარიშის გაგზავნა შემოტანილი, გატანილი და წარმოებული ბუპრენორფინის თაობაზე;
სისტემების შემუშავება ინსპექტირების დასაწესებლად ფსიქოტროპული ნივთიერებების მწარმოებლებზე, ექსპორტიორებზე, იმპორტიორებზე და საბითუმო და საცალო მოვაჭრეებზე, აგრეთვე, იმ სამედიცინო და სამეცნიერო ინსტიტუტებზე, რომლებიც ამ ნივთიერებებს იყენებენ; საჭიროა ტერიტორიის, მარაგების და ჩანაწერების შემოწმება;
ბუპრენორფინის არადანიშნულებით გამოყენების თავიდან აცილების უზრუნველყოფა.
ადგილობრივი წარმოება
მეთადონის საჭირო რაოდენობა ან მისი ნაწილი შეიძლება იწარმოებოდეს ქვეყანაში არსებულ საწარმოებში მთავრობის ზედამხედველობით. ფსიქოტროპული ნივთიერებების წარმოების რეგულირება გულისხმობს ლიცენზირებას, მოთხოვნებს ჩანაწერების წარმოებასა და ანგარიშგებაზე. ასევე დაცული უნდა იყოს ზოგადად ფარმაცევტული პროდუქციისთვის საჭირო პირობები, როგორებიცაა: უსაფრთხო შენახვა და ხარისხის კონტროლი.
სამედიცინო პერსონალის მუშაობის რეგულირება
კონვენცია განმარტავს, რომ ცალკეული ქვეყნის მთავრობამ უნდა გადაწყვიტოს ფსიქოტროპული ნივთიერებების განაწილებაში უშუალოდ ჩართული პერსონალის (ფარმაცევტები, ექიმები და ექთნები) მუშაობის რეგულირების (კონტროლის) დონე. თუმცა, მასში გაცხადებულია რამდენიმე პრინციპი, რომელთა დაცვა აუცილებელია:
საჭიროა, პიროვნებას ჰქონდეს ფსიქოტროპული ნივთიერებების გაცემის უფლება - ეს უფლება შეიძლება მიენიჭოს პროფესიული ლიცენზიის საშუალებით ან ამისათვის სპეციალური ლიცენზიის გაცემით.
გადატანისას ფსიქოტროპული ნივთიერებები ყოველთვის უნდა რჩებოდეს უფლებამოსილი მხარეების ხელში.
პაციენტზე ფსიქოტროპული ნივთიერებების გასაცემად საჭიროა სამედიცინო რეცეპტი, გარდა იმ შემთხვევებისა, როცა პირს შეუძლია კანონიერად მიიღოს, გამოიყენოს, გასცეს ან დანიშნოს ეს ნივთიერებები თერაპიული ან სამეცნიერო მიზნით.
რეცეპტები უნდა გაიცეს სწორი სამედიცინო პრაქტიკის შესაბამისად საზოგადოებრივი ჯანმრთელობის და კეთილდღეობის დამცველი კანონების საფუძველზე. განსაკუთრებით, ყურადღება უნდა მიექცეს, რამდენჯერ შეიძლება ამ რეცეპტების განახლება და რამდენი ხნის განმავლობაშია რეცეპტი ძალაში.
მედიკამენტი, როგორც ნარკოტიკული და როგორც პაციენტისთვის საჭირო ნივთიერება
კონვენციაში გაცხადებულია, რომ მთავრობებს აქვთ უფლება (თუ საჭიროდ მიიჩნევენ), დააწესონ დამატებითი შეზღუდვები ფსიქოტროპული ნივთიერებების არასათანადო და არასწორი გამოყენების თავიდან ასაცილებლად. თუმცა, ეს უფლება უნდა შეჯერდეს მთავრობის პასუხისმგებლობასთან და უზრუნველყოფილ უნდა იქნეს სამედიცინო მიზნებისთვის საჭირო ფსიქოტროპული ნივთიერებების მუდმივი წვდომა.
ბუპრენორფინის მოწოდების უზრუნველყოფა
ბუპრენორფინის საიმედო მოწოდების უზრუნველყოფა უმნიმნიშვნელოვანესია, რადგან მოწოდების შეფერხება დიდი სტრესია პაციენტისთვის და ზრდის უკანონო ოპიოიდების მოხმარების განახლების რისკს. მართალია, კონვენციით მოთხოვნილი არ არის, მაგრამ ექსპორტიორი ქვეყნების უმრავლესობა იღებს კონტროლის დამატებით ნებაყოფლობით ზომებს, რომლებიც რეკომენდებულია ECOSOC-ის მიერ (იხ. ქვემოთ). პრაქტიკულ საქმიანობაში ყველა იმპორტიორი ქვეყნის მთავრობას უნდა ახსოვდეს, რომ ბუპრენორფინის შემოტანა შეიძლება გართულდეს, თუ არ არის შეფასებული ბუპრენორფინის საჭიროება (ფსიქოტროპულ ნივთიერებებზე ყოველწლიური მოთხოვნის გამარტივებული შეფასება) და არ არსებობს იმპორტზე ნებართვა ან დაშვების სერტიფიკატი თითოეული იმპორტისთვის.
ბუპრენორფინის სამედიცინო საჭიროების შეფასება ECOSOC-ის 1993/38 რეზოლუციის მიხედვით
წამლის მარეგულირებელმა ეროვნულმა უწყებებმა უნდა მოამზადონ ქვეყანაში ბუპრენორფინზე ყოველწლიური მოთხოვნილების შეფასება. INCB გვირჩევს, რომ ეს შეფასება, სულ ცოტა, წელიწადში სამჯერ გადაისინჯოს. შეფასების გადასინჯვა და მასში შესწორების შეტანა ნებისმიერ დროს შეიძლება. სამედიცინო და სამეცნიერო მიზნებისთვის საჭირო ბუპრენორფინის რაოდენობის განსაზღვრაზე პასუხისმგებლობა მთლიანად ქვეყნის მთავრობამ უნდა აიღოს. INCB ყოველთვიურად აქვეყნებს შეფასებებში შეტანილ ცვლილებებს, რის მიხედვითაც ხელმძღვანელობენ ექსპორტიორი ქვეყნები.
იმპორტ-ექსპორტის სისტემა
კონვენციაში მოცემულია ფსიქოტროპული ნივთიერებების იმპორტისა და ექსპორტისთვის საჭირო ეტაპები სპეციფიკური თანმიმდევრობით. ECOSOC-ის მიერ რეკომენდებულია დამატებითი მოთხოვნები, რომელთაც ქვეყნების უმრავლესობა ასრულებს.
1. კონვენციით გათვალისწინებული სავალდებულო კონტროლი
კონვენციით იმპორტ-ექსპორტის ნებართვა სავალდებულოდ ითვლება მხოლოდ I და II ცხრილებში მოცემული ნივთიერებებისთვის.
III ცხრილში შეტანილი ნივთიერებების (ბუპრენორფინი) ექსპორტისას ექსპორტიორებმა ექსპორტის დეკლარაციის ორი ასლი უნდა შეიტანონ ექსპორტიორი ქვეყნის შესაბამის უწყებაში, ექსპორტის დეკლარაციის მესამე ასლი კი თან უნდა ახლდეს მედიკამენტის პარტიას. ექსპორტიორი ქვეყნის მთავრობამ ექსპორტის დელკარაცია რაც შეიძლება სწრაფად უნდა გადაუგზავნოს იმპორტიორი ქვეყნის შესაბამის ორგანოებს, არა უგვიანეს ტვირთის გაგზავნიდან 90 დღისა. ზოგიერთ ქვეყანაში შეიძლება საჭირო იყოს იმპორტიორის მიერ ტვირთის თანმხლები ასლის გაგზავნა იმპორტიორი ქვეყნის შესაბამის უწყებაში, მიღებული მედიკამენტის რაოდენობის და ტვირთის ჩამოსვლის თარიღის მითითებით.
ექსპორტის დეკლარაცია უნდა მოიცავდეს შემდეგ ინფორმაციას:
ნივთიერების საერთაშორისო, არა კერძო (INN) დასახელება. ასეთის არარსებობის შემთხვევაში მითითებული უნდა იყოს ნივთიერების ადგილი ცხრილში;
ნივთიერების რაოდენობა და ფარმაცევტული ფორმა, თუ პრეპარატის ფორმითაა - პრეპარატის დასახელება;
იმპორტიორის დასახელება და მისამართი;
ექსპორტიორის დასახელება და მისამართი;
გაგზავნის თარიღი.
2. ECOSOC-ით გათვალისწინებული ნებაყოფლობითი კონტროლის ზომები
ECOSOC-ის 1996/30 რეზოლუციის შესაბამისად, ქვეყნების უმრავლესობა იმპორტ-ექსპორტის ნებართვის სისტემას III და IV ცხრილში შეტანილი ნივთიერებებისთვისაც იყენებს, მათ შორის, ბუპრენორფინისთვის. იმპორტი შეიძლება განხორციელდეს მხოლოდ იმპორტიორი ქვეყნის წამლის მარეგულირებელი ეროვნული უწყების ნებართვით. შემოტანილი რაოდენობა უნდა შეესაბამებოდეს იმპორტიორი ქვეყნის მიერ გაკეთებულ შეფასებას ბუპრენორფინის საჭიროებაზე. თითოეულ პარტიას უნდა ახლდეს ექსპორტის ნებართვა.
იმპორტის ნებართვა უნდა შეიცავდეს შემდეგ ინფორმაციას:
ნებართვის ნომერი;
გაცემის თარიღი;
ვის მიერ იქნა გაცემული;
ნივთიერებ(ებ)ის საერთაშორისო არაკერძო დასახელება (INN). ასეთის არარსებობის შემთხვევაში უნდა მიეთითოს ნივთიერების ადგილი ცხრილში;
ნივთიერების ფარმაცავტული ფორმა და რაოდენობა, თუ პრეპარატის ფორმითაა - პრეპარატის დასახელება;
იმპორტიორის დასახელება და მისამართი;
ექსპორტიორის დასახელება და მისამართი;
ნებართვის ძალაში ყოფნის პერიოდი.
იმპორტ-ექსპორტის პროცესის ეტაპები, ECOSOC-ის რეზოლუციაში მოცემული რეკომენდაციების შესაბამისად
ორგანიზაცია, რომელსაც სურს ბუპრენორფინის იმპორტი, მიმართავს მარეგულირებელ ორგანოს იმპორტზე ნებართვისთვის.
მარეგულირებელი ორგანო განიხილავს, არის თუ არა კომპანია სათანადოდ ლიცენზირებული და შეესაბამება თუ არა პრეპარატი და მისი რაოდენობა ქვეყანაში არსებული მოთხოვნის შეფასებას; დასტურის შემთხვევაში გაიცემა იმპორტზე ნებართვის ან „აკრძალვის არარსებობის“ სერტიფიკატის ორიგინალი და ასლების შესაბამისი რაოდენობა (ერთი ასლი უნდა გაეგზავნოს ექსპორტიორი ქვეყნის შესაბამის ორგანოებს. ორიგინალი და ერთი ასლი - იმპორტიორს, რომელიც ორიგინალს უგზავნის ექსპორტიორს, ერთი ინახება საბაჟოზე წარსადგენად, ერთი ეგზავნება შემომტანი ქვეყნის საბაჟოს, კიდევ ერთი კი შენახულ უნდა იქნეს შემომტანი ქვეყნის შესაბამისი უწყების არქივში).
შემოტანის ნებართვის ან სერტიფიკატის ორიგინალს იმპორტიორი უგზავნის ნივთიერების ექსპორტზე პასუხისმგებელ კომპანიას.
ექსპორტიორი მიმართავს თავისი ქვეყნის მარეგულირებელ ორგანოს ექსპორტზე ნებართვისთვის.
ექსპორტიორი ქვეყნის მარეგულირებელი ორგანო ამოწმებს, გაცემულია თუ არა ნებართვა იმპორტზე, აქვს თუ არა ექსპორტიორს შესაბამისი ლიცენზია და შეესაბამება თუ არა რომ იმპორტიორი ქვეყნის მიერ შესყიდული რაოდენობა მოთხოვნილებას; თუ განაცხადი დამტკიცდა, გაიცემა ნებართვა ექსპორტზე.
მარეგულირებელი ორგანო ექსპორტიორ ქვეყანაში ექსპორტის ნებართვის ასლს უგზავნის იმპორტიორი ქვეყნის მარეგული რებელ ორგანოს. ექსპორტიორს უნდა მიეწოდოს ორი ასლი, რომელთაგან ერთი თან უნდა ახლდეს ტვირთს. ერთი ასლი უნდა გაეგზავნოს ექსპორტიორი ქვეყნის საბაჟოს, ერთი კი შენახულ უნდა იქნეს ქვეყნის შესაბამისი უწყების არქივში.
ექსპორტიორი პრეპარატს უგზავნის იმპორტიორს ექსპორტზე ნებართვასთან ერთად.
ტვირთმა უნდა გაიაროს საბაჟო შემოწმება.
იმპორტიორი ექსპორტის ნებართვას უგზავნის თავის მარეგულირებელ უწყებას. იმპორტიორი ქვეყნის მარეგულირებელი ორგანო ექსპორტზე ნებართვას უბრუნებს ექსპორტიორი ქვეყნის მარეგულირებელ ორგანოს მედიკამენტის ფაქტობრივად შემოტანილი რაოდენობის დამადასტურებელ დოკუმენტთან ერთად.
A7.3 სამედიცინო პერსონალის მუშაობის რეგულირების მეთოდები
კანონით გათვალისწინებული მოთხოვნები პაციენტებზე ოპიოიდის გამცემი ექიმების, ექთნების და ფარმაცევტების მიმართ, ბუნებრივია, სხვადასხვა ქვეყანაში განსხვავებულია. თუმცა, ქვემოთ მოცემულია ზოგადი კრიტერიუმები, რომელთა გამოყენება შესაძლებელია პრაქტიკული სისტემის შემუშავებისათვის:
1. ლეგალური ნებართვა: ექიმებს, ექთნებს და ფარმაცევტებს უნდა ჰქონდეთ კანონით მინიჭებული უფლება, გამოწერონ, გასცენ და დანიშნონ ოპიოიდები ადგილობრივი მოთხოვნების შესაბამისად.
2. ანგარიშგება: პერსონალმა ოპიოიდები უნდა გასცეს მხოლოდ სამედიცინო დანიშნულებით, წინააღმდეგ შემთხვევაში უნდა ეკისრებოდეს პასუხისმგებლობა კანონის წინაშე.
3. სათანადო ჩანაწერები: თუ ექიმებს სხვა ჩანაწერების წარმოებაც მოეთხოვებათ (კარგ სამედიცინო პრაქტიკასთან დაკავშირებული ჩანაწერების გარდა), ეს დამატებითი სამუშაო არ უნდა იყოს დიდი მოცულობის და არ უნდა აფერხებდეს სამედიცინო საქმიანობას. საავადმყოფოებს და აფთიაქებს უნდა ჰქონდეს კანონით განსაზღვრული პასუხისმგებლობა ოპიოიდების უსაფრთხო შენახვაზე და მიღებული და გაცემული ოპიოიდების შესახებ ჩანაწერების წარმოებაზე. ჩანაწერები ოპიოიდების თითოეული პარტიის მიღებაზე და გაცემაზე უნდა შეინახონ სულ ცოტა, ორი წლის განმავლობაში.
4. ჩანაწერების გონივრული წარმოების და ანგარიშგების პირობები არ უნდა იყოს იმდენად რთული, რომ უბიძგოს სამედიცინო პერსნალს, არ გამოწეროს ოპიოიდები ან თავი აარიდოს ოპიოიდების სათანადო მარაგის უზრუნველყოფას.
5. რეცეპტები: რეცეპტების მიმართ კანონით არსებული მოთხოვნები განსხვავებულია. თუმცა, ზოგადად, ოპიოიდური აგონისტებით ჩანაცვლებითი თერაპიის რეცეპტში უნდა იყოს შემდეგი ინფორმაცია:
- რეცეპტის გამცემი ექიმის სახელი და გვარი, მისამართი და ტელეფონის ნომერი;
- აფთიაქის დასახელება;
- პაციენტის სახელი, გვარი და მისამართი;
- რეცეპტის გამოწერის თარიღი;
- გასაცემი პრეპარატი (მაგ. მეთადონი ან ბუპრენორფინი);
- გასაცემი დოზა მილიგრამებში (სიტყვიერად და რიცხვობრივად);
- გაცემის სიხშირე (ყოველდღე, დღეში ორჯერ, ყოველ მეორე დღეს, კვირაში სამჯერ);
- რეცეპტით წამლის გაცემის დაწყების და დასრულების თარიღები;
- საჭიროა თუ არა დოზებზე ზედამხედველობა თუ შეიძლება სახლში გატანება;
6. ხელმისაწვდომობა პაციენტისთვის: ოპიოიდები რაც შეიძლება ბევრი დამოკიდებული პაციენტისთვის ადვილად ხელმისაწვდომი უნდა იყოს ადგილმდებარების თვალსაზრისით;
7. სამედიცინო გადაწყვეტილებები: გადწყვეტილებები იმის შესახებ, თუ რა ტიპის პრეპარატი უნდა გამოვიყენოთ, რამდენი უნდა გამოვწეროთ რეცეპტში და რა ხანგრძლივობის უნდა იყოს მკურნალობა, უნდა მიიღოს პროფესიონალმა პაციენტის ინდივიდუალური საჭიროებების მიხედვით.
 |
17 დანართი 8. პრიორიტეტები კვლევისთვის |
▲back to top |
ამ დანართში აღწერილია სახელმძღვანელოს მომზადებისას მკურნალობასთან დაკავშირებული მონაცემების მიმოხილვის შედეგად აღმოჩენილი სისუსტეები და ნაკლოვანებები.
A8.1 მტკიცებულებების ნაკლებობა
ოპიოიდური აგონისტებით მხარდაჭერის, დეტოქსიკაციისა და ოპიოიდური ანტაგონისტების გამოყენების მეთოდების შედარება ნალტრექსონით მკურნალობა ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობასთან შედარებული იყო რამდენიმე კვლევავაში. მხოლოდ ერთ რანდომიზებული კვლევაში მოხდა მეთადონის ან ბუპრენორფინის ნალტრექსონთან შედარება ბუპრენორფინის ინტრავენურ მომხმარებლებში [142]. არც ერთი კვლევა არ მოიძებნა, სადაც შედარებული იქნებოდა გახანგრძლივებული მოქმედების ნალტრექსონი და ოპიოიდური აგონისტებით მკურნალობის მეთოდები.
არც ერთ კვლევას არ შეუფასებია ერთზე მეტი სამკურნალო პრეპარატის არსებობით გამოწვეული სარგებელი მოსახლეობისთვის (მაგ., ბუპრენორფინი და მეთადონი, ან ოპიოიდური ანტაგონისტები და ოპიოიდური აგონისტები).
არცერთი რანდომიზებული კვლევა არ ჩატარებულა სპეციფიკურ პოპულაციებში (მაგ., ახალგაზრდები, ადამიანები დამოკიდებულების ხანმოკლე ანამნეზით, ადამიანები, რომლებიც არ იყენებენ საინექციო პრეპარატებს და ორსულები), სადაც ოპიოიდურ დეტოქსიკაციაზე დამყარებული მეთოდები შედარებული იქნებოდა ოპიოიდური აგონისტებით მხარდამჭერ თერაპიაზე დამყარებულ მეთოდებთან. მართალია, არსებული მონაცემები მტკიცედ უჭერს მხარს ოპიოიდური აგონისტების გამოყენებას, ბევრ შემთხვევაში ოპიოიდური დეტოქსიკაცია ყველაზე ხშირად მოთხოვნილ მკურნალობად რჩება.
მკურნალობის გავლენა აივ ინფექციის გადაცემაზე
სასარგებლო იქნებოდა დაკვირვების პრინციპით კარგად ჩატარებული კვლევები ფარმაკოლოგიური მკურნალობის მნიშვნელობის შესახებ აივ ინფექციის გადაცემისათვის, რადგან რანდომიზებული კვლევების უმრავლესობაში არ იყო შეგროვილი ინფორმაცია აივ-ის რისკის და აივ-ის გადაცემის შესახებ. კერძოდ, საჭიროა მეტი მონაცემი ბუპრენორფინით მკურნალობის აივ ინფექციის გადაცემაზე გავლენის შესახებ, რადგან ეს მკურნალობა ბევრ სქემაში ზედამხედველობის გარეშე ტარდება.
ოპტიმალური დოზები
მეთადონის ოპტიმალურ დოზებთან დაკავშირებით კვლევები საკმარისია რეკომენდაციების გასაცემად, თუმცა, იმავეს ვერ ვიტყვით ბუპრენორფინზე. ასევე, საჭიროა კვლევები მეთადონის და ბუპრენორფინის ოპტიმალური დოზების შესახებ არასაინექციო ნარკოტიკების მომხმარებელთა შორის (მაგ. ოპიუმის მწეველები). დოზაზე ზედამხედველობა
აგონისტებით ჩანაცვლებითი მკურნალობის დროს
საკვირველია, მაგრამ როგორც მეთადონის, ისე ბუპრენორფინისთვის ცოტაა კვლევები იმის შესახებ, თუ რა გავლენა აქვს მკურნალობის შედეგზე დოზის ზედამხედველობით მიცემას. ეს განსაკუთრებით მნიშვნელოვანი საკითხია, თუ გავითვალისწინებთ, რომ რამდენიმე ქვეყანაში ბუპრენორფინით მკურნალობა ზედამხედველობის გარეშე ხდება.
ანტაგონისტებით მკურნალობის სხვადასხვა სქემა
არსებობს შეუსაბამობა, კერძოდ, განვითარებულ ქვეყნებში პერორალური ნალტრექსონით მკურნალობა მოკრძალებულ შედეგებს იძლევა, განვითარებად ქვეყნებში კი ექიმები ნალტრექსონს ეფექტიან პრეპარატად მიიჩნევენ. საჭიროა ოპიოიდური ანტაგონისტების დამატებითი კვლევა განვითარებად ქვეყნებში.
დამოკიდებულება დანიშნულ ოპიოიდებზე
ბევრ ქვეყანაში, დანიშნულ ოპიოიდებზე დამოკიდებული ადამიანების რაოდენობა უკვე აჭარბებს უკანონო ოპიოიდებზე დამოკიდებულთა რაოდენობას. საჭიროა მეტი კვლევა ამ პოპულაციაში ოპიოიდური დეტოქსიკაციის და აგონისტებით მხარდამჭერი მკურნალობის შესახებ, ზედამხედველობის საჭირო დონის უზრუნველყოფით.
მოზარდები
სამწუხაროა შედარებით მცირე რაოდენობით კვლევების არსებობა ახალგაზრდებში და ოპიოიდური დამოკიდებულების ხანმოკლე ანამნეზის მქონე ადამიანებში, რადგან ამ პოპულაციას ცვლილებების ყველაზე მეტი უნარი აქვს. მეტი კვლევებია საჭირო ფსიქო-სოციალური დახმარების (მათ შორის, ოჯახურ დახმარებაზე დამყარებული მეთოდები) და მათი გავლენის შესახებ ოპიოიდური აგონისტებით მკურნალობასა და აღკვეთის მდგომარეობის მკურნალობაზე, ასევე ანტაგონისტებით მკურნალობაზე.
ორსულობა და ძუძუთი კვება
სასურველი იქნებოდა მეტი კვლევა ორსულ და მეძუძურ ქალებში ბუპრენორფინის და ნალოქსონის უსაფრთხოების დასადგენად.
აგონისტებით მხარდამჭერი თერაპიის დაგეგმილი შეწყვეტის შედეგი
აუცილებელია მეტი კვლევა იმის შესახებ, თუ როდის შეიძლება შეწყდეს ოპიოიდების აგონისტებით მკურნალობა რეციდივის მაღალი რისკის გარეშე. ასევე, საჭიროა კვლვები, რომლებშიც შედარებული იქნება აგონისტებით მხარდამჭერი თერაპიის შეწყვეტის მეთოდები.
ფსიქოსოციალური დახმარება
საჭიროა დამატებითი კვლევა სხვადასხვა ფსიქოსოციალური მეთოდის შესახებ, განსაკუთრებით, სოციალური მეთოდების შესახებ, როგორიცაა დასაქმება და ბინით უზრუნველყოფის პროგრამები.
A8.2 მეთოდოლოგიური საკითხები კვლევაში
კვლევის მოცულობა
ბევრი კვლევა ძალიან მცირემასშტაბიანია იმისათვის, რომ ადეკვატური პასუხი გასცეს მასში დასმულ კითხვებს. ამის მიზეზი შეიძლება იყოს ამ პოპულაციაში კლინიკური კვლევების დაფინანსების სირთულე, ასევე ის, რომ ბევრი სამკურნალო ცენტრი პატარა ზომისაა. უმრავლეს საკითხზე საჭიროა უფრო ფართომასშტაბიანი კვლევები. ამასთანავე, ბევრი კვლევა იმეორებს ადრე ჩატარებულ კვლევებს, მიუხედავად იმისა, რომ მონაცემები არასრულია. შესაძლოა, საჭირო იყოს მკურნალობის საერთაშორისო ქსელის არსებობა, რათა მოხდეს დიდი კვლევების კოორდინირება მარტივ შეკითხვებზე პასუხის გასაცემად. ეს არის მეთოდი, რომელიც ბოლო წლებში მედიცინის ბევრ სფეროში გამოიყენება.
კვლევის ხანგრძლივობა
კვლევების უმრავლესობაში დაკვირვების პერიოდი ძალიან ხანმოკლეა, იმის გათვალისწინებით, რომ ოპიოიდური დამოკიდებულება ქრონიკული დაავადებაა.
კვლევის დიზაინი
ამ მიმოხილვაში გათვალისწინებულ რანდომიზებული კვლევების
უმრავლესობაში არ იყო გამოყენებული «მკურნალობის განზრახვის»
ანალიზი, ბევრში ასევე არ იყო მითითებული ინოფორმაცია
დაფარვის შესახებ. რადგან ფსიქოაქტიურ მედიკამენტებზე ჩატარებულ
კვლევებში პაციენტის მხრივ ბრმა მეთოდის გამოყენება რთულია,
უფრო დიდი ყურადღება უნდა მიექცეს ამ მეთოდის გამოყენებას
გამოსავლის ანალიზის და სტატისტიკური ანალიზის დროს.
გამოსავლის მსაზღვრელები
მკურნალობის განზრახვის ანალიზი მოიცავს როგორც „მკურნალობაში ჩართულ“, ისე „მკურნალობაში ჩაურთველ“ პაციენტებს. გამოთვლების უმრავლესობაში მიჩნეულია, რომ პაციენტები, რომლებიც ტოვებენ მკურნალობას, უბრუნდებიან ნარკოტიკების მოხმარების საწყის დონეს. რეალურად, ზოგიერთი ადამიანი სხვა ფორმის მკურნალობას იწყებს, ზოგს საერთოდ აღარ სჭირდება მკურნალობა. მკურნალობის პროგრამაში დარჩენა სხვა გამოსავლის არარსებობისას მნიშვნელოვანი საზომია, მაგრამ მკურნალობის გაგრძელება და მკურნალობის სტატუსი დაკვირვების პერიოდში განხილული უნდა იყოს, როგორც გარკვეული ჩარევის პირობებში ყოფნა და არა როგორც ჯანმრთელობის გამოსავალი.
ამის ნაცვლად კვლევები კონცენტრირებული უნდა იყოს პრეპარატის გამოყენებაზე და მასთან დაკავშირებულ სარისკო ქცევაზე (მაგ., ინექციები, სქესობრივი აქტივობა, რომელმაც შეიძლება დაავადების გავრცელება გამოიწვიოს) და ჯანმრთელობის გამოსავალზე. ჯანმრთელობის გამოსავლები უნდა მოიცავდეს ფსიქოლოგიური ჯანმრთელობის და კეთილდღეობის საზომებს, ფუნქციას ან დისფუნქციას, ცხოვრების ხარისხს, სიკვდილიანობას და, სადაც საჭიროა, სპეციფიკურ დაავადებებს (მაგ. აივ ინფექცია, C ჰეპატიტი, სქესობრივი გზით გადამდები დაავადებები).
იმის გამო, რომ ფარმაკოგენეტიკურ კვლევაში დიდი პროგრესია, სერიოზული მნიშვნელობა უნდა მიენიჭოს კვლევაში მონაწილეთა სისხლის ნიმუშების შენახვას მოგვიანებითი ანალიზისთვის, რა თქმა უნდა, მონაწილეთა თანხმობის საფუძველზე.
კვლევებში გათვალისწინებული უნდა იყოს ნარკოტიკების მოხმარების გავლენა პიროვნების გარდა სხვა ადამიანებზეც (მაგ., ოჯახი, მომვლელები და საზოგადოება). სოციალური ხარჯების შეფასების მონაცემები (მაგ., კრიმინალური აქტივობა, სამედიცინო მომსახურება, მთავრობისგან გამოყოფილი დახმარების მიღება) ბევრ შემთხვევაში არასაკმარისია. ხარჯების ეფექტიანობის და ხარჯი-სარგებლის ანალიზიც შესაძლებელია, თუ განისაზღვრება მკურნალობის ღირებულება.
A8.3 პროგრამების და სისტემების კვლევა
ოპიოიდური დამოკიდებულების მკურნალობის შესახებ ჩატარებული კვლევების უმრავლესობაში ანალიზის ერთეულად აღებულია ინდივიდუალური პაციენტი. მსოფლიოში ოპიოიდური დამოკიდებულების მკურნალობა სხვადასხვაგვარად ტარდება. მკურნალობის პროგრამის და სისტემის მიმართ მეტი ყურადღების გამოჩენამ შეიძლება გააუმჯობესოს მკურნალობის სისტემების ეფექტიანობა. რეკომენდებული საკვლევი თემები მოიცავს მკურნალობის სქემის არჩევას (მაგ., პირველადი ჯანდაცვა), დოზირების მექანიზმებს და ინტეგრაციას სხვა მკურნალობის სისტემებთან (მაგ., აივ-ის მკურნალობის პროგრამები).
საზოგადოებრივი ჯანდაცვის მხრივ ყველაზე დიდი პრიორიტეტია ოპიოიდური დამოკიდებულების მქონე ადამიანების რაოდენობასა და ეფექტიანი მკურნალობის ხელმისაწვდომობის მქონე ადამიანების რაოდენობას შორის სხვაობის შემცირება.
 |
18 დანართი 9. სახელმძღვანელოს შემუშავების შესახებ ტექნიკური ექსპერტების შეხვედრებისთვის მომზადებელი დოკუმენტები |
▲back to top |
ამ დოკუმენტებს შეგიძლიათ გაეცნოთ ჯანმოს ფსიქიკური ჯანმრთელობის და ნივთიერებათა მავნედ მოხმარების დეპარტამენტის ინტერნეტგვერდზე.
ოპიოიდური დამოკიდებულების მკურნალობის შესახებ დაკვირვების პრინციპით ჩატარებული კვლევების სისტემატური მიმოხილვა
ანა მარია ბარგაგლი, მარინა დავოლი, სილვია მინოზი, სიმონა ვეჩი და კარლო ა. პერუჩი
ეპიდემიოლოგიის დეპარტამენტი, ASL, RM E, რომი, იტალია
ოპიოიდური დამოკიდებულების მკურნალობის რესურსების ღირებულება
დან ჩისოლმი, ჯანმო
უკანონო ოპიოიდებზე დამოკიდებულების მკურნალობის ეკონომიკური შეფასება: მონაცემების მიმოხილვა
კრის დორანი
ნარკოტიკებისა და აკლოჰოლის კვლევის ეროვნული ცენტრი
ახალი სამხრეთ უელსის უნივერსიტეტი, ავსტრალია
ოპიუმის მავნედ მოხმარება და მისი მკურნალობა: გლობალური სურათი
რაჯატ რეი, ს. კატიმანი და ჰ.კ. შარმა
წამალდამოკიდებულების მკურნალობის ეროვნული ცენტრი სრულიად ინდოეთის სამედიცინო მეცნიერებათა ინსტიტუტი ნიუ დელი, ინდოეთი
მოზარდებში ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობა: არსებული ლიტერატურის მიმოხილვა
ლიზა ა. მარში, Ph.D.
განვითარების და კვლევის ეროვნული ინსტიტუტები
აშშ
ფსიქოსოციალური დახმარება ოპიოიდური დამოკიდებულების ფარმაკოთერაპიის დროს: ლიტერატურის მიმოხილვა
პროფესორი დ. კოლინ დრამონდი, MBChB, MD, FRCPsych დამოკიდებულების ფსიქიატრიის პროფესორი მის კატრინ პერიმანი, BSc (Hons), MSc მკვლევარი
ნარკომანიის ეროვნული ცენტრი, გაერთიანებული სამეფო
ლიტერატურის მიმოხილვა ორსულობისა და ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის შესახებ (აღკვეთის მდგომარეობის მართვის, აგონისტებით და ანტაგონისტებით მხარდამჭერი თერაპიის და დამატებითი ფარმაკოთერაპიის ჩათვლით)
უნივერსიტეტის პროფესორი გაბრიელე ფიშერი ნინა კოპფი, სტუდენტი
ვენის სამედიცინო უნივერსიტეტი, ავსტრია
ბუპრენორფინის, მეთადონის და ნალტრექსონის უსაფრთხოების სისტემატური მიმოხილვა
ენდი გრეი
თერაპიის და სამედიცინო მენეჯმენტის დეპარტამენტი ნელსონ რ. მანდელას სამედიცინო სკოლა
კვაზულუ-ნატალის უნივერსიტეტი დურბანი, სამხრეთ აფრიკა
ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის ეთიკური გამოყენება
ადრიან კარტერი ქუინსლენდის თავის ტვინის ინსტიტუტი ქუინსლენდის უნივერსიტეტი
უეინ ჰოლი მოსახლეობის ჯანმრთელობის სკოლა; ქუინსლენდის უნივერსიტეტი, ავსტრალია
დოზაზე ზედამხედველობის როლი ოპიოიდური მხარდამჭერი მკურნალობის დროს
ჯეიმს ბელი, MD, FRACP, FSChAM
ნარკოდამოკიდებულების ეროვნული ცენტრი, ლონდონი, გაერთიანებული სამეფო
ჯანმოს სახელმძღვანელოები ოპიოიდური დამოკიდებულების ფსიქოსოციალურ დახმარებასთან კომბინირებული ფარმაკოლოგიური მკურნალობის შესახებ: წინასწარი დოკუმენტი, შექმნილი ექსპერტთა სპეციალურ შეხვედრაზე ჟენევაში, 2005 წ. 1-4 ნოემბერი
ა. უხტენჰაგენი, ტ. ლადევიჩი, ჯ. რემი
საზოგადოებრივი ჯანმრთელობის და წამალდამოკიდებულების კვლევითი ინსტიტუტი, ციურიხის უნივერსიტეტი
წამალდამოკიდებულების და ფსიქიკური ჯანმრთელობის ცენტრი ტორონტო, კანადა
 |
19 დანართი 10. ოპიოიდური აღკვეთის მდგომარეობის სკალები |
▲back to top |
ოპიოიდური აღკვეთის მდგომარეობის ობიექტური სკალა (OOჭშ) |
||
დააკვირდით პაციენტს 5 წუთის განმავლობაში, შემდეგ ჩაწერეთ ქულა ოპიოიდური აღკვეთის ქვემოთ ჩამოთვლილი თითოეული ნიშნისთვის (1-13). შეკრიბეთ ქულები საბოლოო ქულის მისაღებად |
||
თარიღი |
|
|
1 |
მთქნარება |
|
2 |
რინორეა |
|
3 |
„ბატის კანი“ |
|
4 |
ოფლიანობა |
|
5 |
ცრემლდენა |
|
6 |
ტრემორი |
|
7 |
მიდრიაზი |
|
8 |
ციებ-ცხელება |
|
9 |
მოუსვენრობა |
|
10 |
ღებინება |
|
11 |
კუნთების |
|
12 |
სპაზმები |
|
13 |
აგზნებადობა |
|
|
საერთო ქულა |
|
წყარო: Handelsman et al 1987 [325]
ოპიოიდური აღკვეთის მდგომარეობის სუბიექტური სკალა (SOWS) |
||||||
ქვემოთ მოცემულ სვეტში ჩაწერეთ დღევანდელი თარიღი და მოცემული დრო. შემდეგ 0-დან 4-მდე ქულით შეაფასეთ თითოეული სიმპტომი, რომელიც ახლა გაქვთ. სკალა: 0 = საერთოდ არ მაქვს, 1 = მცირედ გამოხატული, 2 = საშუალოდ გამოხატული, 3 = საკმაოდ გამოხატული, 4 = მკვეთრად გამოხატული |
||||||
თარიღი |
|
|
|
|
|
|
დრო |
|
|
|
|
|
|
|
სიმპტომი |
ქულა |
ქულა |
ქულა |
ქულა |
ქულა |
1 |
ვგრძნობ დაძაბულობას |
|
|
|
|
|
2 |
მამთქნარებს |
|
|
|
|
|
3 |
მაქვს ოფლიანობა |
|
|
|
|
|
4 |
თვალები მეცრემლება |
|
|
|
|
|
5 |
სურდო მაქვს |
|
|
|
|
|
6 |
მაქვს „ბატის კანის“ სიმპტომი |
|
|
|
|
|
7 |
მაქვს კანკალი |
|
|
|
|
|
8 |
მაქვს წამოწითლება |
|
|
|
|
|
9 |
მაქვს შემცივნება |
|
|
|
|
|
10 |
მტკივა ძვლები და კუნთები |
|
|
|
|
|
11 |
მაქვს მოუსვენრობა |
|
|
|
|
|
12 |
მაქვს გულისრევა |
|
|
|
|
|
13 |
მაქვს ღებინება |
|
|
|
|
|
14 |
მაქვს კუნთების კრთომა |
|
|
|
|
|
15 |
მუცელში მაქვს სპაზმები |
|
|
|
|
|
16 |
მაქვს აგზნებადობა |
|
|
|
|
|
|
ჯამური ქულა |
|
|
|
|
|
წყარო: Handelsman et al 1987 [325]
ოპიოიდების აღკვეთის მდგომარეობის კლინიკური სკალა (COWS) |
|
თითოეული პუნქტისთვის შემოხაზეთ ნომერი, რომელიც ყველაზე კარგად აღწერს პაციენტის ნიშნებს და სიმპტომებს. შეაფასეთ ის სიმპტომები, რომლებიც ოპიოიდური აღკვეთის მდგომარეობასთან არის დაკავშირებული. მაგ., თუ პულსი აჩქარებულია იმის გამო, რომ კითხვარის შევსებამდე პაციენტი დარბოდა, პულსის აჩქარება არ უნდა დაემატოს ამ სკალას. პაციენტის სახელი:______________________________ თარიღი და დრო: -----/-----/----------: ______________ შეფასების მიზეზი: |
|
პულსი მოსვენების მდგომარეობაში: ..................... დარტყმა/წთ იზომება პაციენტის ერთი წუთის განმავლობაში ჯდომის ან წოლის შემდეგ:
0 პულსი 80, ან ნაკლები |
გასტროინტესტინური სიმპტომები: ბოლო 1/2 სთ-ის განმავლობაში 0 გასტროინტესტინური სიმპტომები არ არის
1 მუცელში სპაზმები 5 დიარეის ან ღებინების მრავლობითი ეპიზოდები |
ოფლიანობა: ბოლო 1/2 სთ-ის განმავლობაში, რომელიც არ არის დაკავშირებული ოთახის ტემპერატურასთან ან პაციენტი აქტივობასთან
0 არ აღინიშნება ციებ-ცხელების არც ერთი სიმპტომი
2 სახეზე წამოწითლება ან გამოხატული სისველე |
ტრემორი:
0 ტრემორი არ არის |
მოუსვენრობა:
0 შეუძლია წყნარად ჯდომა |
მთქნარება:
0 არ არის
2 სამჯერ ან მეტჯერ დამთქნარება შეფასების განმავლობაში |
გუგების ზომა
0 წვრილი ან ოთახის განათების შესაბამისი გუგები |
აგზნებადობა ან გაღიზიანებადობა
0 არ არის |
ძვლის ან სახსრების ტკივილი:
0 არ აღინიშნება
4 პაციენტი ისრისავს სახსრებს ან |
„ბატის კანი“
0 კანი გლუვია |
სურდო ან ცრემლდენა:
0 არ არის |
ჯამური ქულა _______________ ჯამური ქულა 11 პუნქტის ქულების ჯამს წარმოადგენს კითხვარის შემვსების ინიციალები: ---------------------------------- |
ქულები: 5-12 = მსუბუქი; 13-24 = საშუალო; 25-36 = ზომიერად
მძიმე; 36-ზე მეტი = მძიმე აღკვეთის მდგომარეობა
წყარო: Wesson and Ling 2003 [326]

ნეონატალური აბსტინენციის სინდრომის შეფასების სქემა
ნეონატალური აბსტინენციის სინდრომის (NAS) შეფასების მეთოდი
ქვემოთ ჩამოთვლილი (გარდა 1-სა) თითოეული მახასიათებელი შეაფასეთ 1 ქულით.
1. გამკივანი ხმით ტირილი: შეაფასეთ 2 ქულით, თუ ტირილი გამკივანი ხდება ტირილის პიკზე, ხოლო 3 ქულით, თუ ტირილი მუდმივად გამკივანია.
2. ძილი: გაითვალისწინეთ ორ კვებას შორის ძილის მთლიანი პერიოდი
3. ტრემორი: მოცემულია მზარდი სიმძიმის მაჩვენებელი სიმპტომები. ამ ოთხი კატეგორიიდან მხოლოდ ერთი უნდა აირჩეს. არაშემაწუხებელი ძილი ნიშნავს, როცა ბავშვს ძინავს ან წევს მოსვენებულ მდგომარეობაში.
4. კუნთების გაზრდილი ტონუსი: ქულა მიანიჭეთ, თუ ბავშვის ზოგადი კუნთოვანი ტონუსი ნორმის ზედა ზღვარზე მაღალია.
5. ექსკორიაცია: ქულა მიანიჭეთ, თუ კანის ექსკორიაცია აღინიშნება 30 წუთში სამ-ოთხჯერ მეტად.
6. ცხვირის გაწითლება: ქულა მიანიჭეთ, თუ ცხვირის გაწითლება აღინიშნება სასუნთქი გზების სხვა დაავადების არსებობის გარეშე.
7. სუნთქვის სიხშირე: ქულა მიანიჭეთ, თუ სუნთქვის სიხშირე წუთში 60-ზე მეტია და ეს არ არის გამოწვეული სასუნთქი გზების რაიმე დაავადებით.
8. გაძლიერებული წოვა: ქულა მიანიჭეთ, თუ ბავშვი ძუძუს წოვს საშუალოზე უფრო ხშირად.
9. ცუდი კვება: ქულა მიანიჭეთ, თუ ბავშვი ძალიან ნელა ჭამს ან საკვების არაადეკვატურ რაოდენობას იღებს.
10. რეგურგიტაცია: ქულა მიანიჭეთ მხოლოდ იმ შემთხვევაში, თუ ბავშვს რეგურგიტაცია უფრო ხშირად აღენიშნება, ვიდრე, ჩვეულებრივ, ახალშობილებს.
დღენაკლული ახალშობილის შემთხვევაში ძირითადად საჭიროა ძილთან დაკავშირებული სექციების მოდიფიკაცია. მაგ., ბავშვს, რომელსაც სამ საათში ერთხელ სჭირდება კვება, კვებებს შორის მაქსიმუმ, 2.5 სთ ძინავს. 1 ქულა უნდა მიენიჭოს, თუ ორ საათზე ნაკლები ძინავს, ორი ქულა - თუ ერთ საათზე ნაკლები და 3, თუ ბავშვს კვებებს შორის საერთოდ არ ძინავს. ბევრ დღენაკლულ ბავშვს ზონდით კვება სჭირდება. თუ ზონდით კვება დღენაკლულობასთან არის დაკავშირებული, ამ სქემაში ცუდი კვების გამო ქულა არ უნდა მიენიჭოს.
თუ ახალშობილს სამჯერ ჩაუტარდა შეფასება და საშუალოდ რვაზე (8) მაღალი ქულა მიიღეთ, ამ ბავშვს NAS-ზე მკურნალობა სჭირდება.
 |
20 დანართი 11. ზოგიერთი ფსიქოაქტიური ნივთიერების შემაჯამებელი დახასიათება |
▲back to top |
ნივთიერება |
მოქმედების |
ქცევითი ეფექტები |
ტოლერანტობა |
აღკვეთა |
გახანგრძლივებული |
ეთანოლი |
GABA-A |
სედაცია, |
მეტაბოლური |
კანკალი, |
თავის |
საძილე და |
ბენზოდიაზეპინები: |
სედაცია, |
ეფექტების |
აგზნებადობა, |
მეხსიერების დარღვევა |
საძილე და |
ბენზოდიაზეპინები: |
სედაცია,
მოტორული |
ეფექტების |
აგზნებადობა, |
მეხსიერების დარღვევა |
ნიკოტინი |
ნიკოტიკური |
სიფხიზლე, |
ტოლერანტობა ცვლილებებით. |
გაღიზიანებადობა, |
მწეველობის |
ოპიოიდები |
CB1 რეცეპტორების აგონისტები |
რელაქსაცია, |
ტოლერანტობა |
იშვიათია, |
კოგნიტური |
კოკაინი |
მონოამინების |
აგზნებადობის, |
შესაძლოა |
მნიშვნელოვანი |
კოგნიტური |
ამფეტამინები |
დოფამინის |
გაზრდილი |
სწრაფად |
დაღლილობა, მადის |
ძილის |
ექსტაზი |
ბლოკავს |
გაზრდილი |
შეიძლება |
გულისრევა, დარღვევა. |
ნეიროტოქსიურია |
აქროლადი |
სავარაუდოდ, |
თავბრუსხვევა, |
ვითარდება |
გულყრების |
დოფამინის |
ჰალუცინოგენები |
სხვადასხვა: |
პულსის |
ფიზიკური და |
მონაცემები |
მწვავე ან ქრონიკული |
წყარო: ჯანმო 2004 [9].
 |
21 დანართი 12. მედიკამენტების დანიშვნის ინსტრუქციები |
▲back to top |
მეთადონის და ბუპრენორფინის გამოყენებისას სპეციფიკური სიფრთხილეა საჭირო
ინტოქსიკაციის ან სედაციის მდგომარეობაში მყოფი პაციენტები
მეთადონი და ბუპრენორფინი არ უნდა მივცეთ პაციენტებს, რომელთაც ინტოქსიკაციის ან სედაციის ნიშნები აღენიშნებათ სედაციური ზედოზირების რისკის გამო. მეთადონის და ბუპრენორფინის გამოყენების რისკი ოპიოიდებზე დამოკიდებულ პაციენტებში, რომლებიც ხშირად არიან სედაციური საშუალებების, როგორებიცაა ალკოჰოლი და ბენზოდიაზეპინები, ზემოქმედების ქვეშ, შეფასებული უნდა იყოს მკურნალობის სარგებელთან მიმართებით.
ღვიძლის/თირკმლის მძიმე დისფუნქცია
მეთადონის და ბუპრენორფინის მეტაბოლიზმზე და ელიმინაციაზე შეიძლება გავლენა მოახდინოს თირკმლის ან ღვიძლის დისფუნქციამ. ამ შემთხვევაში დოზები და მათი მიცემის სიხშირე შესაბამისად უნდა იყოს დარეგულირებული.
სუნთქვის უკმარისობა
პაციენტებს, რომლებსაც აწუხებთ სუნთქვის უკმარისობა, მეთადონის და ბუპრენორფინის მოხმარების დროს შეიძლება აღენიშნოთ სუნთქვის დარღვევა.
ფსიქოზი
აქტიური ფსიქოზით დაავადებული პაციენტებისათვის ყურადღებით უნდა იქნეს შეფასებული მეთადონის და ბუპრენორფინის მიცემის რისკი და სარგებელი.
მეთადონით ჩანაცვლებითი თერაპია
ინდუქცია
მეთადონის საწყისი დღიური დოზა დამოკიდებული უნდა იყოს ოპიოიდების მიმართ ნეიროადაპტაციის დონეზე. საზოგადოდ, დოზა არ უნდა აღემატებოდეს 20 მგ-ს, გარდა იმ შემთხვევებისა, როცა ოპიოიდების მიმართ დიდია ტოლერანტობა და ამ შემთხვევაშიც კი, დოზა 30 მგ-ზე მეტი არ უნდა იყოს. ოპიოიდების მიმართ დაბალი ან გაურკვეველი დონის ტოლერანტობის მქონე ადამიანებისთვის საწყისი დღიური დოზა უნდა იყოს 10-15 მგ. სიფრთხილეა საჭირო, როცა მეთადონის საწყისი დოზა 20 მგ-ზე მეტია. ოპიოიდებისადმი ტოლერანტობის დონის ყველაზე უკეთ შეფასება შესაძლებელია პაციენტზე დაკვირვებით დოზის მიღებიდან 2-3 საათის განმავლობაში. თუ პაციენტებს მეთადონის დოზის მიღებიდან 2-3 საათის შემდეგ მნიშვნელოვანი ოპიოიდური აღკვეთის სინდრომი განუვითარდათ, მაშინ მათ დამატებით უნდა მიეცეთ 5-10 მგ მეთადონი და, შესაბამისად, გაეზარდოთ მომდევნო დღის დოზა. თუ მეთადონის დოზის მიცემის შემდეგ სედაცია განვითარდა, უნდა შევამციროთ შემდეგი დღის დოზა (და დავაკვირდეთ პაციენტს, სანამ სედაცია არ მოიხსნება; საჭიროების შემთხევაში ვუმკურნალოთ ზედოზირებაზე).
პაციენტს უნდა დავაკვირდეთ ყოველდღე, დოზის მიცემამდე. პაციენტებს, რომლებიც სედაციის ან ინტოქსიკაციის მდგომარეობაში იმყოფებიან, სედაციის მოხსნამდე არ უნდა მივცეთ მეთადონის დამატებითი დოზა.
მეთადონის მიღების დაწყებისას სიფრთხილის გამოჩენაა საჭირო შემდეგ შემთხვევებში: ბევრი სხვადასხვა პრეპარატის გამოყენების რისკი, ფსიქიკური დაავადება, ოპიოიდებისადმი ნეიროადაპტაციის დაბალი დონე (მაგ., ცოტა ხნის წინ ციხეში მოხვედრა) და მნიშვნელოვანი თანმხლები სამედიცინო პრობლემები.
სტაბილიზაცია
მას შემდეგ, რაც პაციენტი იტარებს ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობას ინტოქსიკაციის ან მნიშვნელოვანი აღკვეთის მდგომარეობის გარეშე, მიზანი არის მეთადონის დოზის ტიტრაცია ყველაზე ეფექტიან დოზამდე. მეთადონის დღიური დოზა ყოველ რამდენიმე დღეში 5-10 მგ-ით უნდა გაიზარდოს (საჭიროების შემთხვევაში) ოპიოიდების მიმართ ლტოლვისა და ოპიოიდების უკანონო გამოყენების შესამცირებლად. დოზა არ უნდა გაიზარდოს კვირაში 20 მგ-ზე მეტად.
დოზის ყოველი გაზრდის შემდეგ საჭიროა პაციენტზე დაკვირვება.
მეთადონის საშუალო ეფექტიანი დოზა არის 60-120 მგ.
ბუპრენორფინიდან მეთადონზე გადასვლა
მეთადონი უნდა დაიწყოთ ბუპრენორფინის ბოლო დოზის მიღებიდან 24 საათის შემდეგ. თუ ბუპრენორფინის დღიური დოზა 8 მგ და მეტია, დაიწყეთ დღეში 30 მგ მეთადონით, თუ 4-8 მგ-ია - 20-30 მგ-ით, თუ 4 მგ-ია - 20 მგ-ზე ნაკლები მეთადონით.
მეთადონის გამოტოვებული დოზები
თუ ერთი ან ორი დოზაა გამოტოვებული, პაციენტმა შეიძლება გააგრძელოს მეთადონის იმავე დოზის მიღება.
თუ სამი დოზაა გამოტოვებული, მეთადონის შემდეგი დოზა 25%25-ით უნდა შემცირდეს, რათა გათვალისწინებულ იქნეს ტოლერანტობის შესაძლო შემცირება. თუ დოზა კარგად აიტანება, შეიძლება მანამდე მიღებული დოზის გაგრძელება. თუ ოთხი დოზაა გამოტოვებული, შემდეგი დოზა 50%25-ით უნდა შემცირდეს, რათა გათვალისწინებულ იქნეს ტოლერანტობის შესაძლო დაქვეითება. თუ დოზა კარგად ასატანია, შეიძლება რამდენიმე დღის განმავლობაში მისი თანდათან გაზრდა და მანამდე არსებულ დოზაზე დაბრუნება. თუ ოთხზე მეტი დოზაა გამოტოვებული, დოზის ინდუქცია თავიდან უნდა მოხდეს.
დოზების მიცემის სიხშირე
პაციენტების უმრავლესობას მეთადონი შეიძლება ყოველდღიურად დაენიშნოს. პაციენტების დაახლოებით 30%25-ისათვის მეთადონი არ წარმოქმნის 24 საათიან მდგრად ეფექტებს. ეს ასევე შეიძლება მოხდეს ორსულობის დროს ან მეთადონის იმ მედიკამენტებთან კომბინაციაში, რომლებიც აძლიერებს მის მეტაბოლზმს. ამგვარ შემთხვევებში მეთადონი შეიძლება დაინიშნოს დღეში ორჯერ დოზის ორად გაყოფით. როცა მედიკამენტის დღეში ორჯერ მისაღებად მოსვლა ძალიან რთულია ან მიზანშეწონილი არ არის სახლში მისაღები დოზის მიცემა, უნდა განვიხილოთ ბუპრენორფინზე გადასვლის საკითხი. მეთადონის დოზის გაზრდა რამდენადმე გაახანგრძლივებს მის მოქმედებას (თუმცა, მოქმედების ხანგრძლივობას პირველ რიგში მეტაბოლიზმის სიჩქარე განსაზღვრავს).
დოზის შემცირება და მკურნალობის შეწყვეტა
მეთადონით მკურნალობის შეწყვეტის შესახებ გადაწყვეტილების მიღება მკურნალობის გეგმის ნაწილი უნდა იყოს. არსებული მონაცემებით, შეწყვეტა დაკავშირებულია უკანონო ოპიოიდების მოხმარების განახლების რისკთან. საჭიროა, პაციენტს ვაცნობოთ ამ რისკის შესახებ. კვლევები იმის შესახებ, თუ რა წინასწარი ფაქტორები მიუთითებს აგონისტებით მხარდამჭერი თერაპიის წარმატებით შეწყვეტაზე, არ არის საკმარისი. ეს ფაქტორები შეიძლება იყოს: ნარკოტიკების მოხმარების მოკლე ანამნეზი ოპიოიდების აგონისტებით მკურნალობის დაწყებამდე, სხვა მკურნალობის არარსებობა, მუშაობდა თუ არა პაციენტი ოპიოიდების აგონისტებით მკურნალობამდე, აქვს თუ არა სტაბილური საცხოვრებელი, უკანონო ოპიოიდების მოხმარების შეწყვეტა, სხვა პრეპარატებით (მათ შორის კანაფი) სარგებლობის შეწყვეტა და მკურნალობის დაწყების შემდეგ სოციალური და ფიზიკური გარემოს დადებითისკენ შეცვლა.
ყოველდღიური დოზა 2.5-5 მგ-ით კვირაში შეიძლება იმგვარად შემცირდეს, რომ ამას არ მოჰყვეს აღკვეთის მძიმე სიმპტომები. დოზის შემცირების დროს აუცილებელია ხშირი დაკვირვება და დოზის კლინიკური საჭიროების მიხედვით დარეგულირება.
მეთადონი ოპიოიდური დეტოქსიკაციისთვის
დაიწყეთ 10-20 მგ მეთადონით დღეში დამოკიდებულების სიმძიმის და ოპიოიდებისადმი ტოლერანტობის ხარისხის მიხედვით. მეთა დონის დღიური დოზა 1-2 მგ-ით შეამცირეთ. მეთადონის შეწყვეტიდან ერთი კვირის შემდეგაც პაციენტებს ექნებათ ოპიოიდური აღკვეთის მსუბუქი სიმპტომები.
ბუპრენორფინით ჩანაცვლებითი მკურნალობა
ინდუქცია
მნიშვნელოვანია, რაც შეიძლება სწრაფად მივაღწიოთ ადეკვატურ ჩანაცვლებით დოზას და მოვახდინოთ მისი ტიტრაცია კლინიკური ეფექტიანობის გათვალისწინებით, რათა თავიდან ავიცილოთ აღკვეთის სიმპტომები და შეუსაბამო დოზირება.
ინდუქციამდე უნდა გავითვალისწინოთ გამოყენებული ოპიოიდების ტიპი (გახანგრძლივებული თუ ხანმოკლე მოქმედების), რა დროა გასული ოპიოიდის ბოლო მიღებიდან და ოპიოიდური დამოკიდებულების ხარისხი ან დონე (ანუ ოპიოიდური ტოლერანტობა).
პაციენტები, რომლებიც შავ ბაზარზე ნაყიდ ჰეროინს იყენებენ (ან სხვა ხანმოკლე მოქმედების ოპიოიდებს) მკურნალობის დაწყებისას ბუპრენორფინის პირველი დოზა უნდა მივცეთ ოპიოიდის ბოლო გამოყენებიდან, სულ ცოტა, ექვსი საათის შემდეგ ან აღკვეთის პირველი ნიშნების გამოვლინებისას. რეკომენდებული საწყისი დოზა არის 4 მგ ბუპრენორფინი პირველ დღეს. თუ პაციენტი საჭიროებს, შესაძლებელია კიდევ 4 მგ-ის დამატება.
პაციენტები, რომლებიც იყენებენ მეთადონს ბუპრენორფინით მკურნალობის დაწყებამდე მეთადონის დოზა უნდა შემცირდეს დღეში 30 მგ-მდე. ბუპრენორფინის პირველი დოზის მიღება უნდა მოხდეს მეთადონის ბოლო მიღებიდან 24 საათის შემდეგ. ყველაზე უკეთესია, როდესაც ბუპრენორფინის პირველი 4 მგ-ის მიცემა აღკვეთის პირველი ნიშნების გამოვლენისას ხდება.
ბუპრენორფინის დაწყებისას სიფრთხილის გამოჩენაა საჭირო შემდეგ შემთხვევებში: მრავალი სხვადასხვა პრეპარატის გამოყენების რისკი, ფსიქიატრიული დაავადება, ოპიოიდებისადმი ნეიროადაპტაციის დაბალი დონე (მაგ., ცოტა ხნის წინ ციხეში მოხვედრა) და მძიმე თანმხლები დაავადებები.
სტაბილიზაცია
ბუპრენორფინის დოზა თანდათან უნდა გაიზარდოს პაციენტის კლინიკური ეფექტიანობის გათვალისწინებით. რეკომენდებულია დღეში 8-24 მგ. დღიური დოზა არ უნდა აჭარბებდეს 32 მგ-ს. დოზა რეგულირდება პაციენტის კლინიკური და ფსიქოლოგიური სტატუსის საფუძველზე.
ბუპრენორფინის არაყოველდღიური დოზირება
სტაბილიზაციის გარკვეული პერიოდის შემდეგ დოზირების სიხშირე შეიძლება შემცირდეს და პაციენტს დღეგამოშვებით მივცეთ გაორმაგებული ყოველდღიური დოზა. მაგ. თუ სტაბილური პაციენტი დღეში იღებს 8 მგ-ს, შეიძლება დღეგამოშვებით 16 მგ მიეცეს, ანუ იგი ერთი დღე წამლის გარეშე იქნება. თუმცა, ნებისმიერ ერთ დღეს მიღებული დოზა არ უნდა აღემატებოდეს 32 მგ-ს.
ზოგიერთი პაციენტისთვის, სტაბილიზაციის დამაკმაყოფილებელი პერიოდის მიღწევის შემდეგ, დოზის მიცემის სიხშირე შეიძლება შევამციროთ კვირაში სამ მიღებამდე (მაგ., ორშაბათს, ოთხშაბათს და პარასკევს). ორშაბათს და ოთხშაბათს მიცემული დოზა უნდა იყოს გაორმაგებული დღიური დოზა, ხოლო პარასკევს მიცემული დოზა დღიურ დოზას სამჯერ უნდა აღემატებოდეს. დანარჩენ დღეებში პაციენტი წამალს არ მიიღებს. ნებისმიერ ერთ დღეს მიღებული დოზა არ უნდა აღემატებოდეს 32 მგ-ს.
მეთადონზე გადასვლა
მეთადონი დაიწყეთ ბუპრენორფინის ბოლო დოზიდან 24 საათის შემდეგ. თუ ბუპრენორფინის დღიური დოზა 8 მგ და მეტია, დაიწყეთ დღეში 30 მგ მეთადონით; თუ 4-8 მგ-ია, დღეში 20-30 მგ-ით, ხოლო თუ ბუპრენორფინის დოზა დღეში 4 მგ-ზე დაბალია, 20 მგ-ზე ნაკლები მეთადონით.
დოზის შემცირება და მკურნალობის შეწყვეტა
ბუპრენორფინით მკურნალობის შეწყვეტის შესახებ გადაწყვეტილების მიღება მკურნალობის გეგმის ნაწილი უნდა იყოს. არსებული მონაცემებით, შეწყვეტა დაკავშირებულია უკანონო ოპიოიდების მოხმარების განახლების რისკთან. პაციენტმა აუცილებლად უნდა იცოდეს ამ რისკის შესახებ. კვლევები იმაზე, თუ წინასწარგანწყობის რა ფაქტორები მიუთითებს აგონისტებით ჩანაცვლებითი თერაპიის წარმატებით შეწყვეტაზე, არ არის საკმარისი. ეს ფაქტორები შეიძლება იყოს: ნარკოტიკების მოხმარების მოკლე ანამნეზი ოპიოიდების აგონისტებით მკურნალობის დაწყებამდე, სხვა მკურნალობის არარსებობა, მუშაობდა თუ არა პაციენტი ოპიოიდების აგონისტებით მკურნალობამდე, აქვს თუ არა სტაბილური საცხოვრებელი, უკანონო ოპიოიდების მოხმარების შეწყვეტა, სხვა პრეპარატებით (მათ შორის კანაფი) სარგებლობის შეწყვეტა და მკურნალობის დაწყების შემდეგ სოციალური და ფიზიკური გარემოს დადებითისკენ შეცვლა.
ბუპრენორფინის ყოველდღიური დოზა შეიძლება კვირაში 4-8 მგით იმგვარად შემცირდეს, რომ ამას არ მოჰყვეს აღკვეთის მძიმე სიმპტომები. დოზის შემცირების დროს აუცილებელია ხშირი დაკვირვება და დოზის კლინიკური საჭიროების მიხედვით დარეგულირება.
ბუპრენორფინი ოპიოიდური დეტოქსიკაციისთვის
ბუპრენორფინის გამოყენებით ოპიოიდური დეტოქსიკაციისთვის სხვადასხვა სქემები არსებობს. ერთ-ერთი სქემა არის შემდეგი:
1-ლი დღე 6 მგ
მე-2 დღე 10 მგ +/- 2 მგ
მე-3 დღე 10 მგ +/- 2 მგ
მე-4 დღე 8 მგ +/- 2 მგ
მე-5 დღე 4 მგ
ალფა 2 ადრენერგული აგონისტები ოპიოიდური დეტოქსიკაციისთვის
ალფა 2 ადრენერგულ აგონისტებს შეუძლია მნიშვნელოვანი ჰიპოტენზიის და ბრადიკარდიის გამოწვევა. ამიტომ, ეს მედიკამენტები ოპიოიდური აღკვეთის მდგომარეობის სამკურნალოდ არ უნდა შევთავაზოთ ხანდაზმულ პაციენტებს და პაციენტებს კორონარული უკმარისობით, გულის იშემიური დაავადებით, ბრადიკარდიით, ცერებროვასკულური დაავადებით, ასევე ორსულებს და მეძუძურ ქალებს. კლონიდინის გამოყენებისას რეკომენდებულია პულსის და წნევის კონტროლი და კლონიდინის მიცემაზე უარის თქმა ან დოზის შემცირება, თუ პაციენტს ორთოსტატიკური ჰიპოტენზიის ნიშნები აქვს (მაგ., თავბრუსხვევა ფეხზე დგომისას), ან თუ პულსი და წნევა ძალიან დაქვეითდა (პულსი 50-ზე ნაკლები არტერიული წნევა 90/60 mm Hg).
კლონიდინი
ოპიოიდური აღკვეთის მდგომარეობის მკურნალობისას კლონიდინი, ჩვეულებრივ, ინიშნება დოზით 100-300 მკგ სამჯერ ან ოთხჯერ დღეში. მაქსიმალური დოზა არის 10-17 მკგ/კგ/დღეში, რაც პირველი ორი დღის შემდეგ მცირდება და მე-4-5 დღეს წყდება. როგორც საავადმყოფოს, ისე სახლის პირობებში საწყისი დოზა უნდა იყოს 1-2 მკგ/კგ, შემდეგი დოზების დარეგულირება კი პაციენტის მდგომარების გათვალისწინებით ხდება.
ამბულატორიულ პირობებში, როცა არტერიულ წნევაზე მონიტორინგი არ არის, საჭიროა უფრო დაბალი დოზების გამოყენება. მაქსიალური დღიური დოზა შეიძლება იყოს 450-900 მკგ პაციენტის წონის და ოპიოიდური აღკვეთის მდგომარეობის სიმძიმის გათვალისწინებით.
ლოფექსიდინი
საწყისი დოზა არის 0.4-0.6 მგ ორჯერ დღეში, რაც საჭიროებისამებრ იზრდება და შეიძლება დღეში მაქსიმუმ 2.4 მგ-ს მიაღწიოს 2-4 მიღებაზე გაყოფით. მკურნალობა უნდა გაგრძელდეს 7-10 დღე, რასაც მოჰყვება თანდათან მოხსნა (2-4 დღეში).
გუანფაცინი
საწყისი დღიური დოზა უნდა იყოს 0,25-0.5 მგ, საჭიროების მიხედვით დღეში 1-2 მგ-მდე ზრდით (1-4 მიღებად გაყოფილი) 3-5 დღის განმავლობაში. შემდეგ დოზა იკლებს (2-3 დღის განმავლობაში).
ოპიოიდური აღკვეთის მდგომარეობის სხვა სახის მკურნალობა
ოპიოიდური აღკვეთის მდგომარეობის სამკურნალოდ ალფა 2 აგონისტებთან ერთად ბევრი სხვა მედიკამეტიც გამოიყენება (მაგ., ბენზოდიაზეპინები აგზნებისა და უძილობისთვის, ღებინების საწინააღმდეგო პრეპარატები გულისრევა-ღებინებისთვის, პარაცეტამოლი და არასტეროიდული ანთების საწინააღმდეგო პრეპარატები კუნთების ტკივილისთვის). ამ მედიკამენტების გამოყენების შესახებ დეტალური მითითებები სცილდება ამ სახელმძღვანელოს ფუნქციებს.
პაციენტებს, რომელთაც აღენიშნებათ დიარეა, ღებინება და ჭარბი ოფლიანობა, შეიძლება განუვითარდეთ მძიმე დეჰიდრატაცია და საჭირო გახდეს სითხეებით დატვირთვა.
ნალტრექსონით მკურნალობა
ნალტრექსონით მკურნალობა იწყება დეტოქსიკაციის მომდევნო პერიოდში ოპიოიდების მიღების შეწყვეტიდან 7 (ხანმოკლე მოქმედების ოპიოიდების შემთხვევაში) ან 10 დღის შემდეგ (მეთადონის შემთხვევაში). ოპიოიდების შეწყვეტა უნდა შემოწმდეს (თუ ეჭვი გაჩნდა), სულ ცოტა, შარდის უარყოფითი პასუხით და ნალოქსონით დატვირთვის ტესტით. სტანდარტული ჩანაცვლებითი დოზა არის დღეში 50 მგ პერორალურად. თუ პაციენტებს აქვთ გასტროინტესტინური გვერდითი მოვლენები, მდგომარეობის შემსუბუქება შეიძლება ნალტრექსონის დოზის 25 მგ-მდე შემცირებით რამდენიმე დღის განმავლობაში.
მხარდაჭერის ფაზა
თუ პაციენტმა ჰეროინი ნალტრექსონის მიღების დღეს გამოიყენა, შეუძლია ნალტრექსონის მიღება მეორე დღეს გააგრძელოს.
თუ პაციენტმა ჩააგდო ნალტრექსონი და ჰეროინი ან სხვა ოპიოიდი გამოიყენა, მან: ან რაც შეიძლება სწრაფად უნდა განაახლოს ნალტრექსონის მიღება, ან მოიცადოს 7 დღე და თავიდან დაიწყოს ნალტრექსონის დოზის ინდუქცია. თუ ნალტრექსონს პაციენტი მაშინვე მიიღებს, მას აღკვეთის მსუბუქი სინდრომი ექნება.
აღკვეთის სინდრომის სიმძიმის თავიდან ასაცილებლად, პაციენტებს შეიძლება დაენიშნოთ ნალოქსონით დატვირთვა. აღკვეთის აღმოცენებული სინდრომის მკურნალობისთვის შეიძლება გამოვიყენოთ ალფა 2 ადრენერგული აგონისტები.
თუ პაციენტი ნალტრექსონს ორი ან მეტი დღის განმავლობაში არ მიიღებს და ჰეროინს ან სხვა ოპიოიდს გამოიყენებს, ნალტრექსონის მიღების განახლების შემდეგ შეიძლება აღკვეთის მძიმე მდგომარეობა განუვითარდეს. ამდენად, პაციენტს უნდა ვურჩიოთ, 7 დღე მოიცადოს ან დაიწყოს ოპიოიდების აგონისტებით მხარდამჭერი მკურნალობა.
მკურნალობის ოპტიმალური ხანგრძლივობის შესახებ მონაცემები არ არის. რეკომენდებულია, რომ ეს განისაზღვროს ინდივიდუალურად, სპეციფიკური კლინიკური სიტუაციის მიხედვით.
ნალტრექსონის შეწყვეტას არ მოჰყვება მოხსნის სინდრომი. ნალტრექსონიდან ოპიოიდური აგონისტებით მხარდამჭერ მკურნალობაზე გადასვლა დიდი სიფრთხილით უნდა მოხდეს, რადგან ამ დროს ოპიოიდების მიმართ ტოლერანტობა ძალიან დაბალია.
 |
22 დანართი 13. ლექსიკონი |
▲back to top |
აბსტინენცია
ნარკოტიკის გამოყენებისგან თავის შეკავება. ასევე, აბსტინენციის მდგომარეობაში მყოფად ითვლება პიროვნება, რომელიც რეცეპტით გამოწერილ მეთადონს იღებს, მაგრამ არ იღებს უკანონო ოპიოიდებს. ტერმინი აბსტინენცია არ უნდა აგვერიოს ტერმინში „აბსტინენციის სინდრომი“, რაც აღკვეთის სინდრომს აღნიშნავს.
აგონისტებით მხარდამჭერი თერაპია, ოპიოიდები
წამალდამოკიდებულების მკურნალობა ჩანაცვლებითი პრეპარატით, რომლის მიმართაც პაციენტს აქვს ჯვარედინი დამოკიდებულება და ჯვარედინი ტოლერანტობა. აგონისტებით მხარდამჭერი მკურნალობის მაგალითებია: მეთადონის ან ბუპრენორფინის გამოყენება ჰეროინზე დამოკიდებულების დროს და ნიკოტინის საღეჭი რეზინის გამოყენება თამბაქოს წევის ჩასანაცვლებლად. აგონისტებით მხარდამჭერი თერაპიის მიზანია გარკვეული ნივთიერების (განსაკუთრებით, თუ უკანონოა) გამოყენების შეწყვეტა ან შემცირება; ნარკოტიკების მოხმარების გარკვეული მეთოდის ზიანის ან ამით გამოწვეული ჯანმრთელობის რისკების (მაგ., ერთი და იმავე ნემსის გამოყენებასთან დაკავშირებული დაავადებების რისკი) და წამალდამოკიდებულების სოციალური შედეგების შემცირება. აგონისტებით მხარდამჭერი თერაპია შეიძლება გაგრძელდეს რამდენიმე თვიდან 20 წელზე მეტი ხნის განმავლობაში, რასაც ხშირად თან ახლავს სხვა ტიპის მკურნალობაც (ფსიქოსოციალური მკურნალობა). ხშირად იგი განსხვავდება კლებადი დოზებით მკურნალობისგან (იხ. ოპიოიდური აღკვეთის სინდრომი).
სისხლით გადამდები დაავადებები
დაავადებები, როგორებიცაა აივ და B და C ჰეპატიტები, რომლებიც სისხლით გადადის (მაგ. ერთი და იმავე ნემსის გამოყენებით).
კონვენცია ფსიქოტროპული ნივთიერებების შესახებ (1971)
კონვენცია ფსიქოტროპული ნივთიერებების შესახებ (1971) არის წამლებზე კონტროლის მეორე საერთაშორისო შეთანხმება, რომელიც ავსებს ნარკოტიკული პრეპარატების პირველ კონვენციას (1961). მისი მიზანია (როგორც ამ კონვენციითაა განსაზღვრული) ფსიქოტროპული ნივთიერებების კონტროლი და მათი მავნედ მოხმარების თავიდან აცილება. კონვენციაში მოცემულია მხარეთა პასუხისმგებლობები. ნარკოტიკების კონტროლის საერთაშორისო საბჭო (INCB) (რომელიც ნარკოტიკული პრეპარატების კომისიის (CND) საშუალებით თავის ანგარიშებს უგზავნის ეკონომიკურ და სოციალურ საბჭოს (ECOSOC)), პასუხისმგებელია, ზედამხედველობა გაუწიოს ქვეყნების მთავრობების მიერ 1971 წლის კონვენციის შესრულებას: ერთი მხრივ, უზრუნველყოფს, რომ ფსიქოტროპული ნივთიერებები ხელმისაწვდომი იყოს სამედიცინო და სამეცნიერო მიზნებისთვის, ხოლო, მეორე მხრივ, რომ კანონიერი წყაროებიდან პრეპარატები არ მოხვდეს უკანონო მიმოქცევაში. ბუპრენორფინი მოცემულია კონვენციაში ფსიქოტროპული ნივთიერებების შესახებ.
დამოკიდებულება
ზოგადი ტერმინი, რომელიც აღნიშნავს რაიმეზე ან ვინმეზე დამოკიდებულებას ფუნქციონირების ან გადარჩენის მიზნით. ოპიოიდებთან მიმართებით გულისხმობს პრეპარატის განმეორებითი დოზების მიღების საჭიროებას კარგი თვითშეგრძნებისთვის ან ცუდად ყოფნის თავიდან ასაცილებლად.
1964 წელს ჯანმრთელობის მსოფლიო ორგანიზაციის (ჯანმო) ექსპერტთა კომიტეტმა შემოიტანა ტერმინი „დამოკიდებულება“ ტერმინების - ნარკომანია და ჰაბიტუაცია - შესაცვლელად. ტერმინი ზოგადად შეიძლება გამოვიყენოთ ნებისმიერ ფსიქოაქტიურ ნივთიერებაზე დამოკიდებულების (მაგ., პრეპარატზე დამოკიდებულება, ქიმიური დამოკიდებულება, ნივთიერებაზე დამოკიდებულება) ან კონკრეტულ მედიკამენტზე ან მედიკამენტების ჯგუფზე დამოკიდებულების აღსანიშნავად (მაგ., ოპიოიდური დამოკიდებულება). მართალია, ICD-10-ს დამოკიდებულების სპეციფიკური განმარტება აქვს, რომელიც წამლების კლასების მიხედვით არის მოცემული, მაგრამ დამოკიდებულების სიმპტომები თითოეული სპეციფიკური პრეპარატისთვის შეიძლება სხვადასხვა იყოს.
დამოკიდებულება ხშირად ეხება პრეპარატზე დამოკიდებულების როგორც ფიზიკურ, ისე ფსიქოლოგიურ ელემენტს. უფრო კონკრეტულად, ფსიქოლოგიური ან ფსიქიკური დამოკიდებულება გულისხმობს პრეპარატების გამოყენებაზე კონტროლის უნარის დარღვევას (იგულისხმება დაუოკებელი ლტოლვა ნარკოტიკის მოხმარებისკენ), მაშინ, როცა ფიზიოლოგიური ან ფიზიკური დამოკიდებულება გულისხმობს ტოლერანტობას და აღკვეთის მდგომარეობის სიმპტომებს (იხ. ნეიროადაპტაცია). თუმცა, ბიოლოგიურ დისკუსიაში დამოკიდებულება ხშირად გამოიყენება მხოლოდ ფიზიკური დამოკიდებულების აღსანიშნავად.
ტერმინი დამოკიდებულება ან ფიზიკური დამოკიდებულება ასევე ხშირად გამოიყენება უფრო ვიწრო მნიშვნელობით ფსიქოფარმაკოლოგიურ კონტექსტში, რაც გულისხმობს აღკვეთის სიმპტომების განვითარებას პრეპარატის შეწყვეტის შემდეგ.
დეტოქსიკაცია
პროცესი, რომლის დროსაც პიროვნება გამოდის ფსიქოაქტიური ნივთიერების ზემოქმედებიდან. როდესაც ეს კლინიკურ პროცედურას ეხება, დეტოქსიკაცია უსაფრთხო და ეფექტიან პირობებში განხორციელებულ აღკვეთის პროცესს გულისხმობს აღკვეთის მდგომარეობის სიმპტომების მინიმუმამდე შემცირებით. დაწესებულება, სადაც ეს კეთდება, შეიძლება მოიხსენიონ როგორც დეტოქსიკაციის ცენტრი ანუ „დეტოქსცენტრი“.
ზიანის შემცირება
ალკოჰოლის და სხვა ნივთიერებების კონტექსტში ზიანის შემცირებაში (ან ზიანის მინიმიზაცია) მოიაზრება პროგრამები, რომლებიც პირდაპირ კონცენტრირებულია ალკოჰოლის ან ნარკოტიკების გამოყენებით გამოწვეული ზიანის შემცირებაზე. ტერმინი განსაკუთრებით იმ სისტემებს და პროგრამებს გულისხმობს, რომლებიც ზიანს ამცირებს, მაგრამ ყველა შემთხვევაში არ გულისხმობს ნარკოტიკის მოხმარების შეწყვეტას; ამის მაგალითია ნემსის და შპრიცის გაცვლა, როგორც ერთი და იმავე ნემსით სარგებლობისსაწინააღმდეგო ზომა ჰეროინის მომხმარებლებში; თვითგაბერვადი ბალიშები ავტომობილებში ავარიის დროს დაზიანების შესამცირებლად, განსაკუთრებით, ნასვამ მდგომარეობაში მანქანის მართვისას. ზიანის შემცირების სტრატეგიები მოქმედებათა უფრო ფართო სპექტრს მოიცავს, ვიდრე უბრალოდ, მოწოდების და მოთხოვნის შემცირებას.
ოპიოიდების საზიანო მოხმარება
ფსიქოაქტიური ნივთიერების მოხმარება, რაც აზიანებს ჯანმრთელობას (ICD-10, კოდი F11.1). დაზიანება შეიძლება იყოს ფიზიკური (მაგ., ჰეპატიტის საინექციო ფსიქოაქტიური ნივთიერებების გამოყენების შედეგად) ან ფსიქიკური. მავნედ მოხმარება ხშირად, მაგრამ არა ყოველთვის, იწვევს უარყოფით სოციალურ შედეგებს; თუმცა, მხოლოდ სოციალური პრობლემების არსებობა არ არის საკმარისი საზიანო მოხმარების დიაგნოზის დასასმელად.
ტერმინი შემოტანილ იქნა ICD-10-ის მიერ და როგორც დიაგნოსტიკური ტერმინი შეცვალა „მოხმარება დამოკიდებულების გარეშე“.
ნარკოტიკული პრეპარატი
ნარკოტიკული პრეპარატი არის ბუნებრივი ან სინთეზური ნივთიერება, რომელიც შეტანილია ნარკოტიკული პრეპარატების პირველი კონვენციის (1961) I და II ცხრილში (იხ. ქვემოთ). მეთადონი ნარკოტიკული პრეპარატია.
ნეიროადაპტაცია
ცვლილებები ნეირონებში, დაკავშირებული ტოლერანტობასთან და აღკვეთის სინდრომის გამოვლინებასთან. შესაძლებელია, ადამიანს ჰქონდეს ნეიროადაპტაცია დამოკიდებულების კოგნიტური ან ქცევითი გამოვლინებების გარეშე. მაგალითად, ქირურგიულ პაციენტებს, რომელთაც ეძლეოდათ ოპიოიდური ნივთიერებები ტკივილის შესამცირებლად, ზოგჯერ შეიძლება ჰქონდეთ აღკვეთის სიმპტომები, მაგრამ ვერ ამოიცნონ ისინი ან არ ჰქონდეთ ნარკოტიკების მიღების გაგრძელების სურვილი.
ოპიატი
ოპიუმის ყაყაჩოდან მიღებული ალკალოიდების ერთ-ერთი ჯგუფი (Papaver somniferum), რომელსაც შეუძლია ანალგეზიის, ეიფორიის და, მაღალი დოზებით, სტუპორის, კომის და სუნთქვის დათრგუნვის გამოწვევა. ეს ტერმინი არ მოიცავს სინთეზურ ოპიოიდებს.
ოპიოიდი
ტერმინი, რომელიც მოიცავს ყაყაჩოსგან (Papaver somniferum) მიღებულ ალკალოიდებს, მათ სინთეზურ ანალოგებს და ორგანიზმში სინთეზირებულ ნაერთებს. ყველა ეს ნივთიერება მოქმედებს თავის ტვინში არსებულ ერთი და იმავე სპეციფიკურ რეცეპტორზე, აქვს უნარი, შეამსუბუქოს ტკივილი და წარმოქმნას კარგად ყოფნის (ეიფორია) შეგრძნება. ოპიუმის ალკალოიდები და მათი სინთეზური ანალოგები მაღალი დოზებით ასევე იწვევს სტუპორს, კომას და სუნთქვის დათრგუნვას.
ოპიუმის ალკალოიდები და მათი სინთეზური დერივატები მოიცავს მორფინს, დიაცეტილმორფინს (დიამორფინი, ჰეროინი), ჰიდრომორფინს, კოდეინს და ოქსიკოდონს. სინთეზური ოპიოიდები მოიცავს ლევორფანოლს, პროპოქსიფენს, ფენტანილს, მეთადონს, პეტიდინს (მეპერიდინი) და აგონისტ-ანტაგონისტ პენტაზოცინს. ენდოგენურად არსებული ნაერთები ოპიოიდური მოქმედებით მოიცავს ენდორფინებს და ენკეფალინებს.
ყველაზე ხშირად გამოყენებული ოპიოიდები (როგორებიცაა: მორფინი, ჰეროინი, ჰიდრამორფინი, მეთადონი და პეტიდინი) უპირატესად უკავშირდება μ-რეცეპტორებს; ისინი იწვევს ანალგეზიას, გუნება-განწყობის ცვლილებებს (მაგ., ეიფორია, რომელიც შეიძლება შეიცვალოს აპათიით ან დისფორიით), სუნთქვის დათრგუნვას, ძილიანობას, ფსიქომოტორულ ჩამორჩენას, გაურკვეველ მეტყველებას და კონცენტრაციის, მეხსიერების და აზროვნების დარღვევას.
ოპიოიდების მოხმარების ფიზიკური შედეგები (ყველაზე ხშირად გამოწვეული ინტრავენური შეყვანით) მოიცავს B ჰეპატიტს, C ჰეპატიტს, აივ-ს, სეპტიცემიას, ენდოკარდიტს (გულის შიგა გარსის ანთება), პნევმონიას და ფილტვის აბსცესს, თრომბოფლებიტს (სისხლის კოლტებით გამოწვეული ვენის ანთება) და რაბდომიოლიზს (კუნთების ბოჭკოების დაშლა). ხშირია ფსიქოსოციალური და სოციალური უარყოფითი შედეგები, რაც ოპიოიდების არასამედიცინო დანიშნულებით გამოყენების უკანონო ბუნებას ასახავს.
ოპიოიდი ენდოგენური
თავის ტვინის ბუნებრივი ნეიროპეპტიდები, რაც, სულ ცოტა, ორ დიდ ჯგუფს მოიცავს - ენკეფალინები და ენდორფინები. ორივეს შეუძლია იმოქმედოს ოპიოიდების შეკავშირების ადგილებზე (რეცეპტორებზე) და, ამდენად, მოახდინოს ტკივილის აღქმის მოდულაცია. ენდორფინები ასევე ახდენს განწყობის და სტრესულ სტიმულებზე რეაქციის მოდულაციას (იხ. ოპიოიდი).
ოპიოიდური ინტოქსიკაცია
მდგომარეობა, რომელიც ვითარდება ოპიოიდების შეყვანის შემდეგ და იწვევს ცნობიერების, კოგნიტური ფუნქციის, აღქმის, განსჯის, აფექტის, ქცევის და სხვა ფსიქოფიზიოლოგიური ფუნქციების და რეაქციების დარღვევას. ეს დარღვევები დაკავშირებულია ოპიოიდების მწვავე ფარმაკოლოგიურ ეფექტებთან და დასწავლილ პასუხებთან. დროთა განმავლობაში ეს დარღვევები იხსნება და ხდება სრული აღდგენა, გარდა იმ შემთხვევებისა, როცა სახეზეა ქსოვილების დაზიანება ან სხვა გართულებები.
ინტოქსიკაცია დამოკიდებულია ოპიოიდის ტიპსა და დოზაზე და მასზე გავლენას ახდენს იმგვარი ფაქტორები, როგორიცაა ტოლერანტობის ინდივიდუალური დონე. ინდივიდები ხშირად იღებენ ნარკოტიკებს იმ რაოდენობით, რაც საჭიროა ინტოქსიკაციის საჭირო დონის მისაღწევად. ქცევა, რომელიც გამოწვეულია ინტოქსიკაციის მოცემული დონით, მნიშვნელოვნად განისაზღვრება კულტურული და პიროვნული მოლოდინით ნარკოტიკების ეფექტების მიმართ.
მწვავე ინტოქსიკაცია არის ICD-10-ის ტერმინი კლინიკურად მნიშვნელოვანი ინტოქსიკაციისთვის (F11.0). გართულებები შეიძლება მოიცავდეს ტრავმას, პირნაღები მასების ინჰალაციას, დელირიუმს, კომას და კრუნჩხვებს ნივთიერებაზე და შეყვანის მეთოდზე დამოკიდებულებით.
ოპიოიდების ზედოზირება
ოპიოიდების გამოყენება იმ რაოდენობით, რაც იწვევს მწვავე ფიზიკურ და ფსიქიკურ ეფექტებს. განგებ ზედოზირება თვითმკვლელობის ხშირი მეთოდია. აბსოლუტურ რიცხვებს თუ ავიღებთ, კანონიერი ოპიოიდების ზედოზირება უფრო ხშირია, ვიდრე უკანონო ოპიოიდების. ზედოზირებამ შეიძლება გამოიწვიოს გარდამავალი/ხანგრძლივი ეფექტები ან სიკვდილი; კონკრეტული ოპიოიდის სასიკვდილო დოზა ინდივიდუალურია და გარკვეულ პირობებზეც არის დამოკიდებული.
ოპიოიდების გამოყენებასთან დაკავშირებული დაავადებები
დაავადებების ჯგუფი, რომლებიც დაკავშირებულია ოპიოიდების გამოყენებასთან. ICD-10-ში ნაწილი F11.0-0 („ფსიქიკური და ქცევითი დაავადებები, გამოწვეული ფსიქოაქტიური ნივთიერების გამოყენებით (ოპიოიდები)“) მოიცავს სხვადასხვა სიმძიმის და კლინიკური ფორმის დაავადებებს. ყველა მათგანს საერთო აქვს ოპიოიდების მოხმარება, რაც შეიძლება გამოიყენებოდეს როგორც სამედიცინო, ისე არასამედიცინო დანიშნულებით. კლინიკური მდგომარეობები, რომლებიც შეიძლება განვითარდეს, მოიცავს მწვავე ინტოქსიკაციას, საზიანო მოხმარებას, დამოკიდებულების სინდრომს, აღკვეთის სინდრომს (ან აღკვეთის მდგომარებას), აღკვეთის მდგომარეობას დელირიუმთან ერთად, ფსიქოზს და ამნესტიურ სინდრომს.
ოპიოიდური აღკვეთის სინდრომი
დროთა განმავლობაში, როდესაც ხდება პრეპარატის აღკვეთა, მორფინი და მისი ანალოგები იწვევს ტოლერანტობას და ჰიპერაგზნებადობაზე პასუხისმგებელ ნეიროადაპტაციურ ცვლილებებს. აღკვეთის სინდრომი მოიცავს ლტოლვას, აგზნებადობას, დისფორიას, მთქნარებას, ოფლიანობას, ბატის კანს, ცრემლდენას, რინორეას (სურდო), ინსომნიას, გულისრევას ან ღებინებას, დიარეას, სპაზმებს, კუნთების ტკივილს და ცხელებას. ხანმოკლე მოქმედების პრეპარატების შემთხვევაში (მორფინი ან ჰეროინი) აღკვეთის სიმპტომები შეიძლება გაჩნდეს პრეპარატის ბოლო დოზის მიღებიდან 8-12 საათში, პიკს მიაღწევს 48-72 საათში და მოიხსნება 7-10 დღეში. უფრო ხანგრძლივი მოქმედების პრეპარატების შემთხვევაში (მეთადონი) აღკვეთის სიმპტომები შეიძლება არ დაიწყოს ბოლო დოზიდან 1-3 დღის განმავლობაში; სიმპტომები პიკს აღწევს მე-3-8 დღეებს შორის და შეიძლება რამდენიმე კვირის განმავლობაში გაგრძელდეს, მაგრამ, როგორც წესი, უფრო მსუბუქია, ვიდრე მორფინის ან ჰეროინის აღკვეთის შემდეგ განვითარებული სიმპტომები.
ფსიქოსოციალური ჩარევა
ნებისმიერი არაფარმაკოლოგიური ჩარევა, რომელიც ინდივიდს, ოჯახს ან ჯგუფს თერაპიულ კონტექსტში უტარდება. ფსიქოსოციალური ჩარევა შეიძლება მოიცავდეს სტრუქტურირებულ, პროფესიულად განსაზღვრულ (მაგ., კოგნიტური ქცევითი თერაპია ან ორიენტირებული ფსიქოთერაპია) ან არაპროფესიულ ჩარევას (მაგ., თვითდახმარების ჯგუფები და არაფარმაკოლოგიური ჩარევა ტრადიციული მკურნალების მიერ).
ფსიქოტროპული ნივთიერება
ფსიქოტროპული ნივთიერებები ის ბუნებრივი ან სინთეზური ნივთიერებებია, რომლებიც ფსიქოტროპული ნივთიერებების (1971) I, II, III ან IV ცხრილშია მოცემული (იხ. ზემოთ). ბუპრენორფინი და ბენზოდიაზეპინები ფსიქოტროპულ ნივთიერებებს განეკუთვნება.
ნარკოტიკული პრეპარატების პირველი კონვენცია (1961)
ნარკოტიკული პრეპარატების პირველი კონვენცია (1961) (შესწორებები შევიდა 1972 წლის პროტოკოლით) არის ნარკოტიკების კონტროლის ძირითადი საერთაშორისო შეთანხმება. მან ბევრი მანამდე არსებული კონვენცია ჩაანაცვლა. მისი მიზანია, ნარკოტიკული პრეპარატების პროდუქციის, წარმოების და მოხმარების შეზღუდვა მხოლოდ სამედიცინო და სამეცნიერო მიზნებით სარგებლობისათვის (ხელმისაწვდომობის უზრუნველყოფით). კონვენციაში ჩამოთვლილია მრავალი ნარკოტიკული პრეპარატი და მოცემულია პასუხისმგებლობები ქვეყნებში ამ პრეპარატების წარმოების, განაწილების და გამოყენების შესახებ. INCB, რომელიც CND-ის საშუალებით ანგარიშს უგზავნის ECOSOC-ს, პასუხისმგებელია მთავრობების მიერ ამ შეთანხმების პირობების შესრულებაზე. მეთადონი მოცემულია ნარკოტიკული პრეპარატების პირველ კონვენციაში (1961).
ტოლერანტობა
წამლის დოზაზე რეაქციის დაქვეითება ხანგრძლივი გამოყენების შედეგად. თუ ინდივიდი წამლის მიმართ ტოლერანტულია, მას მზარდი დოზები სჭირდება იმისათვის, რომ ის ეფექტი მიიღოს, რასაც ადრე დაბალი დოზები იძლეოდა. ტოლერანტობის განვითარებაზე გავლენას ახდენს როგორც ფიზიოლოგიური, ისე ფსიქოლოგიური ფაქტორები. ფსიქოლოგიური ფაქტორები მოიცავს მეტაბოლურ და ფუნქციურ ტოლერანტობას. მეტაბოლური ტოლერანტობის დროს პრეპარატი ორგანიზმიდან უფრო ადვილად ელიმინირდება, რადგან ნივთიერება უფრო სწრაფად მეტაბოლიზდება. ფუნქციური ტოლერანტობის შემთხვევაში ცენტრალური ნერვული სისტემა ნაკლებად მგრძნობიარეა ნივთიერების მიმართ. ტოლერანტობის ხელშემწყობი ფსიქოსოციალური ფაქტორის მაგალითია ქცევითი ტოლერანტობა, რომლის დროსაც დასწავლა და შეცვლილი გარემო ცვლის პრეპარატის ეფექტს. მწვავე ტოლერანტობა გულისხმობს ნივთიერების ერთი დოზის შემდეგ განვითარებულ სწრაფ, დროებით ეფექტს. რევერსიული ტოლერანტობა, რომელსაც ასევე სენსიტიზაციას უწოდებენ, გულისხმობს მდგომარეობას, რომლის დროსაც ნივთიერებაზე რეაქცია განმეორებითი გამოყენების შედეგად იზრდება. ტოლერანტობა დამოკიდებულების სინდრომის ერთ-ერთი კრიტერიუმია.
აღკვეთის სინდრომი (აბსტინენციის სინდრომი, აღკვეთის რეაქცია, აღკვეთის მდგომარეობა)
ჯგუფი სხვადასხვაგვარი სიმძიმის სიმპტომებისა, რომლებიც აღინიშნება ფსიქოაქტიური ნივთიერების გამოყენების შეწყვეტის ან დოზის შემცირების შედეგად მისი რეგულარული გამოყენების შემდეგ (ICD-10 კოდი F1x.3). აღკვეთის სინდრომს შეიძლება თან ახლდეს ფიზიოლოგიური დარღვევების სინდრომი. ეს დამოკიდებულების სინდრომის ერთ-ერთი ინდიკატორია და დამოკიდებულების ფსიქოფარმაკოლოგიური განსაზღვრების მახასიათებელია.
აღკვეთის სინდრომის დაწყება და მიმდინარეობა დროში შეზღუდულია და უკავშირდება გამოყენების შეწყვეტამდე ან დოზის შემცირებამდე მიღებული ნივთიერების ტიპს და დოზას. ტიპობრივად, აღკვეთის სინდრომის ნიშნები მწვავე ინტოქსიკაციის საწინააღმდეგოა.
ოპიოიდური აღკვეთის მდგომარეობას თან ახლავს რინორეა (სურდო), ცრემლისდენა, კუნთების ტკივილი, ბატის კანი, 24-48 საათის შემდეგ კი კუნთების და აბდომინალური სპაზმები. გამოხატულია ნარკოტიკის მოპოვებისკენ მიმართული ქცევა, რომელიც გრძელდება ფიზიკური სიმპტომების უკუგანვითარების შემდეგაც.
 |
23 გამოყენებული ლიტერატურა |
▲back to top |
1. Economic and Social Council (2004). ECOSOC resolution 2004/40, http://www.un.org/docs/ecosoc/documents/2004/resolutions/eres2004-40.pdf (accessed 1/2/2008).
2. United Nations Office on Drugs and Crime (2007). World Drug Report.
3. Hser YI, Hoffman V, Grella CE and Anglin MD (2001). A 33-year follow-up of narcotics addicts. Archives of General Psychiatry, 58(5):503-508.
4. Mark TL, Woody GE, Juday T and Kleber HD (2001). The economic costs of heroin addiction in the United States. Drug Alcohol Dependence, 61(2):195-206.
5. UNAIDS (Joint United Nations Programme on HIV/AIDS) (2006). Report on the global AIDS epidemic. Geneva, Switzerland. http://www.unaids.org/en/ KnowledgeCentre/HIVData/GlobalReport/2006/ (Accessed 14 July 2008).
6. Piot P and Coll Seck AM (2001). International response to the HIV/AIDS epidemic: planning for success. Bulletin of the World Health Organization, 79(12):1106-1112.
7. World Health Organization (2004) WHO/UNODC/UNAIDS position paper. Substitution maintenance therapy in the management of opioid dependence and HIV/AIDS prevention. Geneva, WHO.
8. World Health Organization (2007). WHO Model List of Essential Medicines. Geneva, World Health Organization. Available from URL: http://www.who.int/medicines.
9. World Health Organization (2004). Neuroscience of psychoactive substance use and dependence. Geneva, WHO.
10. World Health Organization (1996). WHO Expert Committee on Drug Dependence. Geneva, Switzerland, 13th report, WHO technical report series 873. http://whqlibdoc.who.int/trs/WHO_TRS_873.pdf (Accessed 9 July 2008)
11. World Health Organization (2006). Basic Principles for Treatment and Psychosocial Support of Drug Dependent People Living with HIV/AIDS. Geneva, WHO.
12. World Health Organization (2002). Guidelines for WHO Guidelines, Global Programme on Evidence for Health Policy. http://libdoc.who.int/hq/2003/EIP_GPE_EQC_2003_1.pdf (Accessed 9 July 2008).
13. Atkins D, Eccles M, Flottorp S, Guyatt GH, Henry D, Hill S, Liberati A, O'Connell D, Oxman AD, Phillips B, Schunemann H, Edejer TT, Vist GE and Williams JW, Jr. (2004). Systems for grading the quality of evidence and the strength of recommendations I: critical appraisal of existing approaches The GRADE Working Group. BMC Health Services Research, 4(1):38.
14. World Health Organization (2007). International Classification of Diseases, 10th edition (ICD-10). http://www.who.int/classifications/apps/icd/icd10online/(Accessed 2008 9 July).
15. Volkow ND and Li TK (2004). Drug addiction: the neurobiology of behaviour gone awry. Nature Reviews. Neuroscience. 5(12):963-970.
16. Ballantyne JC and LaForge KS (2007). Opioid dependence and addiction during opioid treatment of chronic pain. Pain. 129(3):235-255.
17. Yaksh TL (1984). Multiple opioid receptor systems in brain and spinal cord: Part I. European Journal of Anaesthesiology. 1(2):171-199.
18. Yaksh TL (1984). Multiple opioid receptor systems in brain and spinal cord: Part 2. European Journal of Anaesthesiology. 1(3):201-243.
19. Bodnar RJ and Klein GE (2006). Endogenous opiates and behavior: 2005. Peptides, 27(12):3391-3478.
20. Johnson SW and North RA (1992). Opioids excite dopamine neurons by hyperpolarization of local interneurons. Journal of Neuroscience. 12(2):483-488.
21. Bonci A and Williams JT (1997). Increased probability of GABA release during withdrawal from morphine. Journal of Neuroscience. 17(2):796-803.
22. Cami J and Farre M (2003). Drug addiction. New England Journal of Medicine. 349(10):975-986.
23. Nestler EJ, Berhow MT and Brodkin ES (1996). Molecular mechanisms of drug addiction: adaptations in signal transduction pathways. Molecular Psychiatry. 1(3):190-199.
24. Hyman SE and Malenka RC (2001). Addiction and the brain: the neurobiology of compulsion and its persistence. Nature Reviews. Neuroscience. 2(10):695-703.
25. Williams JT, Christie MJ and Manzoni O (2001). Cellular and synaptic adaptations mediating opioid dependence. Physiological Reviews. 81(1):299-343.
26. Kieffer BL and Evans CJ (2002). Opioid tolerance-in search of the holy grail. Cell, 108(5):587-590.
27. US Census Bureau (2004). The AIDS Pandemic in the 21st Century. International Population Reports. Washington, DC, US Government Printing Office, WP/02-2.
28. Centers for Disease Control (1998). Mortality and Morbidity Weekly Report., 47(RR-19).
29. Hulse GK, English DR, Milne E and Holman CD (1999). The quantification of mortality resulting from the regular use of illicit opiates. Addiction. 94(2):221-229.
30. Darke S and Ross J (2002). Suicide among heroin users: rates, risk factors and methods. Addiction. 97(11):1383-1394.
31. Vlahov D, Wang CL, Galai N, Bareta J, Mehta SH, Strathdee SA and Nelson KE (2004). Mortality risk among new onset injection drug users. Addiction. 99(8):946-954.
32. Goldstein A and Herrera J (1995). Heroin addicts and methadone treatment in Albuquerque: a 22-year follow-up. Drug and Alcohol Dependence. 40(2):139-150.
33. Bargagli AM, Sperati A, Davoli M, Forastiere F and Perucci CA (2001). Mortality among problem drug users in Rome: an 18-year follow-up study, 1980-97. Addiction. 96(10):1455-1463.
34. Stein MD, Mulvey KP, Plough A and Samet JH (1998). The functioning and well being of persons who seek treatment for drug and alcohol use. J Subst Abuse, 10(1):75-84.
35. Ross J, Teesson M, Darke S, Lynskey M, Ali R, Ritter A and Cooke R (2005). The characteristics of heroin users entering treatment: findings from the Australian treatment outcome study (ATOS). Drug and Alcohol Review. 24(5):411-418.
36. Collins DJ and Lapsley HM (1996). The social costs of drug abuse in Australia in 1988 and 1992. Canberra, Australia.
37. Xie X, Rehm J, Single E, Robson L and Paul J (1998). The economic costs of Illicit drug use in Ontario, 1992. electronic Health Economics letters, 2(1):8-14.
38. Clark, N., Gospodarevskaya, E., Harris, A. & Ritter, A. Estimating the Cost of Heroin Use in Victoria. Report to the Premier's Drug Prevention Council. Melbourne: Department of Human Services 2003. Available online at URL: http://www.druginfo.adf.org.au/hidden_articles/estimating_the_cost_of_heroin_1.html39.
39. Darke S, Ross J, Mills KL, Williamson A, Havard A and Teesson M (2007). Patterns of sustained heroin abstinence amongst long-term, dependent heroin users: 36 months findings from the Australian Treatment Outcome Study (ATOS). Addictive Behaviors. 32(9):1897-1906.
40. Maddux JF and Desmond DP (1992). Methadone maintenance and recovery from opioid dependence. American Journal of Drug and Alcohol Abuse. 18(1):63-74.
41. Flynn PM, Joe GW, Broome KM, Simpson DD and Brown BS (2003). Recovery from opioid addiction in DATOS. Journal of Substance Abuse Treatment, 25(3):177-186.
42. Hser YI (2007). Predicting long-term stable recovery from heroin addiction: findings from a 33-year follow-up study. Journal of Addictive Diseases, 26(1):51-60.
43. Teesson M, Ross J, Darke S, Lynskey M, Ali R, Ritter A and Cooke R (2006). One year outcomes for heroin dependence: findings from the Australian Treatment Outcome Study (ATOS). Drug & Alcohol Dependence, 83(2):174-180.
44. Gandhi DH, Jaffe JH, McNary S, Kavanagh GJ, Hayes M and Currens M (2003). Short-term outcomes after brief ambulatory opioid detoxification with buprenorphine in young heroin users. Addiction. 98(4):453-462.
45. Hser YI, Anglin MD and Fletcher B (1998). Comparative treatment effectiveness. Effects of program modality and client drug dependence history on drug use reduction. Journal of Substance Abuse Treatment, 15(6):513-523.
46. Calsyn DA, Malcy JA and Saxon AJ (2006). Slow tapering from methadone maintenance in a program encouraging indefinite maintenance. Journal of Substance Abuse Treatment, 30(2):159-163.
47. Lenne M, Lintzeris N, Breen C, Harris S, Hawken L, Mattick R and Ritter A (2001). Withdrawal from methadone maintenance treatment: prognosis and participant perspectives. Australian & New Zealand Journal of Public Health, 25(2):121-125.
48. Hiltunen AJ and Eklund C (2002). Withdrawal from methadone maintenance treatment. Reasons for not trying to quit methadone. European Addiction Research, 8(1):38-44.
49. World Health Organization (2006). Constitution of the World Health Organization. Geneva, Basic Documents, 45th edition, Supplement October 2006. http://www.who.int/governance/eb/who_constitution_en.pdf (Accessed 9 July 2008).
50. World Health Organization (1986). www.who.int/hpr/NPH/docs/ottawa_charter_hp.pdf (accessed 12 December, 2008).
51. Hall WD, Ross JE, Lynskey MT, Law MG and Degenhardt LJ (2000). How many dependent heroin users are there in Australia? Medical Journal of Australia. 173(10):528-531.
52. World Health Organization (1993). WHO Expert Committee on Drug Dependence, Twenty-eighth Report. WHO Technical Report Series, No. 836.
53. Reilly D, Scantleton J and Didcott P (2002). Magistrates' Early Referral into Treatment (MERIT): preliminary findings of a 12-month court diversion trial for drug offenders. Drug and Alcohol Review. 21(4):393-396.
54. Fielding JE, Tye G, Ogawa PL, Imam IJ and Long AM (2002). Los Angeles County drug court programs: initial results. Journal of Substance Abuse Treatment. 23(3):217-224.
55. Britton B (1994). The privatization of methadone maintenance; changes in risk behavior associated with cost related detoxification. Addiction Research, 2(2):171-181.
56. McCollister K and French M (2003). The relative contribution of outcome domains in the total economic benefit of addiction interventions: a review of first findings. Addiction. 98:1647-1659.
57. French M and Drummond M (2005). A research agenda for economic evaluation of substance abuse services. Journal of Substance Abuse Treatment, 29:125-137.
58. French M and Martin R (1996). The Costs of Drug Abuse Consequences: A Summary of Research Findings. Journal of Substance Abuse Treatment, 13(6):453-466.
59. Choi B, Robson L and Single E (1997). Estimating the economic costs of the abuse of tobacco, alcohol and illicit drugs: a review of methodologies and Canadian data sources. Chronic Diseases in Canada, 18(4):149-165.
60. Cartwright WS (2000). Cost-benefit analysis of drug treatment services: review of the literature. Journal of Mental Health Policy and Economics, 3:11-26.
61. Hall W, Doran C, Degenhardt L and Shepard D (2006). Illicit Opioid Use. In: Musgrove P, ed. Disease control priorities in developing countries. New York, Oxford University Press, 2, 907-932.
62. Simoens S, Ludbrook A, Matheson C and Bond C (2006). Pharmaco-economics of community maintenance for opiate dependence: a review of evidence and methodology. Drug and Alcohol Dependence. 84(1):28-39.
63. Simoens S, Matheson C, Inkster K, Ludbrook A and Bond C (2002). The effectiveness of treatment for drug users: An international systematic review of the evidence. Edinburgh, Scottish Executive Drug Misuse Research Programme
64. World Health Organization (2008). Choosing Interventions that are Cost Effective: Cost-it. http://www.who.int/choice/toolkit/cost_it/en/ (Accessed 2008 16 July).
65. Dole VP and Nyswander M (1965). A medical treatment for diacetylmorphine (heroin) addiction. Journal of the American Medical Association, 193:80-84.
66. Dole V, Robinson J and Orraca J (1969). Methadone treatment of randomly selected criminal addicts. New Engand Journal of Medicine, 280:1372-1375.
67. Dole VP (1971). Methadone maintenance treatment for 25000 addicts. Journal of the American Medical Association, 215:1131-1134.
68. Lintzeris N, Ritter A, Panjari M, Clark N, Kutin J and Bammer G (2004). Implementing buprenorphine treatment in community settings in Australia: experiences from the Buprenorphine Implementation Trial. American Journal of Addiction. 13 Suppl 1:S29-41.
69. Alford DP, LaBelle CT, Richardson JM, O'Connell JJ, Hohl CA, Cheng DM and Samet JH (2007). Treating homeless opioid dependent patients with buprenorphine in an office-based setting. Journal of General Internal Medicine. 22(2):171-176.
70. Fiellin DA, O'Connor PG, Chawarski M, Pakes JP, Pantalon MV and Schottenfeld RS (2001). Methadone maintenance in primary care: a randomized controlled trial. Jama. 286(14):1724-1731.
71. Bell J, Dru A, Fischer B, Levit S and Sarfraz MA (2002). Substitution therapy for heroin addiction. Substance Use and Misuse. 37(8-10):1149-1178.
72. Gibson AE, Doran CM, Bell JR, Ryan A and Lintzeris N (2003). A comparison of buprenorphine treatment in clinic and primary care settings: a randomised trial. Medical Journal of Australia. 179(1):38-42.
73. Vignau J, Boissonnas A, Tignol J, Millot Y and Mucchielli A (2003). [French nationwide survey of abstinence-oriented treatments in opiate-addicted patients. Results at 12 months]. Annales de Médecine Interne (Paris). 154 Spec No 2:S23-32.
74. World Health Organization (2007). Health in prisons: A WHO guide to the essentials in prison health. http://www.euro.who.int/document/e90174.pdf (Accessed 09 July 2008).
75. United Nations General Assembly (1966). International Covenant on Economic, Social and Cultural Rights. http://www.unhchr.ch/html/menu3/b/a_cescr. htm (accessed 2008 1 March), resolution 2200A (XXI).
76. World Health Organization (2005). WHO Resource Book on Mental Health, Human Rights and Legislation. Geneva, WHO.
77. Kornor H and Waal H (2005). From opioid maintenance to abstinence: a literature review. Drug and Alcohol Review. 24(3):267-274.
78. Piper TM, Rudenstine S, Stancliff S, Sherman S, Nandi V, Clear A and Galea S (2007). Overdose prevention for injection drug users: lessons learned from naloxone training and distribution programs in New York City. Harm Reduction Journal. 4:3.
79. Seal KH, Thawley R, Gee L, Bamberger J, Kral AH, Ciccarone D, Downing M and Edlin BR (2005). Naloxone distribution and cardiopulmonary resuscitation training for injection drug users to prevent heroin overdose death: a pilot intervention study. Journal of Urban Health. 82(2):303-311.
80. Fry C, Dietze P and Crofts N (2000). Naloxone distribution: remembering hepatitis C transmission as an issue. Addiction. 95(12):1865-1866.
81. Wang H, He G, Li X, Yang A, Chen X, Fennie KP and Williams AB (2008). Self-Reported Adherence to Antiretroviral Treatment among HIV-Infected People in Central China. AIDS Patient Care STDS. 22(1): 71-80.
82. Smith-Rohrberg D, Mezger J, Walton M, Bruce RD and Altice FL (2006). Impact of enhanced services on virologic outcomes in a directly administered antiretroviral therapy trial for HIV-infected drug users. Journal of the Acquired Immunodeficiency Syndrome. 43 Suppl 1:S48-53.
83. Lucas GM, Gebo KA, Chaisson RE and Moore RD (2002). Longitudinal assessment of the effects of drug and alcohol abuse on HIV-1 treatment outcomes in an urban clinic. Aids. 16(5):767-774.
84. van Beek I (2007). Case study: accessible primary health care - a foundation to improve health outcomes for people who inject drugs. International Journal of Drug Policy. 18(4):329-332.
85. Krook AL, Stokka D, Heger B and Nygaard E (2007). Hepatitis C treatment of opioid dependants receiving maintenance treatment: results of a Norwegian pilot study. European Addiction Research. 13(4):216-221.
86. Sylvestre DL and Clements BJ (2007). Adherence to hepatitis C treatment in recovering heroin users maintained on methadone. European Journal of Gastroenterology and Hepatology. 19(9):741-747.
87. Edlin BR, Kresina TF, Raymond DB, Carden MR, Gourevitch MN, Rich JD, Cheever LW and Cargill VA (2005). Overcoming barriers to prevention, care, and treatment of hepatitis C in illicit drug users. Clinical Infectious Disease. 40 Suppl 5:S276-285.
88. Umbricht-Schneiter A, Ginn DH, Pabst KM and Bigelow GE (1994). Providing medical care to methadone clinic patients: referral vs on-site care. American Journal of Public Health. 84(2):207-210.
89. Weisner C, Mertens J, Parthasarathy S, Moore C and Lu Y (2001). Integrating primary medical care with addiction treatment: a randomized controlled trial. Jama. 286(14):1715-1723.
90. Willenbring ML and Olson DH (1999). A randomized trial of integrated outpatient treatment for medically ill alcoholic men. Archives of Internal Medicine. 159(16):1946-1952.
91. Scholten JN, Driver CR, Munsiff SS, Kaye K, Rubino MA, Gourevitch MN, Trim C, Amofa J, Seewald R, Highley E and Fujiwara PI (2003). Effectiveness of isoniazid treatment for latent tuberculosis infection among human immunodeficiency virus (HIV)-infected and HIV-uninfected injection drug users in methadone programs. Clinical Infectious Disease. 37(12):1686-1692.
92. Gourevitch MN, Selwyn PA, Davenny K, Buono D, Schoenbaum EE, Klein RS and Friedland GH (1993). Effects of HIV infection on the serologic manifestations and response to treatment of syphilis in intravenous drug users. Annals of Internal Medicine. 118(5):350-355.
93. O'Connor PG, Molde S, Henry S, Shockcor WT and Schottenfeld RS (1992). Human immunodeficiency virus infection in intravenous drug users: a model for primary care. American Journal of Medicine. 93(4):382-386.
94. Newman RG (1994). More on methadone treatment. American Journal of Public Health. 84(11):1854.
95. World Health Organization (2004). Weekly Epidemiological Record, 28(79):253-264.
96. Altice FL, Bruce RD, Walton MR and Buitrago MI (2005). Adherence to hepatitis B virus vaccination at syringe exchange sites. Journal of Urban Health. 82(1):151-161.
97. Christensen PB, Fisker N, Krarup HB, Liebert E, Jaroslavtsev N, Christensen K and Georgsen J (2004). Hepatitis B vaccination in prison with a 3-week schedule is more efficient than the standard 6-month schedule. Vaccine. 22(29-30):3897-3901.
98. Macdonald V, Dore GJ, Amin J and van Beek I (2007). Predictors of completion of a hepatitis B vaccination schedule in attendees at a primary health care centre. Sex Health. 4(1):27-30.
99. Okruhlica L and Klempova D (2002). Hodnocení programu vakcinace proti hepatitide typu B u uživatelú drog v Bratislave (Evaluation of a Hepatitis B Vaccination Programme among Drug Users in Bratislava). Adiktologie, 2:11-18.
100. Quaglio G, Talamini G, Lugoboni F, Lechi A, Venturini L, Jarlais D and Mezzelani P (2003). Compliance with hepatitis B vaccination in 1175 heroin users and risk factors associated with lack of vaccine response. Addiction. 97(12):1611-1613.
101. Mattos A, Gomes E, Tovo C, Alexandre C and Remião J (2004). Hepatitis B vaccine efficacy in patients with chronic liver disease by hepatitis C virus. Arq Gastroenterol. 41(3):180-184.
102. World Health Organization (2000). Weekly Epidemiological Record, 5(75):37-44.
103. World Health Organization (2008). WHO collaborative research project on drug dependence treatment and HIV/AIDS. http://www.who.int/substance_ abuse/activities/treatment_HIV/en/index.html (Accessed 12 December 2008).
104. Williams JT, Christie MJ and Manzoni O (2001). Cellular and synaptic adaptations mediating opioid dependence. Physiological Reviews, 81(1):299-343.
105. Mattick RP, Breen C, Kimber J and Davoli M (in press). Methadone maintenance therapy versus no opioid replacement therapy for opioid dependence. Cochrane Database Systematic Review.
106. Newman RG and Whitehill WB (1979). Double-blind comparison of methadone and placebo maintenance treatments of narcotic addicts in Hong Kong. Lancet. 2(8141):485-488.
107. Vanichseni S, Wongsuwan B, Choopanya K and Wongpanich K (1991). A controlled trial of methadone maintenance in a population of intravenous drug users in Bangkok: implications for prevention of HIV. International Journal of Addiction. 26(12):1313-1320.
108. Strain EC, Stitzer ML, Liebson IA and Bigelow GE (1993). Dose-response effects of methadone in the treatment of opioid dependence. Annals of Internal Medicine. 119(1):23-27.
109. Johnson RE, Eissenberg T, Stitzer ML, Strain EC, Liebson IA and Bigelow GE (1995). A placebo controlled clinical trial of buprenorphine as a treatment for opioid dependence. Drug and Alcohol Dependence. 40(1):17-25.
110. Ling W, Charuvastra C, Collins JF, Batki S, Brown LS, Jr, Kintaudi P, Wesson DR, McNicholas L, Tusel DJ, Malkerneker U, Renner JA, Jr, Santos E, Casadonte P, Fye C, Stine S, Wang RI and Segal D (1998). Buprenorphine maintenance treatment of opiate dependence: a multicenter, randomized clinical trial. Addiction. 93(4):475-486.
111. Caplehorn JRM and Drummer OH (1999). Mortality associated with New South Wales methadone programs in 1994: lives lost and saved. Medical Journal of Australia, 170:104-109.
112. Lawrinson P, Ali R, Uchtenhagen A and Newcombe D (2009). The WHO Collaborative Study on Substitution Therapy of Opioid Dependence and HIV/AIDS. Geneva. http://www.who.int/substance_abuse/en/index.html.
113. Moore TJ, Ritter A and Caulkins JP (2007). The costs and consequences of three policy options for reducing heroin dependency. Drug and Alcohol Review. 26(4):369-378.
114. Zarkin GA, Dunlap LJ, Hicks KA and Mamo D (2005). Benefits and costs of methadone treatment: results from a lifetime simulation model. Health Economics. 14(11):1133-1150.
115. Barnett PG (1999). The cost-effectiveness of methadone maintenance as a health care intervention. Addiction. 94(4):479-488.
116. Hall WD, Doran CM, Degenhardt LJ and Shepard D (2006). Illicit Opiate Abuse. In: Department of Mental Health and Substance Abuse, ed. Disease Control Priorities related to Mental, Neurological, Developmental and Substance Abuse Disorders. Geneva, World Health Organization, 77-100.
117. Bell J, Digiusto E and Byth K (1992). Who should receive methadone maintenance? British Journal of Addiction. 87(5):689-694.
118. Mattick RP, Kimber J, Breen C and Davoli M (2004). Buprenorphine maintenance versus placebo or methadone maintenance for opioid dependence. Cochrane Database Systematic Review.(3):CD002207.
119. Auriacombe M, Fatseas M, Dubernet J, Daulouede JP and Tignol J (2004). French field experience with buprenorphine. American Journal of Addiction. 13 Suppl 1:S17-28.
120. Auriacombe M, Franques P and Tignol J (2001). Deaths attributable to methadone vs buprenorphine in France. Jama. 285(1):45.
121. Kintz P (2002). A new series of 13 buprenorphine-related deaths. Clinical Biochemistry. 35(7):513-516.
122. Kintz P (2001). Deaths involving buprenorphine: a compendium of French cases. Forensic Science International. 121(1-2):65-69.
123. Anonymous (2006). Buprenorphine replacement therapy: a confirmed benefit. Prescrire International. 15(82):64-70.
124. Bargagli AM, Sperati A, Davoli M, Forastiere F and Perucci CA (2001). Mortality among problem drug users in Rome: an 18-year follow-up study, 1980-97. Addiction. 96(10):1455-1463.
125. Petitjean S, Stohler R, Deglon JJ, Livoti S, Waldvogel D, Uehlinger C and Ladewig D (2001). Double-blind randomized trial of buprenorphine and methadone in opiate dependence. Drug and Alcohol Dependence. 62(1):97-104.
126. Soyka M, Hock B, Kagerer S, Lehnert R, Limmer C and Kuefner H (2005). Less impairment on one portion of a driving-relevant psychomotor battery in buprenorphine-maintained than in methadone-maintained patients: results of a randomized clinical trial. Journal of Clinical Psychopharmacology. 25(5):490-493.
127. Lenné M, Dietze P, Rumbold GR, Redman JR and Triggs TJ (2003). The effects of the opioid pharmacotherapies methadone, LAAM and buprenorphine, alone and in combination with alcohol, on simulated driving. Drug and Alcohol Dependence. 72(3):271-278.
128. Jenkinson RA, Clark NC, Fry CL and Dobbin M (2005). Buprenorphine diversion and injection in Melbourne, Australia: an emerging issue? Addiction. 100(2):197-205.
129. Fanoe S, Hvidt C, Ege P and Jensen GB (2007). Syncope and QT prolongation among patients treated with methadone for heroin dependence in the city of Copenhagen. Heart. 93(9):1051-5.
130. Anonymous (2005). Torsades de pointes with methadone. Prescrire International. 14(76):61-62.
131. Krantz MJ, Garcia JA and Mehler PS (2005). Effects of buprenorphine on cardiac repolarization in a patient with methadone-related torsade de pointes. Pharmacotherapy. 25(4):611-614.
132. Baker JR, Best AM, Pade PA and McCance-Katz EF (2006). Effect of buprenorphine and antiretroviral agents on the QT interval in opioid-dependent patients. Annals of Pharmacotherapy. 40(3):392-396.
133. Dyer KR and White JM (1997). Patterns of symptom complaints in methadone maintenance patients. Addiction. 92(11):1445-1455.
134. Caplehorn JR, Bell J, Kleinbaum DG and Gebski VJ (1993). Methadone dose and heroin use during maintenance treatment. Addiction. 88(1):119-124.
135. D'Ippoliti D, Davoli M, Perucci CA, Pasqualini F and Bargagli AM (1998). Retention in treatment of heroin users in Italy: The role of treatment type and of methadone maintenance dosage. Drug and Alcohol Dependence. 52(2):167-171.
136. Maxwell S and Shinderman M (1999). Optimizing response to methadone maintenance treatment: use of higher- dose methadone. Journal of Psychoactive Drugs. 31(2):95-102.
137. Strain EC, Stitzer ML, Liebson IA and Bigelow GE (1993). Methadone dose and treatment outcome. Drug and Alcohol Dependence. 33(2):105-117.
138. Hartel DM, Schoenbaum EE, Selwyn PA, Kline J, Davenny K, Klein RS and Friedland GH (1995). Heroin use during methadone maintenance treatment: the importance of methadone dose and cocaine use. American Journal of Public Health. 85(1):83-88.
139. Gerra G, Ferri M, Polidori E, Santoro G, Zaimovic A and Sternieri E (2003). Long-term methadone maintenance effectiveness: psychosocial and pharmacological variables. Journal of Substance Abuse Treatment. 25(1):1-8.
140. Faggiano F, Vigna-Taglianti F, Versino E and Lemma P (2003). Methadone maintenance at different dosages for opioid dependence. Cochrane Database Systematic Review. (3):CD002208.
141. Kosten TR, Schottenfeld R, Ziedonis D and Falcioni J (1993). Buprenorphine versus methadone maintenance for opioid dependence. Journal of Nervous and Mental Disease. 181(6):358-364.
142. Ahmadi J (2003). Methadone versus buprenorphine maintenance for the treatment of heroin-dependent outpatients. Journal of Substance Abuse Treatment. 24(3):217-220.
143. Schottenfeld RS, Pakes JR, Oliveto A, Ziedonis D and Kosten TR (1997). Buprenorphine vs methadone maintenance treatment for concurrent opioid dependence and cocaine abuse [see comments]. Archives of General Psychiatry. 54(8):713-720.
144. Montoya ID, Gorelick DA, Preston KL, Schroeder JR, Umbricht A, Cheskin LJ, Lange WR, Contoreggi C, Johnson RE and Fudala PJ (2004). Randomized trial of buprenorphine for treatment of concurrent opiate and cocaine dependence. Clinical Pharmacology and Therapeutics. 75(1):34-48.
145. Walsh SL, Preston KL, Bigelow GE and Stitzer ML (1995). Acute administration of buprenorphine in humans: partial agonist and blockade effects. Journal of Pharmacology and Experimental Therapeutics. 274(1):361-372.
146. Comer SD, Collins ED and Fischman MW (2001). Buprenorphine sublingual tablets: effects on IV heroin self- administration by humans. Psychopharmacology (Berl). 154(1):28-37.
147. Greenwald MK, Johanson CE and Schuster CR (1999). Opioid reinforcement in heroin-dependent volunteers during outpatient buprenorphine maintenance. Drug and Alcohol Dependence. 56(3):191-203.
148. Greenwald MK, Schuh KJ, Hopper JA, Schuster CR and Johanson CE (2002). Effects of buprenorphine sublingual tablet maintenance on opioid drugseeking behavior by humans. Psychopharmacology (Berl). 160(4):344-352.
149. Schottenfeld RS, Pakes J, Zidenois D and Kosten TR (1993). Buprenorphine: Dose-related effects on cocaine and opioid use in cocaine-abusing opioid dependent humans. Biological Psychiatry, 34:66-74.
150. Strain EC, Walsh SL and Bigelow GE (2002). Blockade of hydromorphone effects by buprenorphine/naloxone and buprenorphine. Psychopharmacology (Berl). 159(2):161-166.
151. Winstock AR, Lea T and Sheridan J (2008). Prevalence of diversion and injection of methadone and buprenorphine among clients receiving opioid treatment at community pharmacies in New South Wales, Australia. International Journal of Drug Policy. 19(6):450-8.
152. Vlahov D, O'Driscoll P, Mehta SH, Ompad DC, Gern R, Galai N and Kirk GD (2007). Risk factors for methadone outside treatment programs: implications for HIV treatment among injection drug users. Addiction. 102(5):771-777.
153. Shields LB, Hunsaker Iii JC, Corey TS, Ward MK and Stewart D (2007). Methadone toxicity fatalities: a review of medical examiner cases in a large metropolitan area. Journal of Forensic Science. 52(6):1389-1395.
154. Gunderson EW and Fiellin DA (2008). Office-Based Maintenance Treatment of Opioid Dependence : How Does it Compare With Traditional Approaches? CNS Drugs, 22(2):99-111.
155. Kraft MK, Rothbard AB, Hadley TR, McLellan AT and Asch DA (1997). Are supplementary services provided during methadone maintenance really costeffective? American Journal of Psychiatry. 154(9):1214-1219.
156. McLellan AT, Arndt IO, Metzger DS, Woody GE and O'Brien CP (1993). The effects of psychosocial services in substance abuse treatment. Jama. 269(15):1953-1959.
157. Avants SK, Margolin A, Sindelar JL, Rounsaville BJ, Schottenfeld R, Stine S, Cooney NL, Rosenheck RA, Li SH and Kosten TR (1999). Day treatment versus enhanced standard methadone services for opioid-dependent patients: a comparison of clinical efficacy and cost. American Journal of Psychiatry. 156(1):27-33.
158. Shanahan MD, Doran CM, Digiusto E, Bell J, Lintzeris N, White J, Ali R, Saunders JB, Mattick RP and Gilmour S (2006). A cost-effectiveness analysis of heroin detoxification methods in the Australian National Evaluation of Pharmacotherapies for Opioid Dependence (NEPOD). Addictive Behaviors. 31(3):371-387.
159. Gowing L, Ali R and White J (2004). Buprenorphine for the management of opioid withdrawal. Cochrane Database Systematic Review. (4):CD002025.
160. Gowing L, Ali R and White J (2006). Opioid antagonists with minimal sedation for opioid withdrawal. Cochrane Database Systematic Review. (1):CD002021.
161. Gowing L, Ali R and White J (2006). Opioid antagonists under heavy sedation or anaesthesia for opioid withdrawal. Cochrane Database Systematic Review. (2):CD002022.
162. McGregor C, Ali R, White JM, Thomas P and Gowing L (2002). A comparison of antagonist-precipitated withdrawal under anesthesia to standard inpatient withdrawal as a precursor to maintenance naltrexone treatment in heroin users: outcomes at 6 and 12 months. Drug and Alcohol Dependence. 68(1):5-14.
163. Collins ED, Kleber HD, Whittington RA and Heitler NE (2005). Anesthesia-assisted vs buprenorphine- or clonidine-assisted heroin detoxification and naltrexone induction: a randomized trial. Jama. 294(8):903-913.
164. Seoane A, Carrasco G, Cabre L, Puiggros A, Hernandez E, Alvarez M, Costa J, Molina R and Sobrepere G (1997). Efficacy and safety of two new methods of rapid intravenous detoxification in heroin addicts previously treated without success [published erratum appears in Br J Psychiatry 1997 Dec;171:588]. British Journal of Psychiatry. 171:340-345.
165. De Jong CA, Laheij RJ and Krabbe PF (2005). General anaesthesia does not improve outcome in opioid antagonist detoxification treatment: a randomized controlled trial. Addiction. 100(2):206-215.
166. Hamilton RJ, Olmedo RE, Shah S, Hung OL, Howland MA, Perrone J, Nelson LS, Lewin NL and Hoffman RS (2002). Complications of ultrarapid opioid detoxification with subcutaneous naltrexone pellets.Academic Emergency Medicine. 9(1):63-68.
167. Kaye AD, Gevirtz C, Bosscher HA, Duke JB, Frost EA, Richards TA and Fields AM (2003). Ultrarapid opiate detoxification: a review. Canadian Journal of Anaesthesiology. 50(7):663-671.
168. Day E, Ison J and Strang J (2005). Inpatient versus other settings for detoxification for opioid dependence. Cochrane Database Systematic Review. (2):CD004580.
169. Amato L, Minozzi S, Davoli M, Vecchi S, Ferri M and Mayet S (2004). Psychosocial and pharmacological treatments versus pharmacological treatments for opioid detoxification. Cochrane Database Systematic Review.(4):CD005031.
170. Minozzi S, Amato L, Vecchi S, Davoli M, Kirchmayer U and Verster A (2006). Oral naltrexone maintenance treatment for opioid dependence. Cochrane Database Systematic Review.(1):CD001333.
171. Carroll KM, Ball SA, Nich C, O'Connor PG, Eagan DA, Frankforter TL, Triffleman EG, Shi J and Rounsaville BJ (2001). Targeting behavioral therapies to enhance naltrexone treatment of opioid dependence: efficacy of contingency management and significant other involvement. Archives of General Psychiatry. 58(8):755-761.
172. Tucker T, Ritter A, Maher C and Jackson H (2004). A randomized control trial of group counseling in a naltrexone treatment program. Journal of Substance Abuse Treatment. 27(4):277-288.
173. Fals-Stewart W and O'Farrell TJ (2003). Behavioral family counseling and naltrexone for male opioid-dependent patients. Journal of Consulting and Clinical Psychology. 71(3):432-442.
174. Magura S, Blankertz L, Madison EM, Friedman E and Gomez A (2007). An innovative job placement model for unemployed methadone patients: a randomized clinical trial. Substance Use and Misuse. 42(5):811-828.
175. Silverman K, Svikis D, Robles E, Stitzer ML and Bigelow GE (2001). A reinforcement-based therapeutic workplace for the treatment of drug abuse: sixmonth abstinence outcomes. Experimental Clinical Psychopharmacology. 9(1):14-23.
176. Platt JJ and Metzger D (1985). The role of employment in the rehabilitation of heroin addicts. NIDA Research Monograph. 58:111-121.
177. Katz A (1986). Fellowship, Helping and Healing: The Re-Emergence of Self-Help Groups. Nonprofit and Voluntary Sector Quarterly. 15(2):4-13.
178. van Dorp EL, Yassen A and Dahan A (2007). Naloxone treatment in opioid addiction: the risks and benefits. Expert Opinion in Drug Safety. 6(2):125-132.
179. Robins LN (1984). The natural history of adolescent drug use. American Journal of Public Health. 74(7):656-657.
180. Bruner AB and Fishman M (1998). Adolescents and illicit drug use. Jama. 280(7):597-598.
181. Marsch LA, Bickel WK, Badger GJ, Stothart ME, Quesnel KJ, Stanger C and Brooklyn J (2005). Comparison of pharmacological treatments for opioiddependent adolescents: a randomized controlled trial. Archives of General Psychiatry. 62(10):1157-1164.
182. Sells SB and Simpson DD (1979). On the effectiveness of treatment for drug abuse: evidence from the DARP research programme in the United States. Bulletin on Narcotics. 31(1):1-11.
183. Nelson-Zlupko L, Dore MM, Kauffman E and Kaltenbach K (1996). Women in recovery : Their perceptions of treatment effectiveness. Journal of Substance Abuse Treatment, 13(1):51-59.
184. Ahmadi J and Bahrami N (2002). Buprenorphine treatment of opium-dependent outpatients seeking treatment in Iran. Journal of Substance Abuse Treatment. 23(4):415-417.
185. Ahmadi J, Babaee-Beigi M, Alishahi M, Maany I and Hidari T (2004). Twelve-month maintenance treatment of opium-dependent patients. Journal of Substance Abuse Treatment. 26(1):363-366.
186. Cicero TJ, Inciardi JA and Munoz A (2005). Trends in abuse of Oxycontin and other opioid analgesics in the United States: 2002-2004. J Pain. 6(10):662-672.
187. Chang G, Chen L and Mao J (2007). Opioid tolerance and hyperalgesia. Medical Clinics of North America. 91(2):199-211.
188. Gunne LM and Gronbladh L (1981). The Swedish methadone maintenance program: a controlled study. Drug and Alcohol Dependence. 7(3):249-256.
189. Yancovitz S (1991). A randomised trial of an interim methadone maintenance clinic. American Journal of Public Health. 81:1185-1191.
190. Appel PW, Joseph H and Richman BL (2000). Causes and rates of death among methadone maintenance patients before and after the onset of the HIV/AIDS epidemic. Mt Sinai Journal of Medicine. 67(5-6):444-451.
191. Brugal MT, Domingo-Salvany A, Puig R, Barrio G, Garcia de Olalla P and de la Fuente L (2005). Evaluating the impact of methadone maintenance programmes on mortality due to overdose and aids in a cohort of heroin users in Spain. Addiction. 100(7):981-989.
192. Caplehorn JR, Dalton MS, Cluff MC and Petrenas AM (1994). Retention in methadone maintenance and heroin addicts' risk of death. Addiction. 89(2):203-209.
193. Davoli M, Bargagli AM, Perucci CA, Schifano P, Belleudi V, Hickman M, Salamina G, Diecidue R, Vigna-Taglianti F and Faggiano F (2007). Risk of fatal overdose during and after specialist drug treatment: the VEdeTTE study, a national multi-site prospective cohort study. Addiction. 102(12):1954-1959.
194. Fugelstad A, Agren G and Romelsjo A (1998). Changes in mortality, arrests, and hospitalizations in nonvoluntarily treated heroin addicts in relation to methadone treatment. Substance Use and Misuse. 33(14):2803-2817.
195. Buster MC, van Brussel GH and van den Brink W (2002). An increase in overdose mortality during the first 2 weeks after entering or re-entering methadone treatment in Amsterdam. Addiction. 97(8):993-1001.
196. van Ameijden EJ, Langendam MW and Coutinho RA (1999). Dose-effect relationship between overdose mortality and prescribed methadone dosage in low-threshold maintenance programs. Addictive Behaviors. 24(4):559-563.
197. Bargagli A, Davoli M, Minozzi S, Vecchi S and Perucci C (2007). A Systematic Review of Observational Studies on Treatment of Opioid Dependence. Geneva, Switzerland, background document prepared for 3rd meeting of Technical Development Group (TDG) for the WHO Guidelines for Psychosocially Assisted Pharmacotherapy of Opiod Dependence, 17-21 September. http://www.who.int/substance_abuse/activities/observational_studies_treatment.pdf (Accessed 09 July 2008).
198. Metzger DS, Woody GE, McLellan AT, O'Brien CP, Druley P, Navaline H, DePhilippis D, Stolley P and Abrutyn E (1993). Human immunodeficiency virus seroconversion among intravenous drug users in- and out-of-treatment: an 18-month prospective follow-up. Journal of the Acquired Immunodeficiency Syndrome. 6(9):1049-1056.
199. Dolan KA, Shearer J, MacDonald M, Mattick RP, Hall W and Wodak AD (2003). A randomised controlled trial of methadone maintenance treatment versus wait list control in an Australian prison system. Drug and Alcohol Dependence. 72(1):59-65.
200. Stark K, Muller R, Bienzle U and Guggenmoos-Holzmann I (1996). Methadone maintenance treatment and HIV risk-taking behaviour among injecting drug users in Berlin. Journal of Epidemiology and Community Health. 50(5):534-537.
201. Thiede H, Hagan H and Murrill CS (2000). Methadone treatment and HIV and hepatitis B and C risk reduction among injectors in the Seattle area. Journal of Urban Health. 77(3):331-345.
202. Moss AR, Vranizan K, Gorter R, Bacchetti P, Watters J and Osmond D (1994). HIV seroconversion in intravenous drug users in San Francisco, 1985-1990. Aids, 8(2):223-231.
203. Gowing L, Farrell M, Bornemann R and Ali R (2004). Substitution treatment of injecting opioid users for prevention of HIV infection. Cochrane Database Systematic Review.(4).
204. Ahmadi J (2003). Methadone versus buprenorphine maintenance for the treatment of heroin-dependent outpatients. Journal of Substance Abuse Treatment. 24(3):217-220.
205. Johnson RE, Chutuape MA, Strain EC, Walsh SL, Stitzer ML and Bigelow GE (2000). A comparison of levomethadyl acetate, buprenorphine, and methadone for opioid dependence. New England Journal of Medicine. 343(18):1290-1297.
206. Kristensen O, Espegren O, Asland R, Jakobsen E, Lie O and Seiler S (2005). [Buprenorphine and methadone to opiate addicts--a randomized trial]. Tidsskrift for den Norske lægeforening. 125(2):148-151.
207. Mattick, R. P., Ali, R., White, J. M., O'Brien, S., Wolk, S., & Danz, C. (2003). Buprenorphine versus methadone maintenance therapy: a randomized doubleblind trial with 405 opioid-dependent patients. Addiction, 98(4), 441-452.
208. Strain EC, Stitzer ML, Liebson IA and Bigelow GE (1994). Comparison of buprenorphine and methadone in the treatment of opioid dependence. American Journal of Psychiatry. 151(7):1025-1030.
209. Strain EC, Stitzer ML, Liebson IA and Bigelow GE (1994). Buprenorphine versus methadone in the treatment of opioid-dependent cocaine users. Psychopharmacology (Berl). 116(4):401-406.
210. Fischer G, Jagsch R, Eder H, Gombas W, Etzersdorfer P, Schmidl-Mohl K, Schatten C, Weninger M and Aschauer HN (1999). Comparison of methadone and slow-release morphine maintenance in pregnant addicts. Addiction. 94(2):231-239.
211. Ling W, Charuvastra C, Kaim SC and Klett CJ (1976). Methadyl acetate and methadone as maintenance treatments for heroin addicts. A veterans administration cooperative study. Archives of General Psychiatry. 33(6):709-720.
212. Preston KL, Umbricht A and Epstein DH (2000). Methadone dose increase and abstinence reinforcement for treatment of continued heroin use during methadone maintenance. Archives of General Psychiatry. 57(4):395-404.
213. Goldstein A and Judson BA (1973). Proceedings: Efficacy and side effects of three widely different methadone doses. Proceedings of the National Conference on Methadone Treatment. 1:21-44.
214. Strain EC, Bigelow GE, Liebson IA and Stitzer ML (1999). Moderate- vs high-dose methadone in the treatment of opioid dependence: a randomized trial. Jama. 281(11):1000-1005.
215. Bearn J, Gossop M and Strang J (1996). Randomised double-blind comparison of lofexidine and methadone in the in-patient treatment of opiate withdrawal. Drug and Alcohol Dependence. 43(1-2):87-91.
216. Howells C, Allen S, Gupta J, Stillwell G, Marsden J and Farrell M (2002). Prison based detoxification for opioid dependence: a randomised double blind controlled trial of lofexidine and methadone. Drug and Alcohol Dependence. 67(2):169-176.
217. Kleber HD, Riordan CE, Rounsaville B, Kosten T, Charney D, Gaspari J, Hogan I and O'Connor C (1985). Clonidine in outpatient detoxification from methadone maintenance. Archives of General Psychiatry. 42(4):391-394.
218. San L, Cami J, Peri JM, Mata R and Porta M (1990). Efficacy of clonidine, guanfacine and methadone in the rapid detoxification of heroin addicts: a controlled clinical trial. British Journal of Addiction. 85(1):141-147.
219. San L, Fernandez T, Cami J and Gossop M (1994). Efficacy of methadone versus methadone and guanfacine in the detoxification of heroin-addicted patients. Journal of Substance Abuse Treatment. 11(5):463-469.
220. Umbricht A, Hoover DR, Tucker MJ, Leslie JM, Chaisson RE and Preston KL (2003). Opioid detoxification with buprenorphine, clonidine, or methadone in hospitalized heroin-dependent patients with HIV infection. Drug and Alcohol Dependence. 69(3):263-272.
221. Washton AM and Resnick RB (1981). Clonidine vs. methadone for opiate detoxification: double-blind outpatient trials. NIDA Research Monograph. 34:89-94.
222. Gowing L, Farrell M, Ali R and White J (2004). Alpha2 adrenergic agonists for the management of opioid withdrawal. Cochrane Database Systematic Review.(4):CD002024. ASHP.
223. Seifert J, Metzner C, Paetzold W, Borsutzky M, Passie T, Rollnik J, Wiese B, Emrich HM and Schneider U (2002). Detoxification of opiate addicts with multiple drug abuse: a comparison of buprenorphine vs. methadone. Pharmacopsychiatry, 35(5):159-164.
224. Amato L, Davoli M, Ferri M and Ali R (2004). Methadone at tapered doses for the management of opioid withdrawal. Cochrane Database Systematic Review.(4):CD003409.
225. Cheskin LJ, Fudala PJ and Johnson RE (1994). A controlled comparison of buprenorphine and clonidine for acute detoxification from opioids. Drug and Alcohol Dependence. 36(2):115-121.
226. Ling W, Amass L, Shoptaw S, Annon JJ, Hillhouse M, Babcock D, Brigham G, Harrer J, Reid M, Muir J, Buchan B, Orr D, Woody G, Krejci J and Ziedonis D (2005). A multi-center randomized trial of buprenorphine-naloxone versus clonidine for opioid detoxification: findings from the National Institute on Drug Abuse Clinical Trials Network. Addiction. 100(8):1090-1100.
227. Nigam AK, Ray R and Tripathi BM (1993). Buprenorphine in opiate withdrawal: a comparison with clonidine. Journal of Substance Abuse Treatment. 10(4):391-394.
228. Fingerhood MI, Thompson MR and Jasinski DR (2001). A Comparison of Clonidine and Buprenorphine in the Outpatient Treatment of Opiate Withdrawal. Substance Abuse. 22(3):193-199.
229. Janiri L, Mannelli P, Persico AM, Serretti A and Tempesta E (1994). Opiate detoxification of methadone maintenance patients using lefetamine, clonidine and buprenorphine. Drug and Alcohol Dependence. 36(2):139-145.
230. Lintzeris N, Bell J, Bammer G, Jolley DJ and Rushworth L (2002). A randomized controlled trial of buprenorphine in the management of short-term ambulatory heroin withdrawal. Addiction. 97(11):1395-1404.
231. O'Connor PG, Carroll KM, Shi JM, Schottenfeld RS, Kosten TR and Rounsaville BJ (1997). Three methods of opioid detoxification in a primary care setting. A randomized trial. Annals of Internal Medicine. 127(7):526-530.
232. Beswick T, Best D, Bearn J, Gossop M, Rees S and Strang J (2003). The effectiveness of combined naloxone/lofexidine in opiate detoxification: results from a double-blind randomized and placebo-controlled trial. American Journal of Addiction. 12(4):295-305.
233. Gerra G, Marcato A, Caccavari R, Fontanesi B, Delsignore R, Fertonani G, Avanzini P, Rustichelli P and Passeri M (1995). Clonidine and opiate receptor antagonists in the treatment of heroin addiction. Journal of Substance Abuse Treatment. 12(1):35-41.
234. Gerra G, Zaimovic A, Rustichelli P, Fontanesi B, Zambelli U, Timpano M, Bocchi C and Delsignore R (2000). Rapid opiate detoxication in outpatient treatment: relationship with naltrexone compliance. Journal of Substance Abuse Treatment. 18(2):185-191.
235. Bearn J, Bennett J, Martin T, Gossop M and Strang J (2001). The impact of naloxone/lofexidine combination treatment on the opiate withdrawal syndrome. Addiction Biology. 6(2):147-156.
236. Buntwal N, Bearn J, Gossop M and Strang J (2000). Naltrexone and lofexidine combination treatment compared with conventional lofexidine treatment for in-patient opiate detoxification. Drug and Alcohol Dependence. 59(2):183-188.
237. O'Connor PG, Waugh ME, Carroll KM, Rounsaville BJ, Diagkogiannis IA and Schottenfeld RS (1995). Primary care-based ambulatory opioid detoxification: the results of a clinical trial. Journal of General Internal Medicine. 10(5):255-260.
238. Wilson BK, Elms RR and Thomson CP (1975). Outpatient vs hospital methadone detoxification: an experimental comparison. International Journal of Addiction. 10(1):13-21.
239. Curran S and Savage C (1976). Patient response to naltrexone: issues of acceptance, treatment effects, and frequency of administration. NIDA Research Monograph.(9):67-69.
240. Krupitsky EM, Zvartau EE, Masalov DV, Tsoi MV, Burakov AM, Egorova VY, Didenko TY, Romanova TN, Ivanova EB, Bespalov AY, Verbitskaya EV, Neznanov NG, Grinenko AY, O'Brien CP and Woody GE (2004). Naltrexone for heroin dependence treatment in St. Petersburg, Russia. Journal of Substance Abuse Treatment. 26(4):285-294.
241. Lerner A, Sigal M, Bacalu A, Shiff R, Burganski I and Gelkopf M (1992). A naltrexone double blind placebo controlled study in Israel. Israeli Journal of Psychiatry and Related Sciences. 29(1):36-43.
242. San L, Pomarol G, Peri JM, Olle JM and Cami J (1991). Follow-up after a six-month maintenance period on naltrexone versus placebo in heroin addicts. British Journal of Addiction. 86(8):983-990.
243. Shufman EN, Porat S, Witztum E, Gandacu D, Bar-Hamburger R and Ginath Y (1994). The efficacy of naltrexone in preventing reabuse of heroin after detoxification. Biological Psychiatry. 35(12):935-945.
244. Guo S, Jiang Z and Wu Y (2001). Efficacy of naltrexone Hydrochloride for preventing relapse among opiate-dependent patients after detoxication. Hong Kong Journal of Psychiatry. 11(4):2-8.
245. Cornish JW, Metzger D, Woody GE, Wilson D, McLellan AT, Vandergrift B and O'Brien CP (1997). Naltrexone pharmacotherapy for opioid dependent federal probationers. Journal of Substance Abuse Treatment. 14(6):529-534.
246. Rawson RA, Glazer M, Callahan EJ and Liberman RP (1979). Naltrexone and behavior therapy for heroin addiction. NIDA Research Monograph.(25):26-43.
247. Abrahms JL (1979). A cognitive-behavioral versus nondirective group treatment program for opioid-addicted persons: an adjunct to methadone maintenance. International Journal of Addiction. 14(4):503-511.
248. Khatami M, Woody G, O'Brien C and Mintz J (1982). Biofeedback treatment of narcotic addiction: a double-blind study. Drug and Alcohol Dependence. 9(2):111-117.
249. Milby JB, Garrett C, English C, Fritschi O and Clarke C (1978). Take-home methadone: contingency effects on drug-seeking and productivity of narcotic addicts. Addictive Behaviors. 3(3-4):215-220.
250. Rounsaville BJ, Glazer W, Wilber CH, Weissman MM and Kleber HD (1983). Short-term interpersonal psychotherapy in methadone-maintained opiate addicts. Archives of General Psychiatry. 40(6):629-636.
251. Stitzer ML, Iguchi MY and Felch LJ (1992). Contingent take-home incentive: effects on drug use of methadone maintenance patients. Journal of Consulting and Clinical Psychology. 60(6):927-934.
252. Thornton PI, Igleheart HC and Silverman LH (1987). Subliminal stimulation of symbiotic fantasies as an aid in the treatment of drug abusers. International Journal of Addiction. 22(8):751-765.
253. Woody GE, McLellan AT, Luborsky L and O'Brien CP (1995). Psychotherapy in community methadone programs: a validation study. American Journal of Psychiatry. 152(9):1302-1308.
254. Abbott PJ, Weller SB, Delaney HD and Moore BA (1998). Community reinforcement approach in the treatment of opiate addicts. American Journal of Drug and Alcohol Abuse. 24(1):17-30.
255. Iguchi MY, Belding MA, Morral AR, Lamb RJ and Husband SD (1997). Reinforcing operants other than abstinence in drug abuse treatment: an effective alternative for reducing drug use. Journal of Consulting and Clinical Psychology. 65(3):421-428.
256. Woody GE, Luborsky L, McLellan AT, O'Brien CP, Beck AT, Blaine J, Herman I and Hole A (1983). Psychotherapy for opiate addicts. Does it help? Archives of General Psychiatry. 40(6):639-645.
257. Amato L, Minozzi S, Davoli M, Vecchi S, Ferri M and Mayet S (2004). Psychosocial combined with agonist maintenance treatments versus agonist maintenance treatments alone for treatment of opioid dependence. Cochrane Database Systematic Review.(4):CD004147.
258. Bickel WK, Amass L, Higgins ST, Badger GJ and Esch RA (1997). Effects of adding behavioral treatment to opioid detoxification with buprenorphine. Journal of Consulting and Clinical Psychology. 65(5):803-810.
259. Higgins ST, Stitzer ML, Bigelow GE and Liebson IA (1984). Contingent methadone dose increases as a method for reducing illicit opiate use in detoxification patients. NIDA Research Monograph. 55:178-184.
260. McCaul ME, Stitzer ML, Bigelow GE and Liebson IA (1984). Contingency management interventions: effects on treatment outcome during methadone detoxification. Journal of Applied Behavioral Analysis. 17(1):35-43.
261. Rawson RA, Mann AJ, Tennant FS, Jr. and Clabough D (1983). Efficacy of psychotherapeutic counselling during 21-day ambulatory heroin detoxification. NIDA Research Monograph. 43:310-314.
262. Robles E, Stitzer ML, Strain EC, Bigelow GE and Silverman K (2002). Voucher-based reinforcement of opiate abstinence during methadone detoxification. Drug and Alcohol Dependence. 65(2):179-189.
263. Yandoli D, Eisler I, Robbins C, Mulleady G and Dare C (2002). A comparative study of family therapy in the treatment of opiate users in a London drug clinic. The Association for Family Therapy and Systemic Practice. 24(4):402-422.
264. Dawe S, Powell J, Richards D, Gossop M, Marks I, Strang J and Gray JA (1993). Does post-withdrawal cue exposure improve outcome in opiate addiction? A controlled trial. Addiction. 88(9):1233-1245.
265. Gruber K, Chutuape MA and Stitzer ML (2000). Reinforcement-based intensive outpatient treatment for inner city opiate abusers: a short-term evaluation. Drug and Alcohol Dependence. 57(3):211-223.
266. Katz EC, Chutuape MA, Jones HE and Stitzer ML (2002). Voucher reinforcement for heroin and cocaine abstinence in an outpatient drug-free program. Experimental Clinical Psychopharmacology. 10(2):136-143.
267. Chiang CN and Hawks RL (2003). Pharmacokinetics of the combination tablet of buprenorphine and naloxone. Drug and Alcohol Dependence. 70(2 Suppl):S39-47.
268. Mendelson J, Jones RT, Fernandez I, Welm S, Melby AK and Baggott MJ (1996). Buprenorphine and naloxone interactions in opiate-dependent volunteers. Clinical Pharmacology and Therapeutics. 60(1):105-114.
269. Comer SD, Walker EA and Collins ED (2005). Buprenorphine/naloxone reduces the reinforcing and subjective effects of heroin in heroin-dependent volunteers. Psychopharmacology (Berl). 181(4):664-675.
270. Stoller KB, Bigelow GE, Walsh SL and Strain EC (2001). Effects of buprenorphine/naloxone in opioid-dependent humans. Psychopharmacology (Berl). 154(3):230-242.
271. Strain EC, Stoller K, Walsh SL and Bigelow GE (2000). Effects of buprenorphine versus buprenorphine/naloxone tablets in non-dependent opioid abusers. Psychopharmacology (Berl). 148(4):374-383.
272. Harris DS, Jones RT, Welm S, Upton RA, Lin E and Mendelson J (2000). Buprenorphine and naloxone co-administration in opiate-dependent patients stabilized on sublingual buprenorphine. Drug and Alcohol Dependence. 61(1):85-94.
273. Kim S, Wagner HN, Jr., Villemagne VL, Kao PF, Dannals RF, Ravert HT, Joh T, Dixon RB and Civelek AC (1997). Longer occupancy of opioid receptors by nalmefene compared to naloxone as measured in vivo by a dual-detector system. Journal of Nuclear Medicine. 38(11):1726-1731.
274. Arizona Center for Education and Research on Therapeutics (2008). Drugs that Prolong the QT Interval and/or Induce Torsades de Pointes Ventricular Arrhythmia. http://www.qtdrugs.org/medical-pros/drug-lists/drug-lists.cfm (Accessed 2008 July 16).
275. Eap CB, Buclin T and Baumann P (2002). Interindividual variability of the clinical pharmacokinetics of methadone: implications for the treatment of opioid dependence. Clinical Pharmacokinetics, 41(14):1153-1193.
276. Kharasch ED, Hoffer C, Whittington D and Sheffels P (2004). Role of hepatic and intestinal cytochrome P450 3A and 2B6 in the metabolism, disposition, and miotic effects of methadone. Clinical Pharmacology and Therapeutics. 76(3):250-269.
277. Lugo RA, Satterfield KL and Kern SE (2005). Pharmacokinetics of methadone. Journal of Pain and Palliative Care Pharmacotherapy. 19(4):13-24.
278. Eap CB, Buclin T and Baumann P (2002). Interindividual variability of the clinical pharmacokinetics of methadone: implications for the treatment of opioid dependence. Clinical Pharmacokinetics. 41(14):1153-1193.
279. Benmebarek M, Devaud C, Gex-Fabry M, Powell Golay K, Brogli C, Baumann P, Gravier B and Eap CB (2004). Effects of grapefruit juice on the pharmacokinetics of the enantiomers of methadone. Clinical Pharmacology and Therapeutics. 76(1):55-63.
280. Crettol S, Deglon JJ, Besson J, Croquette-Krokkar M, Gothuey I, Hammig R, Monnat M, Huttemann H, Baumann P and Eap CB (2005). Methadone enantiomer plasma levels, CYP2B6, CYP2C19, and CYP2C9 genotypes, and response to treatment. Clinical Pharmacology and Therapeutics. 78(6):593-604.
281. Crettol S, Deglon JJ, Besson J, Croquette-Krokar M, Hammig R, Gothuey I, Monnat M and Eap CB (2006). ABCB1 and cytochrome P450 genotypes and phenotypes: influence on methadone plasma levels and response to treatment. Clinical Pharmacology and Therapeutics. 80(6):668-681.
282. American Society of Health System Pharmacists (2006). American Hospital Formulary Service Drug Information
283. Wang JS and DeVane CL (2003). Involvement of CYP3A4, CYP2C8, and CYP2D6 in the metabolism of (R)- and (S)-methadone in vitro. Drug Metabolism and Disposition. 31(6):742-747.
284. World Health Organization (in press). Chronic HIV Care with ARV Therapy and Prevention including IDU_HIV Co-management: Interim Guidelines for Health Workers at Health Centre or Clinic at District Hospital Outpatient. Integrated Management of Adolescent and Adult Illness. Geneva, WHO.
285. World Health Organization (2006). Antiretroviral therapy for HIV infection in adults and adolescents: recommendations for a public health approach - 2006 rev. Geneva, WHO.
286. Panel on Antiretroviral Guidelines for Adults and Adolescents (2008). Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. http://www.aidsinfo.nih.gov/ContentFiles/AdultandAdolescentGL.pdf
287. Ferri M, Davoli M and Perucci CA (2003). Heroin maintenance for chronic heroin dependents. Cochrane Database Systematic Review. (4):CD003410.
288. Broomhead A, Kerr R, Tester W, O'Meara P, Maccarrone C, Bowles R and Hodsman P (1997). Comparison of a once-a-day sustained-release morphine formulation with standard oral morphine treatment for cancer pain.Journal of Pain Symptom Management. 14(2):63-73.
289. Gourlay GK, Cherry DA, Onley MM, Tordoff SG, Conn DA, Hood GM and Plummer JL (1997). Pharmacokinetics and pharmacodynamics of twenty-fourhourly Kapanol compared to twelve-hourly MS Contin in the treatment of severe cancer pain. Pain. 69(3):295-302.
290. Gourlay GK (1998). Sustained relief of chronic pain. Pharmacokinetics of sustained release morphine. Clinical Pharmacokinetics. 35(3):173-190.
291. Mitchell TB, White JM, Somogyi AA and Bochner F (2004). Slow-release oral morphine versus methadone: a crossover comparison of patient outcomes and acceptability as maintenance pharmacotherapies for opioid dependence. Addiction. 99(8):940-945.
292. Mitchell TB, White JM, Somogyi AA and Bochner F (2003). Comparative pharmacodynamics and pharmacokinetics of methadone and slow-release oral morphine for maintenance treatment of opioid dependence. Drug and Alcohol Dependence. 72(1):85-94.
293. Eder H, Jagsch R, Kraigher D, Primorac A, Ebner N and Fischer G (2005). Comparative study of the effectiveness of slow-release morphine and methadone for opioid maintenance therapy. Addiction. 100(8):1101-1109.
294. Clark N, Lintzeris N, Gijsbers A, Whelan G, Dunlop A, Ritter A and Ling W (2002). LAAM maintenance vs methadone maintenance for heroin dependence. Cochrane Database Systematic Review.(2):CD002210.
295. Longshore D, Annon J, Anglin MD and Rawson RA (2005). Levo-alpha-acetylmethadol (LAAM) versus methadone: treatment retention and opiate use. Addiction. 100(8):1131-1139.
296. Deamer RL, Wilson DR, Clark DS and Prichard JG (2001). Torsades de pointes associated with high dose levomethadyl acetate (ORLAAM). Journal of Addictive Diseases. 20(4):7-14.
297. Kang J, Chen XL, Wang H and Rampe D (2003). Interactions of the narcotic l-alpha-acetylmethadol with human cardiac K+ channels. European Journal of Pharmacology. 458(1-2):25-29.
298. Cazorla C, Grenier de Cardenal D, Schuhmacher H, Thomas L, Wack A, May T and Rabaud C (2005). [Infectious complications and misuse of high-dose buprenorphine]. Presse Médicale. 34(10):719-724.
299. Vidal-Trecan G, Varescon I, Nabet N and Boissonnas A (2003). Intravenous use of prescribed sublingual buprenorphine tablets by drug users receiving maintenance therapy in France. Drug and Alcohol Dependence. 69(2):175-181.
300. Obadia Y, Perrin V, Feroni I, Vlahov D and Moatti JP (2001). Injecting misuse of buprenorphine among French drug users. Addiction. 96(2):267-272.
301. Lavelle TL, Hammersley R and Forsyth A (1991). The use of buprenorphine and temazepam by drug injectors. Journal of Addictive Diseases. 10(3):5-14.
302. Robinson GM, Dukes PD, Robinson BJ, Cooke RR and Mahoney GN (1993). The misuse of buprenorphine and a buprenorphine-naloxone combination in Wellington, New Zealand. Drug and Alcohol Dependence. 33(1):81-86.
303. Alho H, Sinclair D, Vuori E and Holopainen A (2007). Abuse liability of buprenorphine-naloxone tablets in untreated IV drug users. Drug and Alcohol Dependence. 88(1):75-78.
304. Comer SD and Collins ED (2002). Self-administration of intravenous buprenorphine and the buprenorphine/naloxone combination by recently detoxified heroin abusers. Journal of Pharmacology and Experimental Therapeutics. 303(2):695-703.
305. Fudala PJ, Yu E, Macfadden W, Boardman C and Chiang CN (1998). Effects of buprenorphine and naloxone in morphine-stabilized opioid addicts. Drug and Alcohol Dependence. 50(1):1-8.
306. Kakko J, Gronbladh L, Svanborg KD, von Wachenfeldt J, Ruck C, Rawlings B, Nilsson LH and Heilig M (2007). A stepped care strategy using buprenorphine and methadone versus conventional methadone maintenance in heroin dependence: a randomized controlled trial. American Journal of Psychiatry. 164(5):797-803.
307. Fiellin DA, Pantalon MV, Chawarski MC, Moore BA, Sullivan LE, O'Connor PG and Schottenfeld RS (2006). Counseling plus buprenorphine-naloxone maintenance therapy for opioid dependence. New England Journal of Medicine. 355(4):365-374.
308. Amass L, Kamien JB and Mikulich SK (2001). Thrice-weekly supervised dosing with the combination buprenorphine-naloxone tablet is preferred to daily supervised dosing by opioid-dependent humans. Drug and Alcohol Dependence. 61(2):173-181.
309. Amass L, Kamien JB and Mikulich SK (2000). Efficacy of daily and alternate-day dosing regimens with the combination buprenorphine-naloxone tablet. Drug and Alcohol Dependence. 58(1-2):143-152.
310. Comer SD, Sullivan MA and Hulse GK (2007). Sustained-release naltrexone: novel treatment for opioid dependence. Expert opinion on Investigative Drugs. 16(8):1285-1294.
311. Sullivan MA, Garawi F, Bisaga A, Comer SD, Carpenter K, Raby WN, Anen SJ, Brooks AC, Jiang H, Akerele E and Nunes EV (2007). Management of relapse in naltrexone maintenance for heroin dependence. Drug and Alcohol Dependence. 91(2-3):289-92.
312. Sullivan MA, Vosburg SK and Comer SD (2006). Depot naltrexone: antagonism of the reinforcing, subjective, and physiological effects of heroin. Psychopharmacology (Berl). 189(1):37-46.
313. Comer SD, Sullivan MA, Yu E, Rothenberg JL, Kleber HD, Kampman K, Dackis C and O'Brien CP (2006). Injectable, sustained-release naltrexone for the treatment of opioid dependence: a randomized, placebo-controlled trial. Archives of General Psychiatry. 63(2):210-218.
314. Comer SD, Collins ED, Kleber HD, Nuwayser ES, Kerrigan JH and Fischman MW (2002). Depot naltrexone: long-lasting antagonism of the effects of heroin in humans. Psychopharmacology (Berl). 159(4):351-360.
315. Hulse GK, Tait RJ, Comer SD, Sullivan MA, Jacobs IG and Arnold-Reed D (2005). Reducing hospital presentations for opioid overdose in patients treated with sustained release naltrexone implants. Drug and Alcohol Dependence. 79(3):351-357.
316. Colquhoun R, Tan DY and Hull S (2005). A comparison of oral and implant naltrexone outcomes at 12 months. Journal of Opioid Management. 1(5):249-256.
317. Waal H, Frogopsahl G, Olsen L, Christophersen AS and Morland J (2006). Naltrexone implants - duration, tolerability and clinical usefulness. A pilot study. European Addiction Research. 12(3):138-144.
318. Foster J, Brewer C and Steele T (2003). Naltrexone implants can completely prevent early (1-month) relapse after opiate detoxification: a pilot study of two cohorts totalling 101 patients with a note on naltrexone blood levels. Addiction Biology. 8(2):211-217.
319. Anton B and Leff P (2006). A novel bivalent morphine/heroin vaccine that prevents relapse to heroin addiction in rodents. Vaccine. 24(16):3232-3240.
320. Kosten T and Owens SM (2005). Immunotherapy for the treatment of drug abuse. Pharmacology and Therapeutics. 108(1):76-85.
321. United Nations (1961). Single Convention on Narcotic Drugs 1961, As amended by the 1972 Protocol amending the Single Convention on Narcotic Drugs, 1961. http://www.incb.org/pdf/e/conv/convention_1961_en.pdf (Accessed 16 July 08).
322. United Nations Office on Drugs and Crime (1971). The Convention on Psychotropic Substances. http://www.unodc.org/pdf/convention_1971_en.pdf (Accessed 16 July 08).
323. World Health Organization (1996). Cancer Pain Relief with a Guide to Opioid Availability. http://www.painpolicy.wisc.edu/publicat/cprguid.htm (Accessed 14 July 2008).
324. International Narcotics Control Board (1989). Demand for and supply of opiates for medical and scientific needs. New York, United Nations.
325. Handelsman L, Cochrane KJ, Aronson MJ, Ness R, Rubinstein KJ and Kanof PD (1987). Two new rating scales for opiate withdrawal. American Journal of Drug and Alcohol Abuse. 13(3):293-308.
326. Wesson DR and Ling W (2003). The Clinical Opiate Withdrawal Scale (COWS). Journal of Psychoactive Drugs. 35(2):253-259.
327. Finnegan L (1980). Drug Dependence in Pregnancy. London, Castle House Publications
328. Schottenfeld, R. S., Chawarski M.C., Pakes J.R., Pantalon M.V., Carroll K.M., & Kosten T.. (2005). Methadone versus buprenorphine with contingency management or performance feedback for cocaine and opioid dependence. Archives of General Psychiatry, 162(2), 340-9.
329. Johnson, R. E., Jaffe, J. H., & Fudala, P. J. (1992). A controlled trial of buprenorphine treatment for opioid dependence. Jama, 267(20), 2750-2755.
330. Ling, W., Wesson, D. R., Charuvastra, C., & Klett, C. J. (1996). A controlled trial comparing buprenorphine and methadone maintenance in opioid dependence. Archives of General Psychiatry, 53(5), 401-407.
331. Oliveto, A. H., Feingold, A., Schottenfeld, R., Jatlow, P., & Kosten, T. R. (1999). Desipramine in opioid-dependent cocaine abusers maintained on buprenorphine vs methadone. Archives of General Psychiatry, 56(9), 812-820.
332. Pani, P. P., Maremmani, I., Pirastu, R., Tagliamonte, A., & Gessa, G. L. (2000). Buprenorphine: A controlled clinical trial in the treatment of opioid dependence. Drug and Alcohol Dependence, 60(1), 39-50.
333. Mattick, R. P., Ali, R., White, J. M., O'Brien, S., Wolk, S., & Danz, C. (2003). Buprenorphine versus methadone maintenance therapy: a randomized doubleblind trial with 405 opioid-dependent patients. Addiction, 98(4), 441-452.